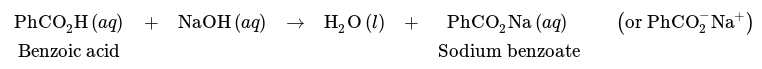G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,654
- Solutions
- 3
- Reaction score
- 2,732
- Points
- 113
- Deals
- 1
Ekstraktionsteori.
"Ekstraktion" henviser til overførsel af stoffer fra et fast stof eller en væske til et andet opløsningsmiddel eller en anden fase. Når en tepose tilsættes varmt vand, ekstraheres de stoffer, der er ansvarlige for teens smag og farve, fra kaffen til vandet. Koffeinfri kaffe fremstilles ved at bruge opløsningsmidler eller superkritisk kuldioxid til at trække koffeinen ud af kaffebønnerne. I kemilaboratoriet er det mest almindeligt at bruge væske-væske-ekstraktion, en proces, der foregår i en skilletragt. En opløsning, der indeholder opløste komponenter, placeres i tragten, og der tilsættes et ikke-blandbart opløsningsmiddel, hvilket resulterer i to lag, der rystes sammen. Det er mest almindeligt, at det ene lag er vandigt, og det andet er et organisk opløsningsmiddel. Komponenter "ekstraheres", når de bevæger sig fra det ene lag til det andet. Skilletragtens form giver mulighed for effektiv dræning og adskillelse af de to lag.
Fig. 1 Skematisk fremstilling af ekstraktion

Forbindelser bevæger sig fra en væske til en anden afhængigt af deres relative opløselighed i hver væske. En hurtig guide til opløselighed er "lignende opløser lignende"-princippet, hvilket betyder, at upolære forbindelser let bør kunne ekstraheres i upolære opløsningsmidler (og omvendt). De forbindelser, der er ansvarlige for teens smag og farve, må være polære, hvis de let kan trækkes ud i varmt vand. Når man lader to væsker stå i ligevægt i en skilletragt, ender størstedelen af en forbindelse ofte i det lag, hvor den er mest opløselig.
Fig. 2

Trin-for-trin-procedurer for ekstraktioner.
Væske-væske-ekstraktion
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/threads/extraction.553/
Enkelt ekstraktion.
Billederne i dette afsnit viser en enkelt ekstraktion af methylrødt (farvet forbindelse, fig. 3) fra en vandig opløsning (nederste lag) til 25 ml ethylacetat (øverste lag). Den vandige opløsning har oprindeligt en lyserød farve, da methylrødt fremstår rødt i en sur opløsning (den vandige opløsning blev fremstillet af 50 ml vand, 5 dråber 0,1 MHCl og 5 dråber 1 % methylrødt-indikatoropløsning). Methylrødt har en stor fordelingskoefficient og ekstraheres fra det vandige lag til ethylacetatet i denne proces.
Forløbet af ekstraktionen af methylrødt (den farvede forbindelse) fra det sure vandige lag (nederst) til det organiske lag (øverst). Inversionerne blev foretaget langsomt for at se ekstraktionen trinvis. Selv ved forsigtig omrøring ekstraheres methylrødt hurtigt.


Forbered opsætningen (til enkelt ekstraktion)
1. Find en skilletragt frem (fig. 4 a).- a) Hvis skilletragten har en teflon-stophane, skal du samle stophanen igen, hvis den blev taget fra hinanden for at tørre, og placere delene i den rigtige rækkefølge (fig. 4 b). Sørg for, at teflonhanen er moderat stram, så den stadig let kan drejes, men ikke er så løs, at der kan sive væske ud omkring samlingen.
- b) Hvis du bruger en glasstophane (fig. 4 c), behøver den sandsynligvis ikke yderligere forberedelse. Der skal bruges et meget tyndt lag fedt til at forsegle stophanen og forhindre frysning. Hvis både glas- og teflonpropper er tilgængelige, er teflon et bedre valg, da der altid er en mulighed for, at opløsningsmiddel kan opløse fedtet, der bruges med glaspropper, og kontaminere prøven.
- c) Anskaf også en prop (teflon eller slebet glas), der passer godt i tragtens øverste led (fig. 4 a).
2. Anbring skilletragten i en ringklemme, der er fastgjort til et ringstativ eller gitterværk. Tragtene er lette at knække, så polstr tragten i metalklemmen med stykker af opskåret gummi- eller plastikslange (fig. 4 d).
Fig.

a) Skilletragt, b) Korrekt rækkefølge af stophanekomponenter, c) Glasstophane, d) Tragt i polstret ringklemme.Tilsæt opløsningerne (til enkelt ekstraktion)
3. Før du hælder noget i en skilletragt, skal du sikre dig, at stophanen er i den "lukkede" position, hvor stophanen er vandret (fig. 5 a). Som en sikkerhedsforanstaltning skal du altid placere en Erlenmeyer-kolbe under skilletragten, før du hælder (fig. 5 b). Den kan opsamle væsken, hvis stophanen ved et uheld bliver efterladt åben, eller hvis stophanen er løs, og der utilsigtet løber væske ud.
4. Brug en tragt til at hælde den væske, der skal udvindes, i skilletragten (fig. 5 b). En skilletragt må aldrig bruges til varm væske. Den slebne glasfuge på toppen af en skilletragt er mere tilbøjelig til at klæbe til proppen, hvis der har været væske i fugen på et tidspunkt. Hvis man hælder væske i skilletragten med en kortskaftet tragt, undgår man at gøre fugen våd, så der er mindre risiko for, at den fryser til under blandingen.
3. Før du hælder noget i en skilletragt, skal du sikre dig, at stophanen er i den "lukkede" position, hvor stophanen er vandret (fig. 5 a). Som en sikkerhedsforanstaltning skal du altid placere en Erlenmeyer-kolbe under skilletragten, før du hælder (fig. 5 b). Den kan opsamle væsken, hvis stophanen ved et uheld bliver efterladt åben, eller hvis stophanen er løs, og der utilsigtet løber væske ud.
4. Brug en tragt til at hælde den væske, der skal udvindes, i skilletragten (fig. 5 b). En skilletragt må aldrig bruges til varm væske. Den slebne glasfuge på toppen af en skilletragt er mere tilbøjelig til at klæbe til proppen, hvis der har været væske i fugen på et tidspunkt. Hvis man hælder væske i skilletragten med en kortskaftet tragt, undgår man at gøre fugen våd, så der er mindre risiko for, at den fryser til under blandingen.
Hæld en mængde af det ekstraherende opløsningsmiddel i skilletragten, som angivet i proceduren (fig. 5 c). Det er ikke nødvendigt at bruge præcise mængder opløsningsmiddel til ekstraktioner, og mængderne kan måles i en gradueret cylinder. Hvis en procedure kræver 20 ml opløsningsmiddel, er det acceptabelt, hvis der bruges mellem 20 og 25 ml hver gang.
Bland opløsningerne (til enkelt ekstraktion)
6. Sæt proppen på tragten, og hold tragten, så den ene hånds fingre dækker proppen, mens den anden hånd griber fat i bunden af tragten (fig. 6 a).
7. Vend forsigtigt tragten om (fig. 6 b), og rør lidt rundt i blandingen. Selv om det ikke er ualmindeligt, at der siver lidt væske ned i den slebne glasfuge, når den vendes, bør det være minimalt. Hvis der drypper væske på dine fingre eller handsker, når du vender tragten, er proppen sandsynligvis den forkerte størrelse.
Bland opløsningerne (til enkelt ekstraktion)
6. Sæt proppen på tragten, og hold tragten, så den ene hånds fingre dækker proppen, mens den anden hånd griber fat i bunden af tragten (fig. 6 a).
7. Vend forsigtigt tragten om (fig. 6 b), og rør lidt rundt i blandingen. Selv om det ikke er ualmindeligt, at der siver lidt væske ned i den slebne glasfuge, når den vendes, bør det være minimalt. Hvis der drypper væske på dine fingre eller handsker, når du vender tragten, er proppen sandsynligvis den forkerte størrelse.
8. Der kan opbygges et tryk i skilletragten, når opløsningerne blandes, så umiddelbart efter omrystningen, og mens tragten stadig vender på hovedet, skal du "udlufte" tragten ved kortvarigt at åbne stophanen, så trykket kan slippe ud (fig. 6 c). Trykket opbygges i tragten, når opløsningsmidlet fordamper ind i hovedrummet og bidrager med yderligere damp til det oprindelige lufttryk på ca. 1 atmosfære i tragten. Med meget flygtige opløsningsmidler (som diethylether) kan der høres et tydeligt "swoosh" ved udluftning, og små mængder væske kan endda sprøjte ud af stophanen. Hvis der sprøjter væske ud af stophanen, skal du prøve at lade den løbe tilbage i tragten. Støjen i forbindelse med udluftning ophører normalt efter anden eller tredje invertering, da hovedrummet bliver mættet med opløsningsmiddeldampe, og trykket inden i og uden for tragten udlignes.
Sikkerhedsanbefaling: Ret aldrig stophanen mod nogen, mens du udlufter, da det er muligt, at der sprøjter væske på ham eller hende.
9. Luk stophanen, og bland opløsningerne lidt kraftigere, og stop jævnligt for at udlufte systemet. Der er forskellige meninger om, hvor kraftigt opløsninger skal blandes i skilletragte, og hvor længe de skal blandes. Som en generel vejledning bør en mild blanding i 10-20 sekunder være nok. Med nogle opløsninger (f.eks. dichlormethan) skal man passe på ikke at ryste for kraftigt, da disse opløsninger ofte danner emulsioner (hvor grænsefladen mellem opløsningerne ikke er klar). Med opløsninger, der er tilbøjelige til at danne emulsioner, skal en tragt vugges forsigtigt i et minut.
10. Placer skilletragten lodret i ringklemmen, så lagene kan adskilles helt. Grænsefladen mellem lagene bør falde til ro ret hurtigt, ofte inden for 10 sekunder eller deromkring. Hvis grænsefladen er uklar eller ikke veldefineret (der er dannet en emulsion), kan du finde tips i afsnittet om fejlfinding.
Adskil lagene (ved enkelt ekstraktion)
11. Væske vil ikke løbe godt ud af en skilletragt, hvis proppen forbliver på, da der ikke kan komme luft ind i tragten til at erstatte den fortrængte væske. Hvis væsken løber ud af tragten uden at blive erstattet af en tilsvarende mængde luft, vil der opstå et undertryk i tragten. Derfor skal proppen fjernes, før der tappes væske fra en skilletragt (fig. 7 a).
12. Tøm størstedelen af bundlaget over i en ren Erlenmeyer-kolbe, og placer ringklemmen, så spidsen af skilletragten ligger i Erlenmeyer-kolben for at forhindre sprøjt (fig. 7 b). Stop aftapningen, når grænsefladen er inden for 1 cm fra bunden af stophanen.
13. Drej forsigtigt tragten for at løsne eventuelle dråber, der klæber til glasset (fig. 7 c). En glasomrører kan bruges til at slå genstridige dråber ned.
14. Dræn desuden det nederste lag, og stop, når grænsefladen lige kommer ind i stophanens kammer (fig. 7 d). Mærk Erlenmeyer-kolben (f.eks. "bundlag").
Sikkerhedsanbefaling: Ret aldrig stophanen mod nogen, mens du udlufter, da det er muligt, at der sprøjter væske på ham eller hende.
9. Luk stophanen, og bland opløsningerne lidt kraftigere, og stop jævnligt for at udlufte systemet. Der er forskellige meninger om, hvor kraftigt opløsninger skal blandes i skilletragte, og hvor længe de skal blandes. Som en generel vejledning bør en mild blanding i 10-20 sekunder være nok. Med nogle opløsninger (f.eks. dichlormethan) skal man passe på ikke at ryste for kraftigt, da disse opløsninger ofte danner emulsioner (hvor grænsefladen mellem opløsningerne ikke er klar). Med opløsninger, der er tilbøjelige til at danne emulsioner, skal en tragt vugges forsigtigt i et minut.
10. Placer skilletragten lodret i ringklemmen, så lagene kan adskilles helt. Grænsefladen mellem lagene bør falde til ro ret hurtigt, ofte inden for 10 sekunder eller deromkring. Hvis grænsefladen er uklar eller ikke veldefineret (der er dannet en emulsion), kan du finde tips i afsnittet om fejlfinding.
Adskil lagene (ved enkelt ekstraktion)
11. Væske vil ikke løbe godt ud af en skilletragt, hvis proppen forbliver på, da der ikke kan komme luft ind i tragten til at erstatte den fortrængte væske. Hvis væsken løber ud af tragten uden at blive erstattet af en tilsvarende mængde luft, vil der opstå et undertryk i tragten. Derfor skal proppen fjernes, før der tappes væske fra en skilletragt (fig. 7 a).
12. Tøm størstedelen af bundlaget over i en ren Erlenmeyer-kolbe, og placer ringklemmen, så spidsen af skilletragten ligger i Erlenmeyer-kolben for at forhindre sprøjt (fig. 7 b). Stop aftapningen, når grænsefladen er inden for 1 cm fra bunden af stophanen.
13. Drej forsigtigt tragten for at løsne eventuelle dråber, der klæber til glasset (fig. 7 c). En glasomrører kan bruges til at slå genstridige dråber ned.
14. Dræn desuden det nederste lag, og stop, når grænsefladen lige kommer ind i stophanens kammer (fig. 7 d). Mærk Erlenmeyer-kolben (f.eks. "bundlag").
Fig.

a) Proppen tages af, før tragten tømmes, b) Tømning til grænsefladen, c) Klæbende dråber (ved hjælp af et andet system), d) Stop, når grænsefladen er i stophanen.15. Hæld det øverste lag fra toppen af skilletragten over i en anden ren Erlenmeyer-kolbe (fig. 8 a), og sørg for at mærke denne kolbe igen (fig. 8 b). Det er korrekt teknik at dræne det nederste lag gennem stophanen og hælde det øverste lag ud fra toppen af tragten. Denne metode minimerer genblanding af opløsningerne, da kun det nederste lag rører ved tragtens stilk.
16. Smid aldrig væsker fra en ekstraktion væk, før du er helt sikker på, at du har den ønskede forbindelse. Uønskede lag kan bortskaffes korrekt, når den ønskede forbindelse er i dine hænder (f.eks. efter at den roterende fordamper har fjernet opløsningsmidlet).
Fejl begået under ekstraktioner (f.eks. at fortsætte med det forkerte lag) kan løses, så længe opløsningerne ikke er blevet anbragt i affaldsbeholderen! Lagene bør også gemmes til efter inddampning, fordi den ønskede forbindelse måske ikke er særlig opløselig i det anvendte opløsningsmiddel. Hvis forbindelsen ikke kan ekstraheres i et opløsningsmiddel, kan man prøve med et andet opløsningsmiddel senere, men igen kun hvis lagene endnu ikke er blevet smidt væk.
Oprydning (ved enkelt ekstraktion)
For at rengøre en skilletragt skal du først skylle den med acetone i en affaldsbeholder. Vask derefter tragten med vand og sæbe på bænken. Afmonter teflon-stophanen (hvis den bruges). Efter skylning med destilleret vand skal du lade delene tørre adskilt i dit skab (fig. 8 c).
Fejl begået under ekstraktioner (f.eks. at fortsætte med det forkerte lag) kan løses, så længe opløsningerne ikke er blevet anbragt i affaldsbeholderen! Lagene bør også gemmes til efter inddampning, fordi den ønskede forbindelse måske ikke er særlig opløselig i det anvendte opløsningsmiddel. Hvis forbindelsen ikke kan ekstraheres i et opløsningsmiddel, kan man prøve med et andet opløsningsmiddel senere, men igen kun hvis lagene endnu ikke er blevet smidt væk.
Oprydning (ved enkelt ekstraktion)
For at rengøre en skilletragt skal du først skylle den med acetone i en affaldsbeholder. Vask derefter tragten med vand og sæbe på bænken. Afmonter teflon-stophanen (hvis den bruges). Efter skylning med destilleret vand skal du lade delene tørre adskilt i dit skab (fig. 8 c).
Flere ekstraktioner.
I dette afsnit er der trinvise instruktioner om, hvordan man ekstraherer en vandig opløsning med et organisk opløsningsmiddel, der er mindre tæt end vand (det organiske lag vil være øverst). Som et eksempel er instruktionerne skrevet for at ekstrahere en vandig opløsning tre gange ved at bruge 25 ml diethylether hver gang (3×25 ml diethylether). En oversigt over fremgangsmåden ved de to første ekstraktioner findes i Fig.9 To ekstraktioner, når det organiske lag ligger øverst.
Fig.det organiske lag er øverst.

Ekstraktion #1
1. Udfør en enkelt ekstraktion med ca. 25 ml diethylether (en nøjagtig mængde er ikke nødvendig), som beskrevet tidligere, og sørg for at mærke hvert lag korrekt (f.eks. "øverste organiske lag" og "nederste vandige lag").
Ekstraktion nr. 2
2. Sæt det vandige lag tilbage i skilletragten. Det er ikke nødvendigt at vaske tragten mellem ekstraktionerne.
3. Tilsæt en ny 25 ml portion diethylether til skilletragten. Luk tragten, vend den om og ryst den med udluftning, og lad så lagene skille sig ad.
På dette trin skal der være to lag i skilletragten. Hvis der ikke er to lag, er det sandsynligt, at det forkerte lag blev tilsat tragten i trin 2 (en almindelig fejl). En måde at teste, om det var fejlen, er at tilsætte lidt vand fra en sprøjteflaske. Hvis det lag, der returneres til skilletragten, er det organiske lag (forkert), vil vandet fra sprøjteflasken ikke blande sig med opløsningen, men i stedet falde til bunds som dråber. Hvis det organiske lag (forkert) ved et uheld blev returneret til skilletragten, er der ingen skade sket, da det organiske lag blot blev fortyndet. Hæld væsken tilbage i kolben, der er beregnet til det organiske lag, og tilsæt i stedet den vandige opløsning til tragten.
4. Tøm det nederste vandige lag over i en Erlenmeyer-kolbe: Det er acceptabelt at bruge den samme kolbe, som blev brugt til det vandige lag i den første ekstraktion (som måske var mærket "nederste vandige lag").
5. Da det er mest almindeligt at kombinere de organiske lag i flere ekstraktioner, kan det øverste organiske lag hældes ud af skilletragten og over i den samme kolbe, som blev brugt til det organiske lag i den første ekstraktion (som kan være mærket "øverste organiske lag"). I denne kolbe bør der være ca. 50 ml diethylether fra de to ekstraktioner.
Ekstraktion nr. 3
6. Gentag ekstraktionen en tredje gang ved at tilsætte det vandige lag fra den anden ekstraktion til skilletragten efterfulgt af endnu en frisk portion på 25 ml diethylether. Luk tragten, vend den om og ryst den med udluftning, og lad derefter lagene adskilles.
7. Tøm det vandige lag over i den relevante kolbe, og hæld igen det øverste lag over i kolben med det organiske lag, hvor der bør være ca. 75 ml diethylether fra de tre ekstraktioner.
1. Udfør en enkelt ekstraktion med ca. 25 ml diethylether (en nøjagtig mængde er ikke nødvendig), som beskrevet tidligere, og sørg for at mærke hvert lag korrekt (f.eks. "øverste organiske lag" og "nederste vandige lag").
Ekstraktion nr. 2
2. Sæt det vandige lag tilbage i skilletragten. Det er ikke nødvendigt at vaske tragten mellem ekstraktionerne.
3. Tilsæt en ny 25 ml portion diethylether til skilletragten. Luk tragten, vend den om og ryst den med udluftning, og lad så lagene skille sig ad.
På dette trin skal der være to lag i skilletragten. Hvis der ikke er to lag, er det sandsynligt, at det forkerte lag blev tilsat tragten i trin 2 (en almindelig fejl). En måde at teste, om det var fejlen, er at tilsætte lidt vand fra en sprøjteflaske. Hvis det lag, der returneres til skilletragten, er det organiske lag (forkert), vil vandet fra sprøjteflasken ikke blande sig med opløsningen, men i stedet falde til bunds som dråber. Hvis det organiske lag (forkert) ved et uheld blev returneret til skilletragten, er der ingen skade sket, da det organiske lag blot blev fortyndet. Hæld væsken tilbage i kolben, der er beregnet til det organiske lag, og tilsæt i stedet den vandige opløsning til tragten.
4. Tøm det nederste vandige lag over i en Erlenmeyer-kolbe: Det er acceptabelt at bruge den samme kolbe, som blev brugt til det vandige lag i den første ekstraktion (som måske var mærket "nederste vandige lag").
5. Da det er mest almindeligt at kombinere de organiske lag i flere ekstraktioner, kan det øverste organiske lag hældes ud af skilletragten og over i den samme kolbe, som blev brugt til det organiske lag i den første ekstraktion (som kan være mærket "øverste organiske lag"). I denne kolbe bør der være ca. 50 ml diethylether fra de to ekstraktioner.
Ekstraktion nr. 3
6. Gentag ekstraktionen en tredje gang ved at tilsætte det vandige lag fra den anden ekstraktion til skilletragten efterfulgt af endnu en frisk portion på 25 ml diethylether. Luk tragten, vend den om og ryst den med udluftning, og lad derefter lagene adskilles.
7. Tøm det vandige lag over i den relevante kolbe, og hæld igen det øverste lag over i kolben med det organiske lag, hvor der bør være ca. 75 ml diethylether fra de tre ekstraktioner.
Fejlfinding.
Dette afsnit beskriver almindelige problemer og løsninger i forbindelse med ekstraktioner.Der er kun ét lag
Den mest almindelige årsag til, at der kun er ét lag i en skilletragt, når der burde være to (som når proceduren siger, at man skal "adskille lagene"), er, at man har begået en fejl. Det, der sandsynligvis er sket, er, at det forkerte lag blev tilføjet til skilletragten - for eksempel blev det organiske lag ubevidst tilføjet i stedet for det vandige lag. Når der tilsættes organisk opløsningsmiddel til et organisk lag i skilletragten, bliver resultatet kun ét lag. Fejlen kan rettes, så længe lagene endnu ikke er blevet smidt væk! Hvis det rigtige lag tilsættes tragten, vil alt gå som planlagt. For at undgå at begå denne fejl i fremtiden skal du sørge for at mærke Erlenmeyer-kolberne. Sørg også for aldrig at smide et lag væk, før du er helt sikker på, at du har gjort alt korrekt.
En grund til, at der kun dannes ét lag i en skilletragt, er, hvis der er store mængder forbindelser til stede, som opløses i begge opløsningsmidler, f.eks. hvis der er store mængder ethanol til stede, som opløses godt i både vandige og organiske opløsningsmidler. I denne situation er det bedst at fjerne den problematiske forbindelse (dvs. ethanolen) på en rotationsfordamper før ekstraktionen.
Der er tre lag
Den mest almindelige årsag til tre lag i en skilletragt er utilstrækkelig blanding (fig. 10 a). Hvis tragten rystes kraftigere, vil den sandsynligvis lægge sig i to lag (fig. 10 b). Det er også muligt, at et tredje lag i midten er en emulsion, hvor de to lag ikke er helt adskilt.
Den mest almindelige årsag til, at der kun er ét lag i en skilletragt, når der burde være to (som når proceduren siger, at man skal "adskille lagene"), er, at man har begået en fejl. Det, der sandsynligvis er sket, er, at det forkerte lag blev tilføjet til skilletragten - for eksempel blev det organiske lag ubevidst tilføjet i stedet for det vandige lag. Når der tilsættes organisk opløsningsmiddel til et organisk lag i skilletragten, bliver resultatet kun ét lag. Fejlen kan rettes, så længe lagene endnu ikke er blevet smidt væk! Hvis det rigtige lag tilsættes tragten, vil alt gå som planlagt. For at undgå at begå denne fejl i fremtiden skal du sørge for at mærke Erlenmeyer-kolberne. Sørg også for aldrig at smide et lag væk, før du er helt sikker på, at du har gjort alt korrekt.
En grund til, at der kun dannes ét lag i en skilletragt, er, hvis der er store mængder forbindelser til stede, som opløses i begge opløsningsmidler, f.eks. hvis der er store mængder ethanol til stede, som opløses godt i både vandige og organiske opløsningsmidler. I denne situation er det bedst at fjerne den problematiske forbindelse (dvs. ethanolen) på en rotationsfordamper før ekstraktionen.
Der er tre lag
Den mest almindelige årsag til tre lag i en skilletragt er utilstrækkelig blanding (fig. 10 a). Hvis tragten rystes kraftigere, vil den sandsynligvis lægge sig i to lag (fig. 10 b). Det er også muligt, at et tredje lag i midten er en emulsion, hvor de to lag ikke er helt adskilt.
.10

a) Tre indledende lag som følge af utilstrækkelig blanding, b) To lag som følge af kraftigere blanding.Der er uopløseligt materiale ved grænsefladen.
En lille mængde uopløselig film mellem to lag er ikke ualmindeligt under en ekstraktion. Polymermaterialer har en tendens til at hvile mellem lagene, da interaktioner med opløsningsmidler minimeres ved grænsefladen. En mindre film er ikke noget, man skal bekymre sig om, for hvis en lille mængde kommer ind i det organiske lag, vil et efterfølgende tørrings- og filtreringstrin ofte fjerne den.
Grænsefladen kan ikke ses.
Af og til er forbindelserne i en skilletragt så mørke, at de skjuler grænsefladen mellem de to lag. Hvis det sker, er der flere metoder, der kan hjælpe dig med at se grænsefladen. En af dem er at holde skilletragten op mod lyset eller at lyse på glasset med en lommelygte (fig. 11 b). Ekstra lys giver dig nogle gange mulighed for at se grænsefladen. En anden metode er omhyggeligt at observere lagene, mens man vipper tragten frem og tilbage til siden (fig. 11 c). Dit øje kan nogle gange opfange subtile forskelle i den måde, væskerne flyder på. En tredje metode er at tilsætte lidt mere opløsningsmiddel til tragten for at fortynde et af lagene lidt, eller at tilsætte et andet opløsningsmiddel for at ændre brydningsindekset.
Lagene adskilles ikke godt (der dannes en emulsion)
Fig.

Emulsioner kan opstå af flere grunde.
1. Tætheden af hvert lag kan være så ens, at der er svag motivation for væskerne til at adskille sig.2. Der kan være sæbelignende forbindelser eller andre emulgeringsmidler til stede, som opløser nogle komponenter i hinanden.
Emulsioner kan være meget vanskelige at rette op på, og det er bedst, hvis de undgås i første omgang ved at ryste opløsninger, der er tilbøjelige til at danne emulsioner (f.eks. dichlormethan med stærkt basiske eller tætte opløsninger), forsigtigt i skilletragten. Hvis der alligevel dannes en emulsion, er der nogle måder at forsøge at afklare dem på.
- a) For milde emulsioner skal du forsigtigt hvirvle lagene rundt og forsøge at slå ophængte dråber ned med en glasrørepind.
- b) Lad opløsningen stå i et stykke tid (selv indtil næste laboratorieperiode), hvis det er muligt. Når der er tid nok, falder nogle opløsninger til ro af sig selv. Det er selvfølgelig ikke sikkert, at det er praktisk muligt.
- c) Brug en centrifuge til små mængder, hvis du har en til rådighed. En centrifuge fremskynder processen med at lade en emulsion bundfælde sig selv. Husk, at en centrifuge skal være afbalanceret, ellers kan den vakle af bænken. Fordel opløsningerne ligeligt ved at sætte rør med samme volumen over for hinanden i centrifugen.
- d) Hvis der dannes en emulsion, fordi de to lag har samme massefylde, så prøv at ændre massefylden i hvert lag for at gøre dem mere forskellige. For at gøre en emulsion klarere kan man forsøge at mindske densiteten i det øverste lag eller øge densiteten i det nederste lag. Hvis der f.eks. opstår en emulsion med ethylacetat (øverste lag) og en vandig opløsning (nederste lag), kan du tilsætte lidt NaCl. NaCl vil opløses i det vandige lag og øge densiteten af den vandige opløsning. Alternativt kan du tilsætte ekstra ethylacetat, som vil fortynde det organiske lag og sænke dets massefylde. Som en sidste udvej kan man tilsætte lidt pentan, som vil blande sig med det øverste organiske lag og mindske densiteten (pentan er et af de mindst tætte organiske opløsningsmidler). Tilsætning af pentan bruges som en sidste indsats, da det vil påvirke det organiske lags evne til at udtrække noget polære forbindelser negativt.
Hvis der opstår en emulsion med en vandig opløsning (øverste lag) og dichlormethan (nederste lag), skal man tilsætte lidt vand fra en sprøjteflaske for at fortynde det øverste lag og mindske dets tæthed. Denne metode fungerede godt til at klargøre emulsionen i Fig. 13 c, som det fremgår af Fig. 13 d. - c) Prøv at mindske opløseligheden af den ene komponent i den anden. En metode er at tilsætte NaCl eller NH4Cl til skilletragten, som opløses i det vandige lag og mindsker organiske forbindelsers evne til at opløses i vand ("saltning").
Syre-base-ekstraktion
Syre-base-ekstraktion
- G.Patton
- 2
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/threads/extraction.553/
Sådan fungerer de.
En modifikation af de ekstraktioner, der tidligere er omtalt i dette kapitel, er at udføre en kemisk reaktion i skilletragten for at ændre polariteten og dermed fordelingen af en forbindelse i det vandige og det organiske lag. En almindelig metode er at udføre en syre-base-reaktion, som kan omdanne nogle forbindelser fra neutrale til ioniske former (eller omvendt).
Forestil dig for eksempel, at en blanding af benzoesyre og cyclohexan opløses i et organisk opløsningsmiddel som ethylacetat i en skilletragt. For at adskille komponenterne kan man forsøge at vaske med vand for at fjerne benzoesyre, men benzoesyre er ikke særlig vandopløselig på grund af sin upolære aromatiske ring, og kun små mængder vil blive ekstraheret i det vandige lag (Fig. 14 a).
Forestil dig for eksempel, at en blanding af benzoesyre og cyclohexan opløses i et organisk opløsningsmiddel som ethylacetat i en skilletragt. For at adskille komponenterne kan man forsøge at vaske med vand for at fjerne benzoesyre, men benzoesyre er ikke særlig vandopløselig på grund af sin upolære aromatiske ring, og kun små mængder vil blive ekstraheret i det vandige lag (Fig. 14 a).
.14

Vask af en blanding af benzoesyre og cyclohexan med: a) vand, b) vandig NaOH.Adskillelse af en blanding af benzoesyre og cyclohexan er dog mulig ved hjælp af en vask med en base, såsom NaOH. På grund af sin sure natur kan benzoesyre undergå en reaktion med NaOH som følger, hvilket resulterer i carboxylatsaltet natriumbenzoat.
Opløselighedsegenskaberne for carboxylsyrer er væsentligt forskellige fra deres tilsvarende carboxylatsalte. Natriumsalicylat er ca. 350 gange mere opløseligt i vand end salicylsyre på grund af dets ioniske karakter (fig. 15), og det er temmelig uopløseligt i organiske opløsningsmidler som f.eks. diethylether.
Fig.

Derfor vil en vask med NaOH omdanne benzoesyre til dens ioniske carboxylatform, som derefter vil være mere opløselig i det vandige lag, hvilket gør det muligt at ekstrahere natriumbenzoat i det vandige lag. Cyclohexan vil forblive i det organiske lag, da det ikke har nogen affinitet for den vandige fase og heller ikke kan reagere med NaOH på nogen måde. På denne måde kan en blanding af benzoesyre og cyclohexan adskilles (fig. 14 b). Det vandige lag kan senere forsures med HCl(aq), hvis det ønskes, for at omdanne benzoesyren tilbage til sin neutrale form.
Vask med natriumbicarbonat
En syre-base-ekstraktion kan bruges til at ekstrahere carboxylsyrer fra det organiske lag til det vandige lag. Som omtalt i det foregående afsnit kan NaOH bruges til at omdanne en carboxylsyre til dens mere vandopløselige ioniske carboxylatform. Men hvis blandingen indeholder en ønsket forbindelse, der kan reagere med NaOH, skal der bruges en mildere base som f.eks. natriumbicarbonat. Der sker en lignende reaktion.
Vask med natriumbicarbonat
En syre-base-ekstraktion kan bruges til at ekstrahere carboxylsyrer fra det organiske lag til det vandige lag. Som omtalt i det foregående afsnit kan NaOH bruges til at omdanne en carboxylsyre til dens mere vandopløselige ioniske carboxylatform. Men hvis blandingen indeholder en ønsket forbindelse, der kan reagere med NaOH, skal der bruges en mildere base som f.eks. natriumbicarbonat. Der sker en lignende reaktion.
En forskel ved at bruge basen NaHCO3 i stedet for NaOH er, at biproduktet kulsyre (H2CO3) kan nedbrydes til vand og kuldioxidgas. Når man ryster en sur opløsning med natriumbicarbonat i en skilletragt, skal man sørge for at hvirvle forsigtigt og lufte ud oftere for at frigøre trykket fra gassen.
Et eksempel på en reaktion, hvor man ofte bruger natriumbikarbonatvask i oparbejdningen, er en Fischer-esterificeringsreaktion. For at demonstrere dette blev benzoesyre tilbagesvalet i ethanol sammen med koncentreret svovlsyre for at danne ethylbenzoat (fig. 16 a og b). En TLC-plade af reaktionsblandingen ved 1 times tilbagesvaling viste resterende ureageret carboxylsyre (fig. 16 c), hvilket ikke er ualmindeligt på grund af reaktionens energetik.
Et eksempel på en reaktion, hvor man ofte bruger natriumbikarbonatvask i oparbejdningen, er en Fischer-esterificeringsreaktion. For at demonstrere dette blev benzoesyre tilbagesvalet i ethanol sammen med koncentreret svovlsyre for at danne ethylbenzoat (fig. 16 a og b). En TLC-plade af reaktionsblandingen ved 1 times tilbagesvaling viste resterende ureageret carboxylsyre (fig. 16 c), hvilket ikke er ualmindeligt på grund af reaktionens energetik.
.16

a) Refluksreagenser, b) Reaktionsskema, c) TLC efter 1 times refluks, hvor den første bane (BA) er benzoesyre, den anden bane (Co) er co-spot, og den tredje bane (Pr) er reaktionsblandingen (kørt med 1:1 hexan:ethylacetat og visualiseret med UV-lys).Den resterende carboxylsyre kan fjernes fra det ønskede esterprodukt ved hjælp af en syre-base-ekstraktion i en skilletragt. En vask med natriumbicarbonat omdanner benzoesyre til den mere vandopløselige natriumbenzoatform og ekstraherer den i det vandige lag (fig. 17). Derudover neutraliserer natriumbicarbonatet den katalytiske syre i denne reaktion.
.

Natriumbicarbonat er at foretrække frem for NaOH i denne proces, da det er en meget svagere base; vask med NaOH kan forårsage hydrolyse af esterproduktet.
Blandinger af syrer og baser
Som det er blevet diskuteret tidligere, kan forbindelsers syre-base-egenskaber udnyttes til selektivt at udtrække visse forbindelser fra blandinger. Denne strategi kan udvides til andre eksemplerBlandinger af syrer og baser
Udvinding af baser
Basiske forbindelser som aminer kan udvindes fra organiske opløsninger ved at ryste dem med sure opløsninger for at omdanne dem til mere vandopløselige salte. På denne måde kan de ekstraheres fra et organisk lag til et vandigt lag.Udvinding af carboxylsyrer vs. phenoler
Som tidligere omtalt kan carboxylsyrer ekstraheres fra et organisk lag til et vandigt lag ved at ryste dem med basiske opløsninger, som omdanner dem til deres mere vandopløselige salte.
Som tidligere omtalt kan carboxylsyrer ekstraheres fra et organisk lag til et vandigt lag ved at ryste dem med basiske opløsninger, som omdanner dem til deres mere vandopløselige salte.
En lignende reaktion sker med fenoler (PhOH), og de kan også ekstraheres til et vandigt NaOH-lag (fig. 18 a).
Phenoler er dog betydeligt mindre sure end carboxylsyrer, og de er ikke sure nok til at reagere fuldstændigt med NaHCO3, som er en svagere base. Derfor kan en opløsning af bikarbonat bruges til at adskille blandinger af phenoler og carboxylsyrer (Fig.18 b).
Phenoler er dog betydeligt mindre sure end carboxylsyrer, og de er ikke sure nok til at reagere fuldstændigt med NaHCO3, som er en svagere base. Derfor kan en opløsning af bikarbonat bruges til at adskille blandinger af phenoler og carboxylsyrer (Fig.18 b).
.18

a) Ekstraktion af både carboxylsyrer og phenoler i 5% NaOH(aq), b) Ekstraktion af kun carboxylsyrer i 5% NaHCO3(aq).Ekstraktion af syre, base og neutrale forbindelser
De tidligere omtalte syre-base-egenskaber gør det muligt at rense en blanding, der indeholder sure (f.eks. RCO2H), basiske (f.eks. RNH2) og neutrale komponenter, gennem en række ekstraktioner, som opsummeret i figur 19 (hvor der anvendes et organisk opløsningsmiddel, der er mindre tæt end vand).
De tidligere omtalte syre-base-egenskaber gør det muligt at rense en blanding, der indeholder sure (f.eks. RCO2H), basiske (f.eks. RNH2) og neutrale komponenter, gennem en række ekstraktioner, som opsummeret i figur 19 (hvor der anvendes et organisk opløsningsmiddel, der er mindre tæt end vand).
Fig.


Det antages, at læsere, der udfører denne type forsøg, er fortrolige med at udføre enkelt- og multiplekstraktioner. I dette afsnit beskrives forskelle mellem generelle ekstraktionsprocedurer og den proces, der er opsummeret i Fig. 19.
1. Isolering af den sure komponent:
a) Når den sure komponent er i det vandige lag i en Erlenmeyer-kolbe, kan den omdannes tilbage til den neutrale komponent ved at tilsætte 2M HCl(aq), indtil opløsningen giver en pH på 3-4 (som bestemt med pH-papir). Hvis der er store mængder syre til stede, så forsuring ville kræve for stor en mængde 2M HCl(aq), kan koncentreret HCl(aq) i stedet tilsættes dråbevis. Lavere koncentrationer af Hcl(aq) er mindre farlige, men en stor forøgelse af volumenet af det vandige lag vil påvirke effektiviteten af de efterfølgende ekstraktioner og filtreringstrin.
b) Efter forsuring kan man gå to veje, afhængigt af om den sure komponent er fast eller flydende.
1. Isolering af den sure komponent:
a) Når den sure komponent er i det vandige lag i en Erlenmeyer-kolbe, kan den omdannes tilbage til den neutrale komponent ved at tilsætte 2M HCl(aq), indtil opløsningen giver en pH på 3-4 (som bestemt med pH-papir). Hvis der er store mængder syre til stede, så forsuring ville kræve for stor en mængde 2M HCl(aq), kan koncentreret HCl(aq) i stedet tilsættes dråbevis. Lavere koncentrationer af Hcl(aq) er mindre farlige, men en stor forøgelse af volumenet af det vandige lag vil påvirke effektiviteten af de efterfølgende ekstraktioner og filtreringstrin.
b) Efter forsuring kan man gå to veje, afhængigt af om den sure komponent er fast eller flydende.
- Hvis der dannes et fast stof ved forsuring af det ioniske salt, kan det opsamles gennem sugefiltrering. Denne metode bør kun anvendes, hvis der ses store mængder af store krystaller. Hvis der dannes fine krystaller (hvilket er ret almindeligt), vil de tilstoppe filterpapiret og forhindre tilstrækkelig dræning. Hvis der kun ses en lille mængde fast stof sammenlignet med den teoretiske mængde, er det sandsynligt, at forbindelsen er ret vandopløselig, og filtrering vil føre til lav genvinding.
- Hvis der ikke dannes noget fast stof ved syrning (eller hvis der dannes fine krystaller eller en lille mængde fast stof), skal den sure komponent ekstraheres tilbage i et organisk opløsningsmiddel (×3). Som en generel tommelfingerregel skal du bruge en tredjedel så meget opløsningsmiddel til ekstraktionerne som det oprindelige lag (f.eks. hvis du bruger 100 ml vandig opløsning, skal du ekstrahere med 33 ml organisk opløsningsmiddel hver gang). Sørg for først at afkøle den vandige opløsning i et isbad før ekstraktion, hvis forsuringen skabte mærkbar varme. Følg op med en saltvandsvask (×1), hvis du bruger diethylether eller ethylacetat, tør med et tørremiddel, og fjern opløsningsmidlet via en rotationsfordamper for at efterlade den rene syrekomponent.
2. Isolering af den basiske komponent:
Brug en lignende proces som ved isolering af den sure komponent, bortset fra at opløsningen basificeres med 2M NaOH(aq), indtil den giver en pH på 9-10 som bestemt ved hjælp af pH-papir.
3. Isolering af den neutrale komponent:
Den neutrale komponent vil være den "resterende" forbindelse i det organiske lag. For at isolere skal du vaske med saltvand (×1), hvis du bruger diethylether eller ethylacetat, tørre med et tørremiddel og fjerne opløsningsmidlet via rotationsfordamperen for at efterlade den rene neutrale komponent.
Brug en lignende proces som ved isolering af den sure komponent, bortset fra at opløsningen basificeres med 2M NaOH(aq), indtil den giver en pH på 9-10 som bestemt ved hjælp af pH-papir.
3. Isolering af den neutrale komponent:
Den neutrale komponent vil være den "resterende" forbindelse i det organiske lag. For at isolere skal du vaske med saltvand (×1), hvis du bruger diethylether eller ethylacetat, tørre med et tørremiddel og fjerne opløsningsmidlet via rotationsfordamperen for at efterlade den rene neutrale komponent.
Konklusion.
Ekstraktionsmetoder bruges til at udtrække nogle stoffer fra en blanding. Disse stoffer kan være basiske, sure eller neutrale (polære eller upolære). For eksempel bruges denne metode under amfetaminproduktion i dekanteringstrinnet: Saml det øverste lag, der indeholder amfetaminbase, i alkohol. Det kan tørres lidt med vandfrit magnesiumsulfat, og slaggen kan desuden ekstraheres med et ikke-polært opløsningsmiddel (ether, benzen, toluen), hvorefter opløsningsmidlet inddampes. Mephedron-produktion omfatter manipulation med separationstragt og ekstraktion. Syre-base-ekstraktion bruges også til rensning af nogle psykoaktive stoffer for urenheder.
Attachments
Last edited: