Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 290
- Reaction score
- 329
- Points
- 63
Psilocybin (3-[2-(Dimethylamino)ethyl]-1H-indol-4-yl-dihydrogenphosphat) ist ein Alkaloid aus der Familie der Tryptamine, ein phosphoryliertes Psilocin-Derivat, das psychedelische Eigenschaften besitzt. Von allen biologischen Psilocybin-Quellen enthalten die Pilzarten der Gattungen Psilocybe, Panaeolus, Stropharia, Gymnopilus und Inocybe die größte Menge, aber auch etwa 200 andere Pilzarten enthalten Psilocybin. Eine psilocybinhaltige Pilzfamilie, die unter dem Namen "Magic Mushrooms" bekannt ist, wurde im Laufe der Geschichte wegen ihrer halluzinogenen Wirkung verwendet. Ende der 1950er Jahre isolierte und synthetisierte Albert Hoffman von der Firma Sandoz Laboratories die psychoaktiven Verbindungen Psilocybin und Psilocin aus psilocybinhaltigen Pilzen. Psilocybin wurde von Sandoz als Indocybin für grundlegende psychopharmakologische und therapeutische klinische Versuche verkauft. Derzeit sind Arten von Psilocybe in Asien, Australien, den Vereinigten Staaten, Kanada, Mexiko, Mittel- und Südamerika, Afrika und Europa bekannt. Es gibt zahlreiche Hinweise darauf, dass die Psilocybin-haltigen Arten ursprünglich aus Afrika und Europa stammen und dass Psilocybe bereits vor dem Auftauchen des modernen Menschen in der Alten Welt verbreitet war. Psilocybin-haltige Pilze können in der freien Natur gefunden oder in kontrollierter Umgebung aus Sporenabdrücken gezüchtet werden. Die Popularität von Psilocybin nahm in den 1960er Jahren rasch zu. Im Jahr 1970 wurde es in die Liste I aufgenommen, was zu einer erheblichen Einschränkung der Forschung über Psilocybin führte. Jüngste Vorstudien zu Psilocybin haben jedoch gezeigt, dass es bei der Behandlung von Zwangsstörungen, Alkoholabhängigkeit, schweren depressiven Störungen und Depressionen bei Patienten mit Krebs im Endstadium eingesetzt werden kann. Psilocybin ist in den Vereinigten Staaten nach dem Controlled Substances Act von 1971 als Schedule-I-Substanz eingestuft; daher dürfen jährlich nur begrenzte Mengen hergestellt werden. Trotz des Schedule-I-Status ist Psilocybin seit den 1960er Jahren eine beliebte Freizeitdroge, und obwohl der Konsum nachgelassen hat, seit es eine kontrollierte Substanz ist, wird es weiterhin zu Freizeitzwecken verwendet. Die meisten anderen Industrieländer haben Psilocybin und psilocybinhaltige Pilze ebenfalls als illegal eingestuft. Die große Ausnahme von dieser Regel sind die Niederlande, wo es eine Gesetzeslücke gibt, die den Anbau, den Verkauf und den Verzehr von psilocybinhaltigen psychoaktiven Trüffeln" erlaubt. Frühe Belege für den Konsum durch mittel- und südamerikanische Schamanen wurden an zahlreichen Orten gefunden. Moderne Studien begannen in den späten 1950er Jahren mit dem Ethnomykologen R. Gordon Wasson und wurden in den 1960er und frühen 1970er Jahren von den berühmten Psychedelik-Forschern Timothy Leary, Ralph Metzner und Ram Dass an der Harvard University, Albert Hofmann von Sandoz Labs, Terrence McKenna und Jonathan Ott fortgesetzt. In den 1950er Jahren erwachte das Interesse von Psychiatern und Psychologen, da man das Potenzial von Psychedelika als Mittel zur Verkürzung der Psychotherapie erkannte. Bereits in den 1950er Jahren begann die Forschung mit der psychedelischen Behandlung von Suchtkrankheiten. Oft wurden aufschlussreiche Wirkungen beobachtet, die zur Nüchternheit beitrugen, was Humphry Osmond dazu veranlasste, den Begriff "psychedelisch" zu prägen, um die "bewusstseinsverändernden" Fähigkeiten dieser Drogenklasse zu beschreiben. Die meisten klinischen Forschungen wurden in den 1960er Jahren durchgeführt, wobei häufig die synthetische Version Indocybin verwendet wurde.
Synthese von Pcilocybin
Synthesevon Pcilocin
Psilocybin wurde in über 100 Pilzarten gefunden, von denen viele zur Gattung Psilocybe gehören. Das Alkaloid Psilocybin in der Familie Inocybeacede taucht zwischen 10 und 20 mya auf, und es ist wahrscheinlich, dass das Auftreten von Psilocybin in der Familie Psilocybe ebenfalls um diese Zeit erfolgte. Derzeit sind Psilocybe-Arten in Asien, Australien, den Vereinigten Staaten, Kanada, Mexiko, Mittel- und Südamerika, Afrika und Europa bekannt. Vieles deutet darauf hin, dass die psilocybinhaltigen Arten in Afrika und Europa entstanden sind, und es gibt auch Hinweise darauf, dass Psiloche in der Alten Welt bereits vor dem Auftauchen des modernen Menschen vorhanden war. Psilocybinhaltige Pilze können in freier Wildbahn gefunden oder in einer kontrollierten Umgebung anhand von Sporenabdrücken gezüchtet werden, die entstehen, wenn man den Hut eines bekannten Pilzes auf ein Blatt Wachspapier legt und die Sporen auf das Papier fallen lässt, wodurch ein einzigartiger Pilz-Fingerabdruck entsteht. Obwohl die letztere Methode wesentlich verbreiteter und sicherer ist, suchen manche Konsumenten immer noch nach "Magic Mushrooms" in der freien Natur. Die Gefahr einer falschen Identifizierung ist allgegenwärtig und ein Fehler, der selbst den erfahrensten Mykologen unterlaufen kann. Eine falsche Identifizierung kann zu einem Fehler führen, für den selbst die erfahrensten Mykologen anfällig sind. Eine Verwechslung kann zu allem Möglichen führen, von leichten Unannehmlichkeiten bis hin zum Tod. Der plötzliche Tod tritt am häufigsten bei Hobby-Mykologen ein, die auf der Suche nach psilocybinhaltigen Pilzen und einer anderen Art psychoaktiver Pilze sind, die gemeinhin als "Fliegenpilz" (Amanita muscaria) bekannt sind, dem ikonischen rot-weiß gepunkteten Pilzkopf, der oft in Märchen vorkommt (statt Psilocybin enthält A. muscaria die psychoaktiven Drogen Muscimol und Ibotensäure). Leider sind mehrere Amanita-Arten tödlich, darunter der treffend benannte "Todeshut" (Amanita phalloides) und der "Zerstörungsengel" (Amanita virosa), der dem Amanita muscaria und verwandten Arten sehr ähnlich sein kann. Das Erbe und die Verwendung von "Magic Mushrooms" ziehen sich durch die gesamte Frühgeschichte und setzen sich bis in die Neuzeit fort. Frühe Belege für die Verwendung durch mittel- und südamerikanische Schamanen sind an zahlreichen Orten gefunden worden. Moderne Studien begannen in den späten 1950er Jahren mit dem Ethnomykologen R. Gordon Wasson und wurden in den 1960er und frühen 1970er Jahren von den berühmten Psychedelik-Forschern Timothy Leary, Ralph Metzner und Ram Dass an der Harvard University, Albert Hofmann von Sandoz Labs, Terrence McKenna und Jonathan Ott fortgesetzt. In den 1950er Jahren wurde das Interesse von Psychiatern und Psychologen geweckt, da man davon ausging, dass sie zur Verkürzung der Psychotherapie beitragen könnten. Bereits in den 1950er Jahren begann die Forschung mit der psychedelischen Behandlung von Suchtkrankheiten. Häufig wurden aufschlussreiche Wirkungen beobachtet, die zur Nüchternheit beitrugen, was Humphry Osmond dazu veranlasste, den Begriff "psychedelisch" zu prägen, um die "bewusstseinsverändernden" Fähigkeiten dieser Drogenklasse zu beschreiben.
Die Struktur von Psilocybin und anderen Indolalkylamin-Halluzinogenen ähnelt dem körpereigenen Neurotransmitter Serotonin, dem Hormon Melatonin und dem mutmaßlich körpereigenen Psychedelikum N,N-Dimethyltryptamin. Sie alle leiten sich von der gleichen Verbindung ab - dem Tryptamin. Psilocybin (O-Phosphoryl-4-hydroxy-N, N-dimethyltryptamin) und sein aktiver dephosphorylierter Metabolit Psilocin (N, N-dimetyltryptamin) gehören strukturell zur Gruppe der Tryptamin/Indolamin-Halluzinogene und sind strukturell mit Serotonin verwandt. Eine äquimolare Dosis zu 1 Mol Psilocin ist 1,4 Mol Psilocybin. Die Substitution des Indolkerns in Position 4 spielt wahrscheinlich eine wesentliche Rolle bei der halluzinogenen Wirkung. Psilocybin und Psilocin sind in ihrer reinen Form weiße, kristalline Pulver. Während Psilocybin in Wasser löslich ist, ist Psilocin eher fettlöslich. Psilocin kann jedoch auch in einer angesäuerten wässrigen Lösung und in Dimethylsulfoxid (DMSO; bis zu 100 mM) verdünnt werden. Darüber hinaus sind beide Substanzen in Methanol und Ethanol löslich, aber nahezu unlöslich in Petrolether und Chloroform. Beide Drogen sind lichtinstabil (insbesondere in Form von Lösungen), ihre Stabilität bei niedrigen Temperaturen im Dunkeln unter inerter Atmosphäre ist sehr gut. Psilocybin ist eine thermolabile Verbindung, löslich in Wasser, Methanol, Ethanol, aber unlöslich in organischen Lösungsmitteln. Es hat eine äußerst geringe Eigenaktivität; es wirkt hauptsächlich als Prodrug von Psilocin. Der pKa-Wert reicht von 1,3 bis 6,5. Bei Einwirkung von ultraviolettem Licht wird seine Stabilität in Lösung gestört, was zu einer Oxidation führt. Löslich in 120 Teilen siedendem Methanol; schwer löslich in Ethanol; praktisch unlöslich in Chloroform, Benzol, Dampfdruck - 1,9X10-12 mm Hg bei 25 °C. Das Molekulargewicht beträgt 285,25; es hat einen Ammoniakgeschmack, einen Schmelzpunkt von 224 Grad Celsius, einen pH-Wert von 5,2 in 50%igem Wasser-Ethanol, eine TDLo von 75 mkg/kg bei intramuskulärer Verabreichung beim Menschen, eine TDLo von 60 mkg/kg bei oraler Verabreichung beim Menschen, eine LD50 von 280 mg/kg bei intravenöser Verabreichung bei Ratten. Es wird davon ausgegangen, dass Psilocybin die Blut-Hirn-Schranke im Vergleich zum Psilocin nur schlecht durchdringt. Dies ist auf die unterschiedlichen Wasserstoffbrückenbindungen zurückzuführen, durch die Psilocybin lypophiler ist, was die Passage durch die Blut-Hirn-Schranke erleichtert. Bei der visuellen Untersuchung sind gereinigtes Psilocybin und Psilocin unterscheidbar. Das eine hat das Aussehen eines weißen oder fast weißen Nadelkristalls, das andere bildet eine ölige dunkelbraune bis schwarze Farbe.
Rechtlicher Status.
Die Regierung hat 1968 ein Verbot des Besitzes von Psilocybin und Psilocin verhängt. Im Jahr 1970 wurden Psilocybin und Psilocin in die Liste der Drogen der Kategorie I aufgenommen. In den USA haben Denver, Oakland, Chicago, Ann Arbor und Santa Cruz den Besitz von Zauberpilzen entkriminalisiert, der Verkauf von Pilzen ist jedoch weiterhin verboten. Im Jahr 2020 hat Oregon Psilocybin legalisiert, und der District of Columbia hat den Konsum von Magic Mushrooms entkriminalisiert. Der Verkauf und Transport von Psilocybin aus Österreich ist illegal. Der Besitz wurde entkriminalisiert, und der Anbau ist legal, solange die Pilze nicht für den Konsum bestimmt sind. Wer mit dem Besitz von Pilzen für den Eigengebrauch erwischt wird, kann zu einer kostenlosen Therapie verpflichtet werden. In Portugal sind Psilocybin-Pilze zwar illegal, aber entkriminalisiert. Personen, die mit für den Eigengebrauch bestimmten Mengen erwischt werden, können zu einer Rehabilitations- oder Therapiemaßnahme verpflichtet werden. In den Niederlanden sind Psilocybin-Pilze in Form von Trüffeln legal. Im Einklang mit der UN-Politik ist Psilocybin in Italien illegal; Psilocybe-Pilze sind jedoch entkriminalisiert. Der Verkauf und die Beschaffung von Anbausätzen und Sporen sind legal, aber Verwaltungsstrafen wie der Verlust des Führerscheins können die Folge sein, wenn man mit Pilzen erwischt wird. Spanien hat den persönlichen Besitz und den Konsum von Psilocybin-Pilzen entkriminalisiert, während Psilocybin selbst weiterhin illegal ist. Anbau und Verkauf sind illegal, und die Legalität von Sporen und Grow-Kits ist unklar. Auf den Britischen Jungferninseln sind Besitz und Anbau von Psilocybin-Pilzen erlaubt. Allerdings ist es illegal (aber nicht strafbewehrt), sie zu verkaufen oder zu transportieren. In Jamaika sind Besitz, Verkauf, Transport und Anbau von Psilocybin-Pilzen legal. Jamaika verkauft Psilocybin-Pilze ganz offen. In Brasilien ist der Besitz, der Verkauf, der Transport und der Anbau von Zauberpilzen legal. Psilocybin und Psilocin sind als illegal eingestuft, die Pilze selbst werden jedoch nicht als illegal angesehen. Der Besitz von Magic Mushrooms ist in Mexiko illegal, obwohl es keine Strafverfolgung gibt, wenn die Magic Mushrooms in indigenen Kulturen vorkommen. Der Anbau von Pilzen ist illegal, es sei denn, die Pilze werden in der freien Natur gezüchtet. Verkauf und Transport sind illegal. Zauberpilze sind in Samoa legal. Ab 2018 sind sie in Vietnam illegal.
Forscher der Johns Hopkins University fordern, dass Psilocybin-Pilze aus der Liste I in die Liste IV herabgestuft werden sollten, da sie derzeit als Stoff der Liste I eingestuft sind. 2019 stimmte die Stadt Oakland (Kalifornien) für die Entkriminalisierung von Magic Mushrooms, nur einen Monat nachdem Denver (Kalifornien) dies beschlossen hatte. In Kalifornien gibt es einen Vorstoß zur Entkriminalisierung von Psilocybin-Pilzen auf landesweiter Ebene, wobei viele psychedelische Bewusstseins- und Interessengruppen diese Änderung unterstützen. Außerdem erwägt die Legislative des Bundesstaates Oregon die Verabschiedung eines Gesetzes zur Entkriminalisierung von Psilocybin-Pilzen und zur Erteilung von Lizenzen für den Anbau. Ein Großteil dieser vielversprechenden Forschung wird von der Multidisciplinary Association of Psychedelic Studies (MAPS) betrieben, die derzeit medizinische Forschung mit MDMA, Psilocybin, LSD, Marihuana, Ibogain und Ayahuasca betreibt. Eine weitere Organisation, das Heffter Research Institute, ist auf die Psilocybin-Forschung spezialisiert. Zum Vorstand des Heffter Research Institute gehört der Mitbegründer Dr. David Nichols, ein weithin bekannter Forscher, Professor und Experte für die Chemie von Halluzinogenen. Zu den weiteren Forschern gehören Dr. Dennis McKenna, ein angesehener Schriftsteller, Ethnopharmakologe, Psychonaut und Bruder des verstorbenen Terrence McKenna, sowie Dr. Roland Griffiths, der an der Johns Hopkins University phänomenale Forschungen über Psilocybin und Sucht betreibt. Auch international werden derzeit mehrere Psilocybin-Studien durchgeführt. Die Beckley Foundation mit Sitz im Vereinigten Königreich fördert einige der fortschrittlichsten Psilocybin-Forschungen, die es derzeit gibt. Die 1996 von Amanda Fielding - einer angesehenen Psychonautin und Wissenschaftlerin - gegründete Beckley Foundation fördert derzeit zusammen mit MAPS und Heffter die neurowissenschaftliche Forschung zu Psilocybin. Diese Forschung findet am Imperial College London mit Dr. David Nutt und Dr. Robin Carhart-Harris statt, die beide in der Vergangenheit Psilocybin-Forschungsarbeiten veröffentlicht haben, insbesondere das "Entropic Brain Model". Heffter sponsert auch eine Studie in der Schweiz mit dem Titel "Psilocybin-Effekte auf Aufmerksamkeit, Wahrnehmung und Kognition". In ähnlicher Weise sponsert MAPS in Deutschland eine Studie mit dem Titel "Experimentelle Studien über die Auswirkungen von Psilocybin auf die binokulare Tiefeninversion, binokulare Rivalität".
Pharmakokinetik und Pharmakodynamik.
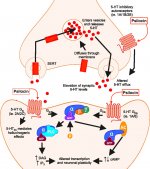
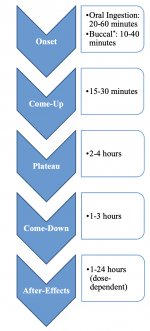
Nach der Einnahme wird Psilocybin in der Leber biotransformiert, wo es durch ein unbekanntes Enzym zu Psilocin dephosphoryliert wird. Nachdem Psilocin in den systemischen Blutkreislauf gelangt ist, gelangt es in das Gehirn, wo es psychoaktiv wirkt. Anderen Daten zufolge wird Psilocybin nach oraler Verabreichung im sauren Milieu des Magens oder unter Einwirkung der alkalischen Phosphatase (und anderer unspezifischer Esterasen) im Darm, in den Nieren und möglicherweise im Blut rasch dephosphoryliert, wobei eine phenolische Verbindung Psilocin entsteht, die die Blut-Hirn-Schranke leicht passieren kann. Es ist bemerkenswert, dass die relative Potenz von Psilocin und Psilocybin fast identisch ist mit dem Verhältnis des Molekulargewichts dieser Verbindungen. Die Blockierung der alkalischen Phosphotase durch konkurrierende β-Glycerophosphat-Substrate nivelliert die Intoxikationssymptome. Psilocin durchläuft beide Phasen des Metabolismus. Die erste Phase des Metabolismus umfasst die oxidative Desaminierung von Psilocin zu 4-Hydroxyindol-3-Acetaldehyd, katalysiert durch Monoaminoxidase oder Aldehyddehydrogenase in der Leber, mit anschließender Oxidation zu 4-Hydroxyindol-3-Essigsäure, 4-Hydroxyindol-3-Acetaldehyd und 4-Hydroxytryptophole. Die an diesem Prozess beteiligten Enzyme sind noch nicht identifiziert worden. Deshalb können MAO-Hemmer die halluzinogenen Wirkungen von Psilocybin verstärken, so wie Ethanol den Trip verstärken kann, weil sein primärer Metabolit Acetaldehyd in vivo mit endogenen Aminen reagiert, wodurch die MAO-Hemmer Tetrahydroisochinoline und β-Carboline gebildet werden. Da Psilocybin eine kompetitive Hemmung der MAO (die Serotonin verstoffwechselt) bewirkt, steigt der Serotoninspiegel im Gehirn und gleichzeitig sinkt die 5-HIAA-Konzentration. Außerdem gibt es einen für die klinischen Auswirkungen unbedeutenden Stoffwechselweg, der eine Oxidation beinhaltet, die zur Bildung eines dunkelblauen Produkts führt, das die Struktur von o-Chinon oder Iminochinon hat. Dieser Stoffwechselweg wird durch Hydroxyindol-Oxidasen katalysiert (Ceruloplasmin, die kupferhaltige Oxidase des Säugetierplasmas, und Cytochromoxidase). Die oben genannten Metaboliten zeigen nur eine unbedeutende physiologische Aktivität. Bei parenteraler Verabreichung von Psilocybin spielen die Gewebephosphatasen die gleiche Rolle, wobei die Nierenphosphatasen zu den aktivsten gehören. Wenn man bedenkt, dass die kompetitive Blockade der Dephosphorylierung die psychotrope Wirkung von Psilocybin blockiert, ist klar, dass Psilocin der wichtigste aktive Metabolit von Psilocybin ist. Innerhalb von 5 Stunden nach der oralen Verabreichung von Psilocybin sind bis zu 80 % des Psilocins als konjugiertes O-Glucuronid im Blut vorhanden und werden unverändert mit dem Urin ausgeschieden. Die Glucuronidierung der Hydroxylgruppe zu Psilocin-O-Glucuronid ist eine wichtige Stufe der Entgiftung, weshalb die enzymatische Hydrolyse die Nachweiszeit in Urinproben verlängert. Während Psilocin im Dünndarm einer umfassenden Glucoronidierung durch UDP-Glucuronosyltransferasen (UGT)1A10 unterzogen wird, leistet UGT1A9 den Hauptbeitrag zur Glucoronidierung nach seiner Aufnahme ins Blut. Die N-Glucuronidierung findet in diesem Fall nicht während des gesamten Stoffwechsels statt. Neben dem oben genannten Stoffwechselweg unterliegt Psilocin selbst auch einem oxidativen Stoffwechsel. Die Demethylierung und Desaminierung von 4-Hydroxyindol-3-yl-acetaldehyd (4-HIA) mit anschließender Oxidation (vermutlich durch hepatische Aldehyddehydrogenase und Monoaminoxidase) führt zur Bildung von 4-Hydroxyindol-3-essigsäure (4-HIAA) und 4-Hydroxytryptofol (4-HT). Diese unbedeutenden Metaboliten (etwa 4 % werden auf die oben beschriebene Weise abgebaut) können im menschlichen Blutplasma nachgewiesen werden. Der dritte Weg des Metabolismus von Psilocin beinhaltet, wie bereits erwähnt, die Oxidation durch Hydroxyindoloxidasen. Psilocin verteilt sich in allen Geweben, auch im Gehirn, und wird innerhalb von 24 Stunden ausgeschieden. Der größte Teil wird innerhalb der ersten 8 Stunden ausgeschieden (etwa 65 % mit dem Urin und 15-20 % mit der Galle und den Fäkalien). Im Urin kann es 2 Wochen lang nachgewiesen werden. Die höchsten Psilocin-Konzentrationen finden sich im Neokortex, im Hippocampus, im extrapyramidalen motorischen System und in der Retikularformation. Beim Menschen können Psilocybin und Psilocin nach 20-40 Minuten nach oraler Verabreichung im Blutplasma nachgewiesen werden. Maximale Konzentrationen werden in 80-100 Minuten erreicht und können innerhalb von sechs Stunden nachgewiesen werden. Die Halbwertszeit von Psilocin im Blutplasma beträgt etwa 2/5 Stunden nach der oralen Verabreichung und 1,23 Stunden nach der parenteralen Verabreichung. Wie bereits erwähnt, liegen etwa 80 % des Psilocins im Plasma in konjugierter Form vor. Psilocin (90-97%) und Psilocybin (3-10%) können im Urin unverändert oder konjugiert mit Glucoronsäure nachgewiesen werden. Die Eliminationshalbwertszeit beträgt etwa 50 Minuten, die Eliminationskonstante liegt bei 0,307/h. Der größte Teil der Substanz wird innerhalb der ersten drei Stunden nach oraler Verabreichung ausgeschieden und innerhalb von 24 Stunden vollständig mit dem Urin ausgeschieden. Der vollständige Stoffwechselweg von Psilocybin ist noch wenig erforscht, und es müssen noch viele Informationen gesammelt werden, um die genauen Mechanismen des Stoffwechsels zu bestimmen.
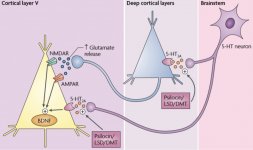
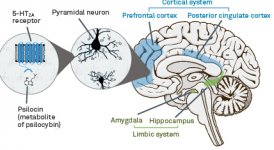
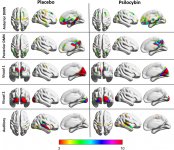
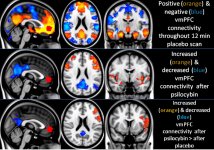
Die Pharmakologie von Psilocybin ist sehr komplex und nur unzureichend untersucht worden. Psilocybin kann vermutlich eine eigene, unbedeutende Wirkung haben, wirkt jedoch hauptsächlich als Prodrug von Psilocin. Letzteres passiert leicht die Blut-Hirn-Schranke und entfaltet dort seine psychoaktive Wirkung. Die wichtigsten Bindungsstellen sind in der obigen Tabelle zusammengefasst. Psilocin bindet am stärksten an Serotoninrezeptoren: 5-HT1D,2B,2C,5,6,7), es hat auch ein mäßiges Bindungspotenzial an Serotoninrezeptoren (5-HT1A, 1B, 2A). Neben den Serotoninrezeptoren hat Psilocin eine gewisse Affinität zu Histaminrezeptoren des ersten Typs (H1), Alpha-2A- und -2B-Rezeptoren sowie zu Dopaminrezeptoren des dritten Typs (D3). In Neuronen, die den 5HT2A-Rezeptor exprimieren, aber nicht in 5HT2A-Knockouts, erhöht Psilocybin die Expression von frühen Genen (erg-1, erg-2, c-fos, jun-B, period-1, gpcr-26, fra-1, N- 10, I-κBα) und reduziert die Expression von sty-kinase. Natürlich ist der genaue Signalweg, der vom Rezeptor zur Aktivierung der frühen Gene führt, noch nicht bekannt. In Anbetracht der Tatsache, dass ein nicht halluzinogenes Lisurid auch c-fos aktiviert, ist es wahrscheinlich, dass die Expression von c-fos nur eine erhöhte neuronale Aktivität widerspiegelt, während die Expression von egr-1/ egr-2 spezifisch für die halluzinogene Wirkung ist. Gonzales-Meaeso erklärte diese Selektivität mit der "Agonist trafficking of receptor signaling theory", wonach Halluzinogene den 5HT2A/mGlu2-Rezeptor-Heterokomplex und andere G-Proteine aktivieren als nicht halluzinogene 5-HT2A-Agonisten. Diese Hypothese wird durch eine Studie gestützt, in der Mäuse mit einem Knockout-Gen für den mGlu2-Rezeptor kein Kopfzuckungsverhalten zeigen. Psilocilin hemmt nachweislich den Natrium-abhängigen Serotonin-Transporter (SERT), was zu einem Anstieg der Serotonin-Konzentration führt. Das Serotonin verbleibt nach seiner Freisetzung im synaptischen Spalt, was letztlich zu einer wiederholten Aktivierung der serotonergen postganglionären Neuronen führt. Was die Bewertung der Bindungsaffinität zu den Rezeptoren betrifft, so sind sie wie folgt geordnet: 5HT2B > 5HT1D > D1 > 5HT1E > 5HT1A > 5HT5A > 5HT7 > 5HT6 > D3 > 5HT2C > 5HT1B > 5HT2A. Die Bindung an Imidazolinrezeptoren des ersten Typs wurde ebenfalls nachgewiesen. Interessant ist, dass die Affinität von Psilocybin zu den menschlichen 5-НТ2А-Rezeptoren 15-mal höher ist als die von Ratten. Der Agonismus von 5НТ2А-Rezeptoren und die Aktivierung einer übermäßigen Anzahl dieser Rezeptoren und Rezeptorsubtypen sind für die einzigartigen und intensiven psychedelischen Wirkungen von Psilocybin verantwortlich. In der Vergangenheit wurde viel darüber diskutiert, ob 5-НТ2А- oder 5-НТ2С-Rezeptoren für isolierte Halluzinationen nach dem Verzehr von psilocybinhaltigen Pilzen verantwortlich sind. Die Studien haben gezeigt, dass 5-НТ2А-Antagonisten die Halluzinationen unterdrücken, während Antagonisten von 5-НТ2С weder die Potenzierung der Halluzinationen noch die nivellierende Wirkung auf sie haben. So ist der Agonismus der 5-НТ2А-Rezeptoren mit einer allgemeinen Erregung der Neuronen, einer Verbesserung des Gedächtnisses und der Lernfähigkeit, einer Kontraktion der glatten Muskulatur der Gefäße, des Magen-Darm-Trakts und der Bronchien, einer gewissen entzündungshemmenden Wirkung, einer erhöhten Produktion von Prolaktin und Oxytocin, des adrenocorticotropen Hormons und von Renin bei Aktivierung des Renin-Angiotensin-Aldosteron-Systems verbunden. Bei der 5-НТ2С-Aktivierung durch Psilocin kommt es zur Aktivierung von Proopiomelanocortin (dem Vorläufer des α-, β- und γ-melanozytenstimulierenden Hormons und des adrenocorticotropen Hormons) und zur Freisetzung von Cortisol. Diese Hormone sorgen für gesteigerten Appetit, Insulinempfindlichkeit, Glukosestoffwechsel, Stabilisierung auf anxiogene und stressige Reize. Psilocin wirkt als partieller Agonist von 5-НТ1А-Rezeptoren, die hauptsächlich im Nucleus raphe (DRN) und im Nucleus medianus raphe (MRN), die sich in der Nähe der Mittellinie des Hirnstamms entlang seiner gesamten rostro-caudalen Ausdehnung befinden, als somatodendritische Autorezeptoren exprimiert werden. Der MRN fördert die Aktivierung von Gedächtniskonsolidierungsprozessen und wird in den Hippocampus projiziert, während der VRN einer der größten serotonergen Kerne im menschlichen Gehirn ist, der einen bedeutenden Anteil an der serotonergen Innervation des Vorderhirns hat; außerdem hat der MRN Projektionsfasern in die Amygdala und den Hypothalamus, was mit der Regulierung des zirkadianen Rhythmus und verschiedener Arten von Zellen, die Katecholamine und Substanz-P produzieren, in Verbindung gebracht wird. DRN und MRN sind reich an präsynaptischen 5-НТ1А-Rezeptoren, und Psilocin wirkt insbesondere an den präsynaptischen Stellen um ein Vielfaches (5-6 Mal) stärker als an den postsynaptischen. Diese Vorliebe erklärt sich durch eine hohe Dichte von 5-НТ1А-Rezeptoren, die sich in diesen Bereichen befinden. Diese bestimmte Art von Rezeptoren, die sich auf den Körpern der serotonergen Zellen der Raphe-Zone befinden, findet sich beispielsweise nicht auf postsynaptischen Membranen. In fMRT-Studien wurde festgestellt, dass Psilocybin den Blutfluss und die venöse Sauerstoffversorgung des Gehirns deutlich verringert. Diese Tatsache korreliert mit seiner subjektiven Wirkung und verringert die positive Verbindung zwischen zwei wichtigen Strukturknoten (mPFC и PCC) erheblich. Psilocybin erhöht nachweislich den Glukosestoffwechsel im Gehirn. Außerdem wurde in einigen Experimenten nachgewiesen, dass das DMN auch für die Aufrechterhaltung der kognitiven Integration und Einschränkungen unter normalen Bedingungen von entscheidender Bedeutung ist. Nach Bindung von Psilocin an präsynaptische 5-НТ1А-Rezeptoren des DRN-Bereichs unterdrückt es die Wirkungen dieses Bereichs, während die darunter liegenden Zellen intakt bleiben und die mit dem Locus coeruleus verbundene sympathische Aktivität verstärken. Andere Lokalisierungen von 5-НТ2А-Rezeptoren zeigen einen raschen Rückgang der Aktivität dieser Rezeptoren und eine Abnahme ihrer Dichte bei Aktivierung durch Psilocin. Psilocybin hat also keine Toleranz gegenüber der hemmenden Wirkung von DRN. Es ist wichtig anzumerken, dass selektive Agonisten von 5-НТ1а-Rezeptoren in ihrem Kern nicht halluzinogen sind, sie spielen jedoch eine Rolle bei der Beeinflussung der hemmenden Wirkung, die im DRN festgestellt wird.
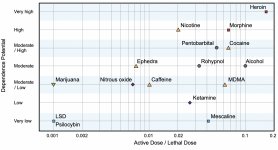
Obwohl der Dopaminrezeptor des zweiten Typs eine wichtige Rolle bei der Entstehung von Halluzinationen bei verschiedenen psychischen Erkrankungen spielt, wird angenommen, dass er keine aktive und indirekte Beziehung zur Psilocin-Wirkung hat. Diese Hypothese wurde erstmals von Vollenweider et al. bewiesen, als sie feststellten, dass die Verabreichung von Galoperidol (Agonist des D2R) die psychoaktiven Wirkungen von Psilocin nicht abschwächt. Obwohl die dopaminergen Wirkungen von Psilocin als minimal angesehen werden, hat es im Vergleich zu anderen Dopaminrezeptor-Subtypen eine relativ hohe Bindungsfähigkeit an den D3-Rezeptor. Obwohl die über den D3R vermittelten Wirkungen nur wenig erforscht sind, tragen sie vermutlich zu den charakteristischen psychoaktiven Eigenschaften von Psilocybin und seiner Fähigkeit zur Suchtentstehung bei. Bei der chemischen Vorstufe von Psilocin, dem 4-Acetoxy-N,N-dimethyltryptamin, ist die Phosphoryloxygruppe durch eine Acetoxygruppe ersetzt. Es wird auf die gleiche Weise verstoffwechselt wie die Phosphoryloxygruppe, und diese Veränderung ermöglicht es, einige Stoffwechselprozesse der ersten Phase zu umgehen. Obwohl Psilacetin pharmakologisch identisch mit Psilocybin ist, berichten viele Anwender, dass es einige unbedeutende, aber erkennbare Unterschiede zwischen ihnen gibt. Psilacetin wird oft als eine Substanz mit schnellerem Wirkungseintritt beschrieben, die keine Angstzustände und Übelkeit hervorruft (die beim Konsum von Psilocybin aufgrund des fehlenden Chitins, das normalerweise in den Pilzen enthalten ist, auftreten) und eine kürzere Wirkungsdauer aufweist. Es ist bekannt, dass die mittlere tödliche Dosis bei Ratten etwa 293 mg/kg beträgt, was auf ein großes therapeutisches Fenster von Psilocin hinweist. Tachyphylaxie, eine schnelle Desensibilisierung gegenüber einer Substanz, die zu einer Abnahme der physiologischen Wirkung führt, ist ein Phänomen, das mit dem Konsum vieler Halluzinogene verbunden ist. Die Toleranz gegenüber Psilocybin entwickelt sich bereits nach dem ersten einmaligen Gebrauch. Der Mechanismus beinhaltet eine physiologische Reaktion auf die übermäßige Stimulation der 5-НТ2А-Rezeptoren durch eine rasche Verringerung der Rezeptorstellen und eine Abnahme der Rezeptordichte auf der Zelle. Im Allgemeinen geht man davon aus, dass diese Rezeptorstellen innerhalb von 3-7 Tagen nach der ersten Einnahme auf die Hälfte des ursprünglichen Niveaus zurückgehen. Je nach Dosis und Dauer der wiederholten Einnahme erreichen sie innerhalb von 4 Wochen wieder ihre ursprüngliche Menge. Außerdem gibt es eine Kreuztoleranz zwischen den Indolalkylamin- und Phenylalkylamin-Klassen der Halluzinogene.
Attachments
-
 aDjgnEic18.jpg572.2 KB · Views: 1,641
aDjgnEic18.jpg572.2 KB · Views: 1,641 -
 sRHGpjI9LU.jpg788.9 KB · Views: 1,613
sRHGpjI9LU.jpg788.9 KB · Views: 1,613 -
 TQv018fRJh.jpg128.6 KB · Views: 959
TQv018fRJh.jpg128.6 KB · Views: 959 -
lF1rOfpW8k.jpg2.6 MB · Views: 993
-
 TSkYz5Gq6P.jpg363.8 KB · Views: 1,773
TSkYz5Gq6P.jpg363.8 KB · Views: 1,773 -
 sPlo2QDBMe.jpg551.6 KB · Views: 1,744
sPlo2QDBMe.jpg551.6 KB · Views: 1,744 -
 AxRV2Hfutv.jpg697.8 KB · Views: 1,766
AxRV2Hfutv.jpg697.8 KB · Views: 1,766 -
 b2Ma0wsVTD.jpg607.2 KB · Views: 1,838
b2Ma0wsVTD.jpg607.2 KB · Views: 1,838 -
 QtXjIHo7PJ.jpg438.5 KB · Views: 1,635
QtXjIHo7PJ.jpg438.5 KB · Views: 1,635 -
 rI0YMKgE6z.jpg1.1 MB · Views: 1,777
rI0YMKgE6z.jpg1.1 MB · Views: 1,777 -
 Q1ueUSGlFN.jpg614.4 KB · Views: 1,787
Q1ueUSGlFN.jpg614.4 KB · Views: 1,787
Last edited by a moderator:
