Mefedroni (4-metyylimetkatinoni) on β-ketoamfetamiinin stimuloiva väärinkäytön huume, jolla on läheisiä rakenteellisia ja mekaanisia yhtäläisyyksiä metamfetamiinin kanssa. Yksi mefedroniin liittyvistä voimakkaimmista vaikutuksista on kyky stimuloida dopamiinin (DA) vapautumista ja estää sen takaisinotto vuorovaikutuksen kautta dopamiinin kuljettajan (DAT) kanssa. Vaikka mefedroni ei aiheuta myrkyllisyyttä DA-hermopäätteille, sen kyky toimia DAT:n estäjänä voisi muiden DAT:n estäjien tavoin tarjota suojaa metamfetamiinin aiheuttamaa neurotoksisuutta vastaan. Tämän mahdollisuuden testaamiseksi hiiriä hoidettiin mefedronilla (10, 20 tai 40 mg/kg) ennen jokaista neurotoksisen metamfetamiinin injektiota (4 injektiota 2,5 tai 5,0 mg/kg 2 tunnin välein). Striatumin DA-hermopäätteiden eheyttä arvioitiin mittaamalla DA-, DAT- ja tyrosiinihydroksylaasitasoja. Metamfetamiinin eri annoksiin liittyvää kohtalaista tai vakavaa DA-toksisuutta ei estetty millään mefedroniannoksella, vaan se itse asiassa voimistui merkittävästi. Mefedronin ja metamfetamiinin yhdistelmähoidon aiheuttama hypertermia oli sama kuin jommankumman lääkkeen jälkeen yksinään. Mefedroni tehosti myös amfetamiinin ja MDMA:n neurotoksisia vaikutuksia DA-hermopäätteisiin. Sitä vastoin nomifensiini suojasi metamfetamiinin aiheuttamalta neurotoksisuudelta. Koska mefedroni lisää metamfetamiinin neurotoksisuutta, nämä tulokset viittaavat siihen, että se on vuorovaikutuksessa DAT:n kanssa tavalla, joka poikkeaa muiden tyypillisten DAT-estäjien vuorovaikutuksesta. Pelkän mefedronin suhteellisen harmittomat vaikutukset DA-hermopäätteisiin peittävät alleen potentiaalisesti vaarallisen vuorovaikutuksen lääkkeiden kanssa, joita usein käytetään yhdessä sen kanssa, mikä johtaa lisääntyneeseen neurotoksisuuteen.
Mefedroni (4-metyylimetkatinoni) on katinonijohdannainen ja metamfetamiinin ja 3,4-metyleenidioksi-metamfetamiinin (MDMA) rakenteellinen analogi. Mefedroni on yksi "kylpysuolojen" psykoaktiivisista ainesosista yhdessä muiden yhdisteiden, kuten metyloonin, butyloonin ja 3,4-metyleenidioksipyrovaleronin (MDPV), kanssa. β-ketoamfetamiinien väärinkäyttö lisääntyy jatkuvasti, mikä johtuu suurelta osin siitä, että metamfetamiinin ja MDMA:n synteesiin tarvittavien esiasteiden saatavuus on erittäin rajoitettu laittomissa laboratorioissa ja että niiden puhtaus on vastaavasti vähentynyt (Winstock ym. 2011b, Brunt ym. 2011). β-ketoamfetamiinien väärinkäytön lisääntyessä niiden haittavaikutusten luettelo on kasvanut, ja siihen on lisätty sydän- ja verisuonikomplikaatioita, levottomuutta, unettomuutta, psykoosia ja masennusta (Schifano ym. 2011, Prosser ja Nelson 2012).
Metamfetamiinin ja MDMA:n kemiallisina sukulaisaineina ei ole yllättävää, että β-ketoamfetamiineilla on monia samoja vaikutuksia keskushermostoon kuin näillä entisillä huumeilla. Nämä lääkkeet esimerkiksi estävät dopamiinin (DA) ja serotoniinin (5-HT) kuljettajia (DAT ja SERT) (Cozzi ym. 1999, Rothman ym. 2003, Fleckenstein ym. 2000, Lopez-Arnau ym. 2012) ja ne stimuloivat monoamiinin vapautumista in vitro (Kalix ja Glennon 1986, Gygi ym. 1997, Rothman ym. 2003) ja in vivo (Gygi ym. 1997, Kehr ym. 2011). Metkatinoni aiheuttaa pysyviä vähennyksiä tryptofaanihydroksylaasin ja tyrosiinihydroksylaasin (TH) aktiivisuuteen sekä DA:n ja 5-HT:n ehtymistä (Gygi et al. 1997, Gygi et al. 1996, Sparago et al. 1996). PET-kuvantamistutkimukset metkatinonin käyttäjillä, jotka ovat pidättäytyneet metkatinonin käytöstä, paljastivat vähentyneen striatumin DAT-tiheyden, mikä viittaa DA-päätteiden häviämiseen (McCann ym. 1998). DA:n vapautumisen samanaikainen stimulointi ja sen ottamisen estäminen heijastavat metamfetamiiniin liittyvän neurotoksisuuden taustalla olevia kriittisiä tekijöitä (Kuhn et al. 2008, Yamamoto ja Bankson 2005, Cadet et al. 2007, Fleckenstein et al. 2007).
Me (Angoa-Perez ym. 2012) ja muut (Baumann ym. 2012, Hadlock ym. 2011) tutkimme hiljattain mahdollisuutta, että mefedroni voisi aiheuttaa metamfetamiinin ja MDMA:n tavoin neurotoksisuutta. Yllättäen mefedroni ei ollut myrkyllinen striatumin DA-hermopäätteille (Hadlock ym. 2011, Baumann ym. 2012, Angoa-Perez ym. 2012). Kysymys siitä, vahingoittaako mefedroni 5-HT-hermopäätteitä, on edelleen epäselvä, sillä yksi tutkimus dokumentoi positiivisia vaikutuksia (Hadlock et al. 2011), kun taas toinen oli negatiivinen (Baumann et al. 2012). Ottaen huomioon mefedronin suhteellisen hyvänlaatuisen vaikutuksen DA-hermopäätteisiin ja ottaen huomioon sen ominaisuudet DAT-salpaajana, oletimme, että se voisi itse asiassa suojata DA-neuronaalijärjestelmää metamfetamiinin neurotoksisilta vaikutuksilta, aivan kuten tiedetään tapahtuvan muiden DAT-salpaajien, kuten amfoneelihapon (Pu et ai. 1994, Schmidt ja Gibb 1985, Marek et ai. 1990) ja nomifensiinin (Poth et ai. 2012) kanssa. Raportoimme tällä hetkellä, että mefedroni lisää merkittävästi metamfetamiinin neurotoksisuutta. Tämä vaikutus ulottuu myös amfetamiiniin ja MDMA:han, huumausaineisiin, joita käytetään usein yhdessä mefedronin kanssa (Feyissa ja Kelly 2008, Schifano ym. 2011). Nämä yllättävät tulokset asettavat mefedronin väärinkäytön uuteen valoon ja lisäävät kiireellisesti tämän β-ketoamfetamiinin hienovaraisen ja vaarallisen ominaisuuden tunnustamista.
Aineisto ja menetelmät
Huumeet ja reagenssit
Mefedronihydrokloridi ja 3,4-metyleenidioksimetamfetamiini (MDMA) saatiin NIDA:n tutkimusresurssien huumeiden hankintaohjelmasta. (+) Metamfetamiinihydrokloridi, nomifensiinimaleaatti, d-amfetamiinisulfaatti, pentobarbitaali, DA sekä kaikki puskurit ja HPLC-reagenssit ostettiin Sigma-Aldrichilta (St. Louis, MO, USA). Bikinikoniinihappoproteiinimäärityssarjat saatiin Pierce-yhtiöltä (Rockford, IL, USA). Polyklonaaliset vasta-aineet rotan TH:ta vastaan valmistettiin aiemmin kuvatulla tavalla (Kuhn ja Billingsley 1987). Monoklonaaliset vasta-aineet rotan DAT:tä vastaan saatiin avokätisesti tohtori Roxanne A. Vaughanilta (University of North Dakota, Grand Forks, ND, USA). HRP-konjugoidut anti-IgG-vasta-aineet toimitti Jackson ImmunoResearch Laboratories, Inc. (West Grove, PA, USA).
Eläimet
Naaraspuolisia C57BL/6-hiiriä (Harlan, Indianapolis, IN, USA), jotka painoivat koehetkellä 20-25 g, pidettiin 5 kappaletta häkkiä kohti suurissa kenkälaatikkohäkeissä valoisassa (12 h valoa/pimeää) ja lämpötilakontrolloidussa huoneessa. Naarashiiriä käytettiin, koska niiden tiedetään olevan hyvin herkkiä neurotoksisten amfetamiinien aiheuttamille hermostovaurioille ja jotta säilytettäisiin johdonmukaisuus aiempien metamfetamiinin neurotoksisuutta koskevien tutkimustemme kanssa (Thomas ym. 2010, Thomas ym. 2008, Thomas ym. 2009). Hiirillä oli vapaa pääsy ruokaan ja veteen. Waynen valtionyliopiston institutionaalinen hoito- ja käyttökomitea hyväksyi eläinten hoidon ja kokeelliset menettelyt. Kaikki menettelyt olivat myös NIH:n laboratorioeläinten hoito- ja käyttöoppaan mukaisia.
Farmakologiset, fysiologiset ja käyttäytymiseen liittyvät toimenpiteet
Hiiriä hoidettiin mefedronilla käyttäen humalahakuista hoitoa, joka koostui neljästä 10, 20 tai 40 mg/kg:n injektiosta, joiden välillä oli 2 tunnin väli. Kun tätä humalahoitoohjelmaa käytetään substituoitujen amfetamiinien ja katinonijohdannaisten injektointiin, se johtaa laajaan DA-hermopäätteen vaurioon. Tällä hetkellä käytetyt mefedroniannokset ovat aiemmin osoittautuneet myrkyttömiksi DA-hermopäätteille (Angoa-Perez et al. 2012). Hiiriä hoidettiin metamfetamiinilla (4X 2,5 tai 5 mg/kg), amfetamiinilla (4X 5 mg/kg) tai MDMA:lla (4X 20 mg/kg) yksin tai yhdessä mefedronin kanssa. Kun hiiriä hoidettiin kahdella lääkkeellä, ne saivat mefedroni-injektion 30 minuuttia ennen kutakin neljää metamfetamiini-, amfetamiini- tai MDMA-injektiota. Kontrolliryhmät saivat fysiologista suolaliuosta samalla aikataululla, jota käytettiin mefedronille yksinään tai yhdessä muiden amfetamiinien kanssa. DAT:n estäjän vaikutusten kontrolloimiseksi metamfetamiinin myrkyllisyyteen hiirille annettiin nomifensiinia (4X 5 mg/kg) 30 minuuttia ennen kutakin metamfetamiini-injektiota (4X 5 mg/kg). Kaikki injektiot annettiin i.p.-reitin kautta. Hiiret uhrattiin 2 päivää viimeisen lääkehoidon jälkeen, kun amfetamiiniin liittyvä neurotoksisuus oli saavuttanut maksiminsa. Ruumiinlämpöä seurattiin telemetrisesti käyttämällä Bio Medic Data Systems, Inc:n (Seaford, DE, USA) IPTT-300-istutettavia lämpötilavastaajia. Lämpötilat rekisteröitiin noninvasiivisesti 20 minuutin välein alkaen 60 minuuttia ennen ensimmäistä METH-injektiota ja jatkuen 9 tunnin ajan sen jälkeen Bio Medicin DAS-5001-konsolijärjestelmän avulla.
Striatumin DA-pitoisuuden määrittäminen
Striatal-kudos leikattiin kahdenvälisesti aivoista hoidon jälkeen ja säilytettiin -80 °C:ssa. Pakastetut kudokset punnittiin ja sonikoitiin 10 tilavuudessa 0,16 N perkloorihappoa 4 °C:ssa. Liukenematon proteiini poistettiin sentrifugoimalla ja DA määritettiin HPLC:llä, jossa oli sähkökemiallinen ilmaisin, kuten aiemmin on kuvattu metamfetamiinille (Thomas et al. 2010, Thomas et al, 2009).
TH- ja DAT-proteiinitasojen määrittäminen immunoblottaamalla
Lääkehoitojen vaikutukset striatumin TH- ja DAT-pitoisuuksiin määritettiin immunoblottaamalla striatumin DA-hermopäätteisiin kohdistuvan toksisuuden indeksinä. Hiiret uhrattiin dekapitaatiolla hoidon jälkeen ja striatum leikattiin molemmin puolin. Kudos säilytettiin -80 °C:ssa. Jäädytetty kudos hajotettiin sonikoimalla 1 % SDS:ssä 95 °C:ssa, ja liukenematon aines sedimentoitiin sentrifugoimalla. Proteiini määritettiin bikinikoniinihappomenetelmällä, ja yhtä suuret määrät proteiinia (70 μg/taso) erotettiin SDS-polyakryyliamidigeelielektroforeesilla ja sitten elektroblotattiin nitroselluloosalle. Blotit blokattiin Tris-puskuroidussa suolaliuoksessa, joka sisälsi Tween 20:tä (0,1 % v/v) ja 5 % rasvatonta kuivamaitoa, 1 tunnin ajan huoneenlämmössä. Ensisijaiset vasta-aineet TH:tä (1:1000) tai DAT:tä (1:1000) vastaan lisättiin blotteihin ja annettiin inkuboitua 16 tuntia 4 °C:ssa. Blotit pestiin 3 kertaa Tris-puskuroidulla suolaliuoksella reagoimattomien vasta-aineiden poistamiseksi ja inkuboitiin sitten HRP-konjugoidulla anti-IgG:n sekundäärisellä vasta-aineella (1:4000) 1 tunnin ajan huoneenlämmössä. Immunoreaktiiviset bändit visualisoitiin tehostetulla kemiluminesenssillä ja TH- ja DAT-reaktiivisten bändien suhteelliset tiheydet määritettiin kuvantamalla Kodak Image Stationilla (Carestream Molecular Systems, Rochester, NY, USA) ja kvantifioitiin ImageJ-ohjelmistolla (NIH).
Tietojen analysointi
Kaksisuuntaiset ANOVA:t suoritettiin metamfetamiinin ja mefedronin annosvaikutusten analysoimiseksi DA: n, DAT: n ja TH: n suhteen. Lääkehoitojen vaikutukset striatumin DA-, TH- ja DAT-pitoisuuksiin testattiin merkitsevyydelle yksisuuntaisella ANOVA:lla, jota seurasi Tukeyn moninkertainen vertailutesti. Huumehoitojen tulokset kehon sisälämpötilaan ajan kuluessa analysoitiin kaksisuuntaisella ANOVA:lla, jota seurasi Bonferronin testi lämpötilan erojen merkitsevyyden määrittämiseksi yksittäisinä aikoina hoidon jälkeen. Erot katsottiin merkittäviksi, jos p < 0,05. Kaikki tilastolliset analyysit tehtiin GraphPad Prism -ohjelmiston versiolla 5.02 for Windows (GraphPad Software, San Diego, CA, USA, www.graphpad.com).
Siirry osoitteeseen:
Tulokset
Mefedronin vaikutukset metamfetamiinin aiheuttamaan neurotoksisuuteen
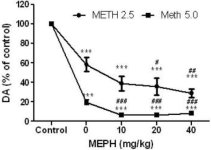
Mefedronia annoksina (10, 20 tai 40 mg/kg), joiden ei tiedetä aiheuttavan DA-hermopäätteen toksisuutta (Angoa-Perez et ai. 2012), annettiin 30 minuuttia ennen kutakin metamfetamiini-injektiota. Metamfetamiinia annettiin annoksina, jotka aiheuttavat kohtalaista (4X 2,5 mg/kg) tai vakavaa (4X 5 mg/kg) vaurioita striatumin DA-hermopäätteille (Thomas ym. 2004, Thomas ym. 2010). Kuvassa 1 esitetyt tulokset osoittavat, että metamfetamiiniannoksen (F1,40 = 66.60, p < 0.0001) ja mefedroniannoksen (F4,40 = 131.3, p < 0.0001) päävaikutukset striatumin DA-tasoihin olivat erittäin merkittäviä kaksisuuntaisella ANOVA:lla. Yhdessä joko 2.5 mg/kg (F4,22 = 35.96, p < 0.001) tai 5.0 mg/kg metamfetamiinin (F4,17 = 953.9, p < 0.0001) kanssa annetun mefedronin päävaikutus oli myös erittäin merkittävä yksisuuntaisella ANOVA:lla. Kaikki käsittelyt jommallakummalla metamfetamiinin ± mefedronin annoksella aiheuttivat merkittävästi suurempia DA: n vähennyksiä verrattuna vastaavaan kontrolliin (p < 0.0001 kaikille). Kuva 1 osoittaa myös, että mefedroniannokset 20 (p < 0,01) ja 40 mg/kg (p < 0,001) lisäsivät merkittävästi 2,5 mg / kg metamfetamiinin DA:ta heikentäviä vaikutuksia, kun taas kaikki mefedroniannokset lisäsivät merkittävästi 5,0 mg / kg metamfetamiinin vaikutuksia DA:n tasoihin (p < 0,0001 kaikkien osalta).
Kuva 1
Mefedronin vaikutukset metamfetamiinin aiheuttamiin striatumin DA:n vähenemisiin. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 min ennen kutakin 2.5 (-) tai 5.0 mg / kg (■) metamfetamiinin (METH) injektiota ja uhrattiin 2d myöhemmin striaatiaalisten DA-tasojen määrittämiseksi HPLC: llä. Tiedot ovat keskiarvoja ± SEM 5-7 hiiristä ryhmää kohti. Jotkin virhepalkit olivat liian pieniä ylittämään symbolien koon, eivätkä ne näy näkyvissä. ***p < 0,001 vs. kontrollit ja #p < 0,01, ##p < 0,001 tai ###p < 0,0001 vs. vastaava metamfetamiiniannos (Tukeyn moninkertainen vertailutesti).
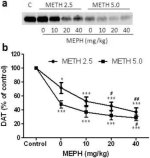
Kuva 2a osoittaa, että mefedroni lisäsi merkittävästi metamfetamiinin aiheuttamaa DAT-tasojen vähenemistä immunoblottauksella määritettynä. Immunoblotsit kvantifioitiin ja DA: n tulosten mukaisesti metamfetamiiniannoksen (F1,92 = 9.48, p < 0.001) ja mefedroniannoksen (F4,92 = 37.56, p < 0.0001) päävaikutukset DAT-tasoihin striatumissa olivat erittäin merkitseviä kaksisuuntaisella ANOVA: lla (Kuva 2b). Yhdessä joko 2.5 mg/kg (F4,56 = 15.55, p < 0.0001) tai 5.0 mg/kg metamfetamiinin (F4,39 = 24.84, p < 0.0001) kanssa annetun mefedronin päävaikutus oli myös erittäin merkittävä yksisuuntaisella ANOVA:lla. Kaikki käsittelyt jommallakummalla metamfetamiinin ± mefedronin annoksella aiheuttivat merkittävästi suurempia DAT-arvon vähennyksiä verrattuna vastaavaan kontrolliin (p < 0.01 pelkälle 2.5 mg / kg metamfetamiinille; p < 0.0001 kaikille muille käsittelyille). Kuva 2b osoittaa myös, että mefedroniannokset 20 mg/kg (p < 0,01) ja 40 mg/kg (p < 0,001) lisäsivät merkittävästi 2,5 mg/kg metamfetamiinin aiheuttamia DAT:n vähennyksiä, kun taas vain 40 mg/kg mefedroniannos lisäsi merkittävästi (p < 0,01) 5,0 mg/kg metamfetamiinin vaikutuksia DAT:n vähennyksiin.
Kuva 2.
Mefedronin vaikutukset metamfetamiinin aiheuttamiin striatumin DAT:n vähennyksiin. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 min ennen kutakin 2.5 (●) tai 5.0 mg / kg (■) metamfetamiinin (METH) injektiota ja uhrattiin 2d myöhemmin striatumin DAT-tasojen määrittämiseksi immunoblottauksella (a). Blotit kvantifioitiin ImageJ: n avulla, ja tiedot ovat keskiarvo ± SEM 10-12 hiirille ryhmää kohti (b). *p < 0,01 tai ***p < 0,0001 vs. kontrolli (C) ja #p < 0,01 tai ##p < 0,001 vs. vastaava metamfetamiiniannos (Tukeyn moninkertainen vertailutesti).
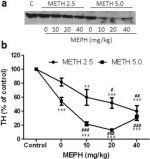
Kuva 3a osoittaa, että mefedroni lisäsi merkittävästi metamfetamiinin aiheuttamaa TH-tasojen vähenemistä immunoblottauksella määritettynä. Immunoblotsit kvantifioitiin, ja edellä DA: n ja DAT: n osalta saatujen tulosten mukaisesti metamfetamiiniannoksen (F1,81 = 47.89, p < 0.0001) ja mefedroniannoksen (F4,81 = 63.57, p < 0.0001) päävaikutukset olivat erittäin merkitseviä kaksisuuntaisella ANOVA: lla (Kuva 3b). Yhdessä joko 2,5 mg/kg (F4,34 = 12,98, p < 0,0001) tai 5,0 mg/kg metamfetamiinin (F4,49 = 99,16, p < 0,0001) kanssa annetun mefedronin päävaikutus oli myös erittäin merkitsevä yksisuuntaisessa ANOVA:ssa. Kaikki käsittelyt jommallakummalla metamfetamiini ± mefedroni -annoksella aiheuttivat merkittävästi suurempia TH:n vähennyksiä verrattuna vastaavaan kontrolliin (p < 0,001, kun kyseessä oli 2,5 mg/kg metamfetamiinia + 10 mg/kg mefedronia; p < 0,0001 kaikkien muiden yhdistelmien osalta) lukuun ottamatta 2,5 mg/kg metamfetamiinia yksinään, joka ei muuttanut TH-tasoja merkittävästi (ts. ei toksisuutta). Kuvasta 3b nähdään myös, että mefedroniannokset 20 mg/kg (p < 0,01) ja 40 mg/kg (p < 0,001) lisäsivät merkittävästi 2,5 mg/kg metamfetamiinin aiheuttamia TH:n vähennyksiä ja kaikki kolme mefedroniannosta lisäsivät merkittävästi (p < 0,0001) 5,0 mg/kg metamfetamiinin vaikutuksia TH:n vähennyksiin.
Kuva 3.
Mefedronin vaikutukset metamfetamiinin aiheuttamiin striatumin TH:n vähennyksiin. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 min ennen kutakin 2,5 (●) tai 5,0 mg / kg (■) metamfetamiinin (METH) injektiota ja uhrattiin 2d myöhemmin TH: n striataalisten TH-tasojen määrittämiseksi immunoblottauksella (a). Blotit kvantifioitiin ImageJ: n avulla, ja tiedot ovat keskiarvo ± SEM 10-12-hiirille ryhmää kohti (b). Jotkin virhepalkit olivat liian pieniä ylittämään symbolien koon, eivätkä ne näy näkyvissä. **p < 0,001 tai ***p < 0,0001 vs. kontrolli (C) ja #p < 0,01, ##p < 0,001 tai ###p < 0,0001) vs. vastaava metamfetamiiniannos (Tukeyn moninkertainen vertailutesti).
Mefedronin vaikutukset metamfetamiinin aiheuttamaan hypertermiaan
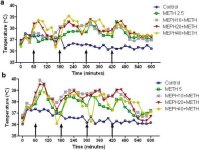
Mefedroni aiheuttaa metamfetamiinin tavoin merkittävää hypertermiaa (Hadlock ym. 2011, Baumann ym. 2012, Angoa-Perez ym. 2012). Kun mefedronia annettiin 30 minuuttia ennen kutakin metamfetamiini-injektiota, kuvasta 4 voidaan nähdä, että metamfetamiini- ja mefedroniannosten päävaikutukset (F1,300 = 11,99, p < 0,0001) ajan suhteen (F4,300 = 51,73, p < 0,0001) olivat erittäin merkitseviä kaksisuuntaisella ANOVA:lla. Päävaikutukset, joita mefedronilla, joka annettiin yhdessä joko 2,5 mg/kg metamfetamiinin (F4,120 = 41,44, p < 0,0001, paneeli a) ajan (F30,120 = 3,84, p < 0,0001) tai 5,0 mg/kg metamfetamiinin (F4,120 = 78,09, p < 0,0001, paneeli b) ajan (F30,120 = 9,98, p < 0,0001) kanssa, olivat myös erittäin merkittäviä kaksisuuntaisen ANOVA:n avulla. Kaikki käsittelyt, joissa käytettiin jompaakumpaa metamfetamiinin ± mefedronin annosta, erosivat merkittävästi vastaavista kontrolleista (p < 0.0001 kaikille käsittelyille).
Kuva 4.
Mefedronin vaikutukset metamfetamiinin aiheuttamaan hypertermiaan. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 minuuttia ennen kutakin 2,5 (a) tai 5,0 mg/kg (b) metamfetamiinin (METH) injektiota. Ydinlämpötilat mitattiin 20 minuutin välein telemetrialla alkaen 60 minuuttia ennen ensimmäistä metamfetamiini-injektiota. Neljä metamfetamiinipistosta on merkitty x-akselilla lepäävillä nuolilla. Tiedot on ilmaistu 6-8 hiiren keskimääräisenä ruumiinlämpötilana ryhmää kohti. SEM:t olivat aina < 10 % keskiarvosta, ja ne on jätetty pois selkeyden vuoksi.
Mefedronin vaikutukset amfetamiinin ja MDMA:n aiheuttamaan neurotoksisuuteen
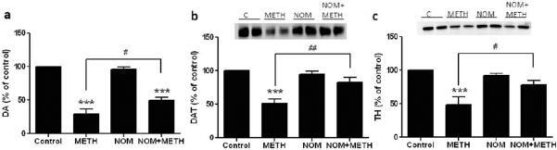
Sen testaamiseksi, voitaisiinko mefedronin metamfetamiinia tehostavat vaikutukset ulottaa koskemaan muita neurotoksisia amfetamiineja, hiiriä hoidettiin tällä β-ketoamfetamiinilla (20 mg/kg) sekä amfetamiinilla (4X 5 mg/kg) tai MDMA:lla (4X 20 mg/kg), ja tulokset on esitetty kuvassa 5. Muistutetaan, että mefedroni itsessään ei vähennä striatumin DA-, DAT- tai TH-arvoja (Angoa-Perez et ai. 2012). Lääkkeen päävaikutus (F5,27 = 27.18, p < 0.0001) oli erittäin merkittävä yksisuuntaisella ANOVA: lla DA-vähennysten osalta (Kuva 5a). Kuvasta 5a voidaan myös nähdä, että kaikki käsittelyt amfetamiinilla (p < 0.001) tai MDMA: lla (p < 0.001) yksinään tai yhdessä mefedronin kanssa (p < 0.0001 molemmille lääkkeille) alensivat merkittävästi DA-tasoja kontrollista. Mefedroni lisäsi merkittävästi amfetamiinin (p < 0.01) tai MDMA: n (p < 0.01) aiheuttamia DA-vähennyksiä. Kuva 5b osoittaa samanlaiset vaikutukset yhdistelmälääkehoitojen DAT-tasoihin striatumissa. Lääkkeen päävaikutus (F4,49 = 42.63, p < 0.0001) oli erittäin merkittävä yksisuuntaisella ANOVA: lla DAT: lle. Kuvasta 5b voidaan myös nähdä, että kaikki amfetamiini- tai MDMA-käsittelyt olivat merkittävästi (p < 0,0001 kaikille) alhaisempia verrattuna kontrolliin. Mefedroni paransi myös merkittävästi joko amfetamiinin tai MDMA:n aiheuttamia DAT-reduktioita (p < 0.0001 molemmissa tapauksissa). Lopuksi kuvio 5c osoittaa, että lääkkeen päävaikutus (F4,50 = 75.06, p < 0.0001) oli erittäin merkittävä yksisuuntaisella ANOVA: lla TH: n vähennysten osalta. Kuvasta 5c voidaan myös nähdä, että kaikki amfetamiini- tai MDMA-käsittelyt olivat merkittävästi (p < 0,0001 kaikille) alhaisempia verrattuna kontrolliin. Mefedroni lisäsi myös merkittävästi joko amfetamiinin tai MDMA:n aiheuttamia TH:n vähennyksiä (p < 0,0001 molemmissa tapauksissa).
Kuva 5.
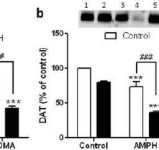
Mefedronin vaikutukset amfetamiinin tai MDMA:n aiheuttamaan DA-hermopäätteiden neurotoksisuuteen. Hiiriä käsiteltiin 20 mg/kg mefedronilla (MEPH) 30 minuuttia ennen kutakin 5,0 mg/kg amfetamiinin (AMPH) tai 20 mg/kg MDMA:n injektiota, ja ne uhrattiin 2d hoidon jälkeen striataalisten (a) DA-pitoisuuksien määrittämiseksi HPLC:llä. (b) DAT ja (c) TH määritettiin immunoblottaamalla ja blotit kvantifioitiin ImageJ: n avulla. DAT:n ja TH:n edustavat immunoblotsit ovat paneelien (b) ja (c) insertteinä, ja molempien paneelien käsittelyt on merkitty seuraavasti: 1,5: kontrolli; 2,6: MEPH; 3: AMPH; 4: AMPH + MEPH; 7: MDMA; ja 8: MDMA + MEPH. Tiedot ovat keskiarvoja ± SEM 5-12 hiirelle kussakin ryhmässä. **p < 0,001 tai ***p < 0,0001 vs. kontrolli ja #p < 0,01 tai ###p < 0,0001 vs. AMPH tai MDMA (Tukeyn moninkertainen vertailutesti).
Nomifensiinin vaikutukset metamfetamiinin aiheuttamaan neurotoksisuuteen
Nomifensiini, voimakas DAT-salpaaja, jolla ei ole tunnettua väärinkäyttö- tai neurotoksista potentiaalia, testattiin sen kyvyn suojata metamfetamiinin aiheuttamalta neurotoksisuudelta ja vastakohtana mefedronin vaikutuksille metamfetamiinin, amfetamiinin ja MDMA:n aiheuttamaan DA-hermopäätteiden toksisuuteen. Kuvassa 6a esitetyt tulokset osoittavat, että lääkkeen päävaikutus (F3,16 = 63,39, p < 0,0001) DA-tasoihin oli erittäin merkittävä yksisuuntaisella ANOVA:lla. Nomifensiini yksinään ei muuttanut DA-tasoja, mutta metamfetamiinin aiheuttama vähennys (p < 0.0001) kumoutui hieman mutta merkittävästi nomifensiinilla (p < 0.01). Lääkkeen päävaikutus (F3,20 = 16.78, p < 0.0001) DAT-tasoihin oli erittäin merkittävä yksisuuntaisella ANOVA: lla, kuten kuvassa 6b on esitetty. Nomifensiini ei muuttanut DAT-tasoja, mutta tarjosi merkittävää suojaa (p < 0.001) metamfetamiinin (p < 0.0001) aiheuttamaa striatumin DAT: n vähenemistä vastaan kontrolliin verrattuna. Lopuksi Kuva 6c osoittaa, että lääkkeen päävaikutus (F3,15 = 14.10, p < 0.0001) TH-tasoihin oli erittäin merkittävä yksisuuntaisella ANOVA: lla. Kuten DA: n ja DAT: n kohdalla nähtiin, metamfetamiinin aiheuttama TH: n väheneminen (p < 0.0001) estettiin hieman mutta merkittävästi nomifensiinillä (p < 0.01).
Kuva 6.
Nomifensiinin vaikutukset metamfetamiinin aiheuttamaan DA-hermopäätteen neurotoksisuuteen. Hiiriä käsiteltiin 5,0 mg / kg nomifensiinillä (NOM) 30 minuuttia ennen kutakin 5,0 mg / kg metamfetamiinin (METH) injektiota, ja ne uhrattiin 2d myöhemmin striatumin (a) DA-pitoisuuksien määrittämiseksi HPLC: llä. (b) DAT ja (c) TH määritettiin immunoblottaamalla ja blotit kvantifioitiin ImageJ: n avulla. DAT:n ja TH:n edustavat immunoblotsit ovat mukana paneelien (b) ja (c) insertteinä. Tiedot ovat keskiarvoja plus SEM 5-7 hiirelle ryhmää kohti. ***p < 0,0001 vs. kontrolli (C) ja #p < 0,01 tai ##p < 0,001 vs. metamfetamiini yksinään (Tukeyn moninkertainen vertailutesti).
Keskustelu
Tämän tutkimuksen tavoitteena oli selvittää, estäisikö mefedroni metamfetamiinin aiheuttamaa DA-hermopäätteiden toksisuutta. Sen kemiallisen samankaltaisuuden perusteella metamfetamiinin ja MDMA:n kanssa odotettiin aluksi, että mefedronilla olisi haitallisia vaikutuksia DA-neuronijärjestelmään. Useissa tutkimuksissa todettiin kuitenkin lähes samanaikaisesti, että mefedroni ei ollut myrkyllistä DA-hermopäätteille (Angoa-Perez ym. 2012, Baumann ym. 2012, Hadlock ym. 2011). Kysymys siitä, aiheuttaako tämä lääke vaurioita 5-HT-neuronaaliselle järjestelmälle, on edelleen avoin. Yhdessä tutkimuksessa raportoitiin 5-HT-hermopäätteiden toiminnan pysyvistä vähenemisistä (Hadlock et al. 2011), kun taas toisessa tutkimuksessa todettiin, että mefedroni ei aiheuttanut vahinkoa (Baumann et al. 2012). Mefedroni on vuorovaikutuksessa DA-hermopäätteen kanssa tavalla, joka viittaa siihen, että se todellakin stimuloi vapautumista ja estää DA:n takaisinottoa vuorovaikutustensa kautta DAT:n kanssa. Metamfetamiinin neurotoksisen vaikutusmekanismin keskeinen puoli on sen kyky päästä DAT:n kautta DA-hermopäätteisiin ja häiritä DA-homeostaasia (Sulzer 2011). Jos tämä metamfetamiinin neurotoksisen kaskadin varhainen vaihe estetään DAT:n estolla, toksisuus estyy (Pu ym. 1994, Poth ym. 2012, Marek ym. 1990, Schmidt ja Gibb 1985). Päättelimme, että mefedronilla voisi olla tämä sama suojaava ominaisuus kuin muilla DAT:n estäjillä, mutta havaitsimme sen sijaan toksisuuden merkittävän lisääntymisen. Tämä vuorovaikutus havaittiin käyttämällä kahta eri metamfetamiiniannosta, jotka aiheuttavat kohtalaisia tai vakavia vaurioita DA-hermopäätteille (4X 2.5 tai 5.0 mg/kg). Tämä mefedronin voimistava vaikutus ei rajoittunut vain metamfetamiiniin, vaan se ulottui myös amfetamiiniin ja MDMA:han, kahteen lääkkeeseen, joita käytetään usein yhdessä mefedronin ja muiden β-ketoamfetamiinien kanssa (Feyissa ja Kelly 2008, Schifano et al. 2011, Kelly 2011). Vaikka mefedroni ei siis aiheuta myrkyllisyyttä ainakaan striatumin DA-hermopäätteille, se voimistaa muiden väärinkäyttöhuumeiden neurotoksisia vaikutuksia. Tämän uuden havainnon pitäisi asettaa mefedronin väärinkäyttö entistäkin jyrkempään valoon, koska sen luontaisen neurotoksisuuden puute saattaa saada sen näyttämään vaarattomalta.
Hypertermia on yleisesti raportoitu metamfetamiinin (Greene ym. 2008) ja β-ketoamfetamiinin nauttimisen akuutti haittavaikutus ihmisillä (Borek ja Holstege 2012, Prosser ja Nelson 2012). Kuten metamfetamiini, myös monet β-ketoamfetamiinihuumeet aiheuttavat jyrsijöillä merkittäviä ydinlämmön kohoamisia (Angoa-Perez ym. 2012, Hadlock ym. 2011, Baumann ym. 2012, Rockhold ym. 1997). Vaikka metamfetamiinin aiheuttama hypertermia voi osaltaan vaikuttaa sen morfologisiin ja hermosoluja vahingoittaviin vaikutuksiin, hypertermia ei välttämättä ole näiden vaikutusten suora syy (Kiyatkin ja Sharma 2009). Mefedronilla ja metamfetamiinilla hoidettujen hiirten kehon sisälämpötilat mitattiin ja havaittiin, että yhdistelmähoito ei nostanut lämpötiloja enempää kuin jommankumman lääkkeen yksinään aiheuttama maksimilämpötilan nousu. Metamfetamiini aiheutti annoksesta riippuvan ruumiinlämmön nousun, ja tämä hypertermia oli muuttumaton koko testatulla mefedroniannosalueella. Itse asiassa mefedronihoidon (Angoa-Perez ym. 2012) jälkeen havaittu ruumiinlämmön lasku injektion jälkeen säilyi mefedronin ja metamfetamiinin suuremmilla annoksilla. Vaikka lääkkeen aiheuttamaa hypertermiaa ei tehostettu yhdistelmähoidolla, neurotoksiset vaikutukset olivat additiivisia. Näin ollen ainakin tässä tapauksessa näyttää siltä, että mefedroni voi tehostaa metamfetamiinin neurotoksisia vaikutuksia tavalla, joka on riippumaton hypertermiasta.
Mefedroni estää selvästi DAT:n toimintaa ja estää DA:n takaisinottoa in vitro (Lopez-Arnau ym. 2012, Hadlock ym. 2011, Kehr ym. 2011, Martinez-Clemente ym. 2012, Cozzi ym. 1999). Mefedroni syrjäyttää WIN-35,428:n DAT:n sitoutumiskohdasta, mikä viittaa siihen, että se on DA:n takaisinoton kilpaileva estäjä (Martinez-Clemente et ai. 2012, Lopez-Arnau et ai. 2012). Mefedronin teho tässä suhteessa on hyvin samankaltainen kuin metamfetamiinin (Cozzi ym. 1999) ja MDMA:n (Escubedo ym. 2011). Ei tiedetä, kulkeutuuko mefedroni DAT:n kautta, mutta metkatinoni kulkeutuu (Cozzi ja Foley 2003). Nomifensiini ja amfoneelihappo, jotka sitoutuvat DAT:hen ja estävät DA:n ottoa, antavat merkittävän suojan metamfetamiinin aiheuttamaa neurotoksisuutta vastaan (Pu ym. 1994, Marek ym. 1990, Schmidt ja Gibb 1985, Poth ym. 2012), ja hiiret, joilta DAT puuttuu, ovat vastustuskykyisiä metamfetamiinin hermostotoksisuudelle (Fumagalli ym. 1998). Tieto siitä, että mefedroni ei ole neurotoksinen ja DAT:n salpaaja, johtaa ennusteeseen, että sen pitäisi estää toksisuutta. Testasimme nomifensiinia tässä suhteessa positiivisena kontrollina ja vahvistimme, että se suojaa metamfetamiinin aiheuttamalta DA:n, DAT:n ja TH:n ehtymiseltä. Nomifensiini estää myös noradrenaliinin kuljettajaa (Brogden ym. 1979), mutta tämä ominaisuus ei voi selittää näitä tuloksia, koska useimmat β-ketoamfetamiinit, mukaan lukien mefedroni, estävät noradrenaliinin kuljettajaa ja estävät noradrenaliinin ottoa (Kelly 2011, Rothman ym. 2003, Cozzi ym. 1999, Sogawa ym. 2011, Lopez-Arnau ym. 2012). 5-HT-neuronaalisen järjestelmän rooli joissakin mefedronin farmakologisissa vaikutuksissa on mahdollinen, kun otetaan huomioon tämän lääkkeen, kuten MDMA:n (Yamamoto et al. 1995), kyky aiheuttaa striatumin DA:n ulosvirtausta vuorovaikutustensa kautta 5-HT2A-reseptorien kanssa (Lopez-Arnau et al. 2012, Martinez-Clemente et al. 2012). Mefedronin aiheuttama hyper-locomotion on riippuvainen endogeenisesta 5-HT:stä (Lopez-Arnau et al. 2012), ja tämä lääke stimuloi myös 5-HT:n vapautumista ja estää sen imeytymistä in vitro (Sogawa et al. 2011, Cozzi et al. 1999, Nagai et al. 2007, Hadlock et al. 2011, Lopez-Arnau et al. 2012, Martinez-Clemente et al. 2012) ja in vivo (Baumann et al. 2012, Kehr et al. 2011). Voimme kuitenkin sulkea pois endogeenisen 5-HT:n roolin ainakin metamfetamiinin DA-neurotoksisuudessa osoittamalla, että 5-HT:n geneettisesti köyhdytetyt hiiret säilyttävät herkkyytensä neurotoksisuudelle (Thomas et ai. 2010).
Mefedroni voisi lisätä metamfetamiinin neurotoksisuutta useilla mahdollisilla mekanismeilla. Ensinnäkin mefedroni voisi olla vuorovaikutuksessa VMAT:n kanssa ja aiheuttaa DA:n vuotoa presynaptisen hermopäätteen sytoplasmaan. Hoidot, jotka lisäävät DA:n sytoplasmallista poolia (eli lääkkeen vapautuvaa), lisäävät metamfetamiinin neurotoksisuutta (Thomas ym. 2008, Thomas ym. 2009, Schmidt ym. 1985). Tämä mekanismi ei ole todennäköinen, koska metkatinoni on vain heikosti vuorovaikutuksessa VMAT:n kanssa (Cozzi ym. 1999). Toiseksi mefedronin ja metamfetamiinin yhdistelmällä voisi olla synergistinen vaikutus DA: n ei-vesikulaariseen vapautumiseen, mutta tämä mahdollisuus vaikuttaa myös epätodennäköiseltä, kun otetaan huomioon tulokset, jotka osoittavat, että DAT- tai SERT-ekspressoivien CHO-solujen käsittelyllä mefedronilla ja metamfetamiinilla ei ole additiivista vaikutusta DA: n tai 5-HT: n vapautumiseen (Sogawa et ai. 2011). Kolmanneksi mefedroni voisi olla vuorovaikutuksessa DAT:n kanssa uudella tavalla, joka edistää additiivista toksisuutta. On osoitettu, että mefedroni yhdessä metamfetamiinin kanssa aiheuttaa synergististä sytotoksisuutta CHO-soluissa, jotka ilmentävät DAT:ää tai SERT:iä, mutta ei villityyppisissä CHO-soluissa, joista puuttuvat transporterit (Sogawa et ai. 2011). Näissä tutkimuksissa viljellyissä soluissa havaittu sytotoksisuus (eli LDH:n vapautuminen) on hyvin erilainen kuin metamfetamiinin aiheuttamat vauriot DA-hermopäätteille, mutta tämä mekanismi viittaa DAT:n mielenkiintoiseen, mutta määrittelemättömään rooliin lisääntyneessä sytotoksisuudessa. Lopuksi mefedroni voisi muuttaa metamfetamiinin metaboliaa. Mefedroni metaboloituu ensisijaisesti N-demetyloitumalla (Meyer ja Maurer 2010), kuten metamfetamiini ja MDMA (Caldwell 1976). Tätä mekanismia tukee osoitus siitä, että metamfetamiini ja MDMA estävät vastavuoroisesti ensisijaisten metaboliittiensa tuotantoa ja nostavat huumeiden plasmapitoisuuksia korkeammiksi kuin ne, jotka havaitaan kumman tahansa huumeen antamisen jälkeen yksinään (Kuwayama ym. 2012). Nyt ja aiemmassa tutkimuksessamme (Angoa-Perez ym. 2012) käytetyt mefedroniannokset ovat suuria, mutta ne eivät ole neurotoksisia ja kuuluvat ihmisten väärinkäytön piiriin (McErath ja O'Neill 2011). Siksi mefedroni saattaa MDMA:n tavoin nostaa metamfetamiinin plasmapitoisuuksia estämällä sen aineenvaihduntaa. Tämän jälkimmäisen mahdollisuuden vahvistamiseksi tarvitaan perusteellinen farmakokineettinen analyysi.
β-ketoamfetamiinien väärinkäyttö lisääntyy hälyttävää vauhtia, ja mefedroni on nyt yksi yleisimmin käytetyistä huumeista kannabiksen, MDMA:n ja kokaiinin jälkeen (Morris 2010, Winstock ym. 2011b). Lisäksi mefedroni aiheuttaa ihmisissä voimakkaamman himon tunteen verrattuna MDMA:han (Brunt ym. 2011), ja mefedronia nuuskaavat käyttäjät pitävät sitä kokaiinia riippuvuutta aiheuttavampana (Winstock ym. 2011b). Ihmiset käyttävät mefedronia humalahakuisesti (eli "pinoamalla"), ja sitä käytetään usein muiden huumeiden, kuten kannabiksen ja amfetamiinipsykostimulanttien, kanssa (Schifano ym. 2011, Fass ym. 2012, Winstock ym. 2011a, Kelly 2011, Torrance ja Cooper 2010). Mefedronia esiintyy yhä useammin MDMA:na myytävissä tableteissa (Brunt ym. 2011), ja sen käyttö ylittää todennäköisesti MDMA:n käytön, kun jälkimmäisen huumeen puhtausaste laskee edelleen (Brunt ym. 2011, Tanner-Smith 2006, Teng ym. 2006). Mefedronin ja muiden "kylpysuolojen" ainesosien yleisten väärinkäyttömallien perusteella on tärkeää pohtia, aiheutuuko ihmisille lisää terveysriskejä, kun näitä huumeita yhdistetään amfetamiinien kanssa tarkoituksellisesti tai tahattomasti. Tuloksemme, jotka osoittavat, että ainakin mefedroni lisää merkittävästi metamfetamiinin, amfetamiinin ja MDMA:n aiheuttamaa striatumin DA-hermopäätteiden neurotoksisuutta, paljastavat tämän β-ketoamfetamiinin erityisen vaarallisen ja odottamattoman ominaisuuden.
Käytetyt lyhenteet
5-HT serotoniini
DA dopamiini
DAT DA DA-siirtäjä
MDMA 3,4-metyleenidioksimetamfetamiini
TH tyrosiinihydroksylaasi
VMAT vesicular monoamine transporter
Mefedroni (4-metyylimetkatinoni) on katinonijohdannainen ja metamfetamiinin ja 3,4-metyleenidioksi-metamfetamiinin (MDMA) rakenteellinen analogi. Mefedroni on yksi "kylpysuolojen" psykoaktiivisista ainesosista yhdessä muiden yhdisteiden, kuten metyloonin, butyloonin ja 3,4-metyleenidioksipyrovaleronin (MDPV), kanssa. β-ketoamfetamiinien väärinkäyttö lisääntyy jatkuvasti, mikä johtuu suurelta osin siitä, että metamfetamiinin ja MDMA:n synteesiin tarvittavien esiasteiden saatavuus on erittäin rajoitettu laittomissa laboratorioissa ja että niiden puhtaus on vastaavasti vähentynyt (Winstock ym. 2011b, Brunt ym. 2011). β-ketoamfetamiinien väärinkäytön lisääntyessä niiden haittavaikutusten luettelo on kasvanut, ja siihen on lisätty sydän- ja verisuonikomplikaatioita, levottomuutta, unettomuutta, psykoosia ja masennusta (Schifano ym. 2011, Prosser ja Nelson 2012).
Metamfetamiinin ja MDMA:n kemiallisina sukulaisaineina ei ole yllättävää, että β-ketoamfetamiineilla on monia samoja vaikutuksia keskushermostoon kuin näillä entisillä huumeilla. Nämä lääkkeet esimerkiksi estävät dopamiinin (DA) ja serotoniinin (5-HT) kuljettajia (DAT ja SERT) (Cozzi ym. 1999, Rothman ym. 2003, Fleckenstein ym. 2000, Lopez-Arnau ym. 2012) ja ne stimuloivat monoamiinin vapautumista in vitro (Kalix ja Glennon 1986, Gygi ym. 1997, Rothman ym. 2003) ja in vivo (Gygi ym. 1997, Kehr ym. 2011). Metkatinoni aiheuttaa pysyviä vähennyksiä tryptofaanihydroksylaasin ja tyrosiinihydroksylaasin (TH) aktiivisuuteen sekä DA:n ja 5-HT:n ehtymistä (Gygi et al. 1997, Gygi et al. 1996, Sparago et al. 1996). PET-kuvantamistutkimukset metkatinonin käyttäjillä, jotka ovat pidättäytyneet metkatinonin käytöstä, paljastivat vähentyneen striatumin DAT-tiheyden, mikä viittaa DA-päätteiden häviämiseen (McCann ym. 1998). DA:n vapautumisen samanaikainen stimulointi ja sen ottamisen estäminen heijastavat metamfetamiiniin liittyvän neurotoksisuuden taustalla olevia kriittisiä tekijöitä (Kuhn et al. 2008, Yamamoto ja Bankson 2005, Cadet et al. 2007, Fleckenstein et al. 2007).
Me (Angoa-Perez ym. 2012) ja muut (Baumann ym. 2012, Hadlock ym. 2011) tutkimme hiljattain mahdollisuutta, että mefedroni voisi aiheuttaa metamfetamiinin ja MDMA:n tavoin neurotoksisuutta. Yllättäen mefedroni ei ollut myrkyllinen striatumin DA-hermopäätteille (Hadlock ym. 2011, Baumann ym. 2012, Angoa-Perez ym. 2012). Kysymys siitä, vahingoittaako mefedroni 5-HT-hermopäätteitä, on edelleen epäselvä, sillä yksi tutkimus dokumentoi positiivisia vaikutuksia (Hadlock et al. 2011), kun taas toinen oli negatiivinen (Baumann et al. 2012). Ottaen huomioon mefedronin suhteellisen hyvänlaatuisen vaikutuksen DA-hermopäätteisiin ja ottaen huomioon sen ominaisuudet DAT-salpaajana, oletimme, että se voisi itse asiassa suojata DA-neuronaalijärjestelmää metamfetamiinin neurotoksisilta vaikutuksilta, aivan kuten tiedetään tapahtuvan muiden DAT-salpaajien, kuten amfoneelihapon (Pu et ai. 1994, Schmidt ja Gibb 1985, Marek et ai. 1990) ja nomifensiinin (Poth et ai. 2012) kanssa. Raportoimme tällä hetkellä, että mefedroni lisää merkittävästi metamfetamiinin neurotoksisuutta. Tämä vaikutus ulottuu myös amfetamiiniin ja MDMA:han, huumausaineisiin, joita käytetään usein yhdessä mefedronin kanssa (Feyissa ja Kelly 2008, Schifano ym. 2011). Nämä yllättävät tulokset asettavat mefedronin väärinkäytön uuteen valoon ja lisäävät kiireellisesti tämän β-ketoamfetamiinin hienovaraisen ja vaarallisen ominaisuuden tunnustamista.
Aineisto ja menetelmät
Huumeet ja reagenssit
Mefedronihydrokloridi ja 3,4-metyleenidioksimetamfetamiini (MDMA) saatiin NIDA:n tutkimusresurssien huumeiden hankintaohjelmasta. (+) Metamfetamiinihydrokloridi, nomifensiinimaleaatti, d-amfetamiinisulfaatti, pentobarbitaali, DA sekä kaikki puskurit ja HPLC-reagenssit ostettiin Sigma-Aldrichilta (St. Louis, MO, USA). Bikinikoniinihappoproteiinimäärityssarjat saatiin Pierce-yhtiöltä (Rockford, IL, USA). Polyklonaaliset vasta-aineet rotan TH:ta vastaan valmistettiin aiemmin kuvatulla tavalla (Kuhn ja Billingsley 1987). Monoklonaaliset vasta-aineet rotan DAT:tä vastaan saatiin avokätisesti tohtori Roxanne A. Vaughanilta (University of North Dakota, Grand Forks, ND, USA). HRP-konjugoidut anti-IgG-vasta-aineet toimitti Jackson ImmunoResearch Laboratories, Inc. (West Grove, PA, USA).
Eläimet
Naaraspuolisia C57BL/6-hiiriä (Harlan, Indianapolis, IN, USA), jotka painoivat koehetkellä 20-25 g, pidettiin 5 kappaletta häkkiä kohti suurissa kenkälaatikkohäkeissä valoisassa (12 h valoa/pimeää) ja lämpötilakontrolloidussa huoneessa. Naarashiiriä käytettiin, koska niiden tiedetään olevan hyvin herkkiä neurotoksisten amfetamiinien aiheuttamille hermostovaurioille ja jotta säilytettäisiin johdonmukaisuus aiempien metamfetamiinin neurotoksisuutta koskevien tutkimustemme kanssa (Thomas ym. 2010, Thomas ym. 2008, Thomas ym. 2009). Hiirillä oli vapaa pääsy ruokaan ja veteen. Waynen valtionyliopiston institutionaalinen hoito- ja käyttökomitea hyväksyi eläinten hoidon ja kokeelliset menettelyt. Kaikki menettelyt olivat myös NIH:n laboratorioeläinten hoito- ja käyttöoppaan mukaisia.
Farmakologiset, fysiologiset ja käyttäytymiseen liittyvät toimenpiteet
Hiiriä hoidettiin mefedronilla käyttäen humalahakuista hoitoa, joka koostui neljästä 10, 20 tai 40 mg/kg:n injektiosta, joiden välillä oli 2 tunnin väli. Kun tätä humalahoitoohjelmaa käytetään substituoitujen amfetamiinien ja katinonijohdannaisten injektointiin, se johtaa laajaan DA-hermopäätteen vaurioon. Tällä hetkellä käytetyt mefedroniannokset ovat aiemmin osoittautuneet myrkyttömiksi DA-hermopäätteille (Angoa-Perez et al. 2012). Hiiriä hoidettiin metamfetamiinilla (4X 2,5 tai 5 mg/kg), amfetamiinilla (4X 5 mg/kg) tai MDMA:lla (4X 20 mg/kg) yksin tai yhdessä mefedronin kanssa. Kun hiiriä hoidettiin kahdella lääkkeellä, ne saivat mefedroni-injektion 30 minuuttia ennen kutakin neljää metamfetamiini-, amfetamiini- tai MDMA-injektiota. Kontrolliryhmät saivat fysiologista suolaliuosta samalla aikataululla, jota käytettiin mefedronille yksinään tai yhdessä muiden amfetamiinien kanssa. DAT:n estäjän vaikutusten kontrolloimiseksi metamfetamiinin myrkyllisyyteen hiirille annettiin nomifensiinia (4X 5 mg/kg) 30 minuuttia ennen kutakin metamfetamiini-injektiota (4X 5 mg/kg). Kaikki injektiot annettiin i.p.-reitin kautta. Hiiret uhrattiin 2 päivää viimeisen lääkehoidon jälkeen, kun amfetamiiniin liittyvä neurotoksisuus oli saavuttanut maksiminsa. Ruumiinlämpöä seurattiin telemetrisesti käyttämällä Bio Medic Data Systems, Inc:n (Seaford, DE, USA) IPTT-300-istutettavia lämpötilavastaajia. Lämpötilat rekisteröitiin noninvasiivisesti 20 minuutin välein alkaen 60 minuuttia ennen ensimmäistä METH-injektiota ja jatkuen 9 tunnin ajan sen jälkeen Bio Medicin DAS-5001-konsolijärjestelmän avulla.
Striatumin DA-pitoisuuden määrittäminen
Striatal-kudos leikattiin kahdenvälisesti aivoista hoidon jälkeen ja säilytettiin -80 °C:ssa. Pakastetut kudokset punnittiin ja sonikoitiin 10 tilavuudessa 0,16 N perkloorihappoa 4 °C:ssa. Liukenematon proteiini poistettiin sentrifugoimalla ja DA määritettiin HPLC:llä, jossa oli sähkökemiallinen ilmaisin, kuten aiemmin on kuvattu metamfetamiinille (Thomas et al. 2010, Thomas et al, 2009).
TH- ja DAT-proteiinitasojen määrittäminen immunoblottaamalla
Lääkehoitojen vaikutukset striatumin TH- ja DAT-pitoisuuksiin määritettiin immunoblottaamalla striatumin DA-hermopäätteisiin kohdistuvan toksisuuden indeksinä. Hiiret uhrattiin dekapitaatiolla hoidon jälkeen ja striatum leikattiin molemmin puolin. Kudos säilytettiin -80 °C:ssa. Jäädytetty kudos hajotettiin sonikoimalla 1 % SDS:ssä 95 °C:ssa, ja liukenematon aines sedimentoitiin sentrifugoimalla. Proteiini määritettiin bikinikoniinihappomenetelmällä, ja yhtä suuret määrät proteiinia (70 μg/taso) erotettiin SDS-polyakryyliamidigeelielektroforeesilla ja sitten elektroblotattiin nitroselluloosalle. Blotit blokattiin Tris-puskuroidussa suolaliuoksessa, joka sisälsi Tween 20:tä (0,1 % v/v) ja 5 % rasvatonta kuivamaitoa, 1 tunnin ajan huoneenlämmössä. Ensisijaiset vasta-aineet TH:tä (1:1000) tai DAT:tä (1:1000) vastaan lisättiin blotteihin ja annettiin inkuboitua 16 tuntia 4 °C:ssa. Blotit pestiin 3 kertaa Tris-puskuroidulla suolaliuoksella reagoimattomien vasta-aineiden poistamiseksi ja inkuboitiin sitten HRP-konjugoidulla anti-IgG:n sekundäärisellä vasta-aineella (1:4000) 1 tunnin ajan huoneenlämmössä. Immunoreaktiiviset bändit visualisoitiin tehostetulla kemiluminesenssillä ja TH- ja DAT-reaktiivisten bändien suhteelliset tiheydet määritettiin kuvantamalla Kodak Image Stationilla (Carestream Molecular Systems, Rochester, NY, USA) ja kvantifioitiin ImageJ-ohjelmistolla (NIH).
Tietojen analysointi
Kaksisuuntaiset ANOVA:t suoritettiin metamfetamiinin ja mefedronin annosvaikutusten analysoimiseksi DA: n, DAT: n ja TH: n suhteen. Lääkehoitojen vaikutukset striatumin DA-, TH- ja DAT-pitoisuuksiin testattiin merkitsevyydelle yksisuuntaisella ANOVA:lla, jota seurasi Tukeyn moninkertainen vertailutesti. Huumehoitojen tulokset kehon sisälämpötilaan ajan kuluessa analysoitiin kaksisuuntaisella ANOVA:lla, jota seurasi Bonferronin testi lämpötilan erojen merkitsevyyden määrittämiseksi yksittäisinä aikoina hoidon jälkeen. Erot katsottiin merkittäviksi, jos p < 0,05. Kaikki tilastolliset analyysit tehtiin GraphPad Prism -ohjelmiston versiolla 5.02 for Windows (GraphPad Software, San Diego, CA, USA, www.graphpad.com).
Siirry osoitteeseen:
Tulokset
Mefedronin vaikutukset metamfetamiinin aiheuttamaan neurotoksisuuteen
Mefedronia annoksina (10, 20 tai 40 mg/kg), joiden ei tiedetä aiheuttavan DA-hermopäätteen toksisuutta (Angoa-Perez et ai. 2012), annettiin 30 minuuttia ennen kutakin metamfetamiini-injektiota. Metamfetamiinia annettiin annoksina, jotka aiheuttavat kohtalaista (4X 2,5 mg/kg) tai vakavaa (4X 5 mg/kg) vaurioita striatumin DA-hermopäätteille (Thomas ym. 2004, Thomas ym. 2010). Kuvassa 1 esitetyt tulokset osoittavat, että metamfetamiiniannoksen (F1,40 = 66.60, p < 0.0001) ja mefedroniannoksen (F4,40 = 131.3, p < 0.0001) päävaikutukset striatumin DA-tasoihin olivat erittäin merkittäviä kaksisuuntaisella ANOVA:lla. Yhdessä joko 2.5 mg/kg (F4,22 = 35.96, p < 0.001) tai 5.0 mg/kg metamfetamiinin (F4,17 = 953.9, p < 0.0001) kanssa annetun mefedronin päävaikutus oli myös erittäin merkittävä yksisuuntaisella ANOVA:lla. Kaikki käsittelyt jommallakummalla metamfetamiinin ± mefedronin annoksella aiheuttivat merkittävästi suurempia DA: n vähennyksiä verrattuna vastaavaan kontrolliin (p < 0.0001 kaikille). Kuva 1 osoittaa myös, että mefedroniannokset 20 (p < 0,01) ja 40 mg/kg (p < 0,001) lisäsivät merkittävästi 2,5 mg / kg metamfetamiinin DA:ta heikentäviä vaikutuksia, kun taas kaikki mefedroniannokset lisäsivät merkittävästi 5,0 mg / kg metamfetamiinin vaikutuksia DA:n tasoihin (p < 0,0001 kaikkien osalta).
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/sywobkqrnd-jpg.47/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Kuva 1
Mefedronin vaikutukset metamfetamiinin aiheuttamiin striatumin DA:n vähenemisiin. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 min ennen kutakin 2.5 (-) tai 5.0 mg / kg (■) metamfetamiinin (METH) injektiota ja uhrattiin 2d myöhemmin striaatiaalisten DA-tasojen määrittämiseksi HPLC: llä. Tiedot ovat keskiarvoja ± SEM 5-7 hiiristä ryhmää kohti. Jotkin virhepalkit olivat liian pieniä ylittämään symbolien koon, eivätkä ne näy näkyvissä. ***p < 0,001 vs. kontrollit ja #p < 0,01, ##p < 0,001 tai ###p < 0,0001 vs. vastaava metamfetamiiniannos (Tukeyn moninkertainen vertailutesti).
Kuva 2a osoittaa, että mefedroni lisäsi merkittävästi metamfetamiinin aiheuttamaa DAT-tasojen vähenemistä immunoblottauksella määritettynä. Immunoblotsit kvantifioitiin ja DA: n tulosten mukaisesti metamfetamiiniannoksen (F1,92 = 9.48, p < 0.001) ja mefedroniannoksen (F4,92 = 37.56, p < 0.0001) päävaikutukset DAT-tasoihin striatumissa olivat erittäin merkitseviä kaksisuuntaisella ANOVA: lla (Kuva 2b). Yhdessä joko 2.5 mg/kg (F4,56 = 15.55, p < 0.0001) tai 5.0 mg/kg metamfetamiinin (F4,39 = 24.84, p < 0.0001) kanssa annetun mefedronin päävaikutus oli myös erittäin merkittävä yksisuuntaisella ANOVA:lla. Kaikki käsittelyt jommallakummalla metamfetamiinin ± mefedronin annoksella aiheuttivat merkittävästi suurempia DAT-arvon vähennyksiä verrattuna vastaavaan kontrolliin (p < 0.01 pelkälle 2.5 mg / kg metamfetamiinille; p < 0.0001 kaikille muille käsittelyille). Kuva 2b osoittaa myös, että mefedroniannokset 20 mg/kg (p < 0,01) ja 40 mg/kg (p < 0,001) lisäsivät merkittävästi 2,5 mg/kg metamfetamiinin aiheuttamia DAT:n vähennyksiä, kun taas vain 40 mg/kg mefedroniannos lisäsi merkittävästi (p < 0,01) 5,0 mg/kg metamfetamiinin vaikutuksia DAT:n vähennyksiin.
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/bfu3sx5dnr-jpg.4797/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Kuva 2.
Mefedronin vaikutukset metamfetamiinin aiheuttamiin striatumin DAT:n vähennyksiin. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 min ennen kutakin 2.5 (●) tai 5.0 mg / kg (■) metamfetamiinin (METH) injektiota ja uhrattiin 2d myöhemmin striatumin DAT-tasojen määrittämiseksi immunoblottauksella (a). Blotit kvantifioitiin ImageJ: n avulla, ja tiedot ovat keskiarvo ± SEM 10-12 hiirille ryhmää kohti (b). *p < 0,01 tai ***p < 0,0001 vs. kontrolli (C) ja #p < 0,01 tai ##p < 0,001 vs. vastaava metamfetamiiniannos (Tukeyn moninkertainen vertailutesti).
Kuva 3a osoittaa, että mefedroni lisäsi merkittävästi metamfetamiinin aiheuttamaa TH-tasojen vähenemistä immunoblottauksella määritettynä. Immunoblotsit kvantifioitiin, ja edellä DA: n ja DAT: n osalta saatujen tulosten mukaisesti metamfetamiiniannoksen (F1,81 = 47.89, p < 0.0001) ja mefedroniannoksen (F4,81 = 63.57, p < 0.0001) päävaikutukset olivat erittäin merkitseviä kaksisuuntaisella ANOVA: lla (Kuva 3b). Yhdessä joko 2,5 mg/kg (F4,34 = 12,98, p < 0,0001) tai 5,0 mg/kg metamfetamiinin (F4,49 = 99,16, p < 0,0001) kanssa annetun mefedronin päävaikutus oli myös erittäin merkitsevä yksisuuntaisessa ANOVA:ssa. Kaikki käsittelyt jommallakummalla metamfetamiini ± mefedroni -annoksella aiheuttivat merkittävästi suurempia TH:n vähennyksiä verrattuna vastaavaan kontrolliin (p < 0,001, kun kyseessä oli 2,5 mg/kg metamfetamiinia + 10 mg/kg mefedronia; p < 0,0001 kaikkien muiden yhdistelmien osalta) lukuun ottamatta 2,5 mg/kg metamfetamiinia yksinään, joka ei muuttanut TH-tasoja merkittävästi (ts. ei toksisuutta). Kuvasta 3b nähdään myös, että mefedroniannokset 20 mg/kg (p < 0,01) ja 40 mg/kg (p < 0,001) lisäsivät merkittävästi 2,5 mg/kg metamfetamiinin aiheuttamia TH:n vähennyksiä ja kaikki kolme mefedroniannosta lisäsivät merkittävästi (p < 0,0001) 5,0 mg/kg metamfetamiinin vaikutuksia TH:n vähennyksiin.
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/tggfrjpqru-jpg.4798/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Kuva 3.
Mefedronin vaikutukset metamfetamiinin aiheuttamiin striatumin TH:n vähennyksiin. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 min ennen kutakin 2,5 (●) tai 5,0 mg / kg (■) metamfetamiinin (METH) injektiota ja uhrattiin 2d myöhemmin TH: n striataalisten TH-tasojen määrittämiseksi immunoblottauksella (a). Blotit kvantifioitiin ImageJ: n avulla, ja tiedot ovat keskiarvo ± SEM 10-12-hiirille ryhmää kohti (b). Jotkin virhepalkit olivat liian pieniä ylittämään symbolien koon, eivätkä ne näy näkyvissä. **p < 0,001 tai ***p < 0,0001 vs. kontrolli (C) ja #p < 0,01, ##p < 0,001 tai ###p < 0,0001) vs. vastaava metamfetamiiniannos (Tukeyn moninkertainen vertailutesti).
Mefedronin vaikutukset metamfetamiinin aiheuttamaan hypertermiaan
Mefedroni aiheuttaa metamfetamiinin tavoin merkittävää hypertermiaa (Hadlock ym. 2011, Baumann ym. 2012, Angoa-Perez ym. 2012). Kun mefedronia annettiin 30 minuuttia ennen kutakin metamfetamiini-injektiota, kuvasta 4 voidaan nähdä, että metamfetamiini- ja mefedroniannosten päävaikutukset (F1,300 = 11,99, p < 0,0001) ajan suhteen (F4,300 = 51,73, p < 0,0001) olivat erittäin merkitseviä kaksisuuntaisella ANOVA:lla. Päävaikutukset, joita mefedronilla, joka annettiin yhdessä joko 2,5 mg/kg metamfetamiinin (F4,120 = 41,44, p < 0,0001, paneeli a) ajan (F30,120 = 3,84, p < 0,0001) tai 5,0 mg/kg metamfetamiinin (F4,120 = 78,09, p < 0,0001, paneeli b) ajan (F30,120 = 9,98, p < 0,0001) kanssa, olivat myös erittäin merkittäviä kaksisuuntaisen ANOVA:n avulla. Kaikki käsittelyt, joissa käytettiin jompaakumpaa metamfetamiinin ± mefedronin annosta, erosivat merkittävästi vastaavista kontrolleista (p < 0.0001 kaikille käsittelyille).
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/x0ik9hdwsw-jpg.4799/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Kuva 4.
Mefedronin vaikutukset metamfetamiinin aiheuttamaan hypertermiaan. Hiiriä käsiteltiin ilmoitetuilla mefedroniannoksilla (MEPH) 30 minuuttia ennen kutakin 2,5 (a) tai 5,0 mg/kg (b) metamfetamiinin (METH) injektiota. Ydinlämpötilat mitattiin 20 minuutin välein telemetrialla alkaen 60 minuuttia ennen ensimmäistä metamfetamiini-injektiota. Neljä metamfetamiinipistosta on merkitty x-akselilla lepäävillä nuolilla. Tiedot on ilmaistu 6-8 hiiren keskimääräisenä ruumiinlämpötilana ryhmää kohti. SEM:t olivat aina < 10 % keskiarvosta, ja ne on jätetty pois selkeyden vuoksi.
Mefedronin vaikutukset amfetamiinin ja MDMA:n aiheuttamaan neurotoksisuuteen
Sen testaamiseksi, voitaisiinko mefedronin metamfetamiinia tehostavat vaikutukset ulottaa koskemaan muita neurotoksisia amfetamiineja, hiiriä hoidettiin tällä β-ketoamfetamiinilla (20 mg/kg) sekä amfetamiinilla (4X 5 mg/kg) tai MDMA:lla (4X 20 mg/kg), ja tulokset on esitetty kuvassa 5. Muistutetaan, että mefedroni itsessään ei vähennä striatumin DA-, DAT- tai TH-arvoja (Angoa-Perez et ai. 2012). Lääkkeen päävaikutus (F5,27 = 27.18, p < 0.0001) oli erittäin merkittävä yksisuuntaisella ANOVA: lla DA-vähennysten osalta (Kuva 5a). Kuvasta 5a voidaan myös nähdä, että kaikki käsittelyt amfetamiinilla (p < 0.001) tai MDMA: lla (p < 0.001) yksinään tai yhdessä mefedronin kanssa (p < 0.0001 molemmille lääkkeille) alensivat merkittävästi DA-tasoja kontrollista. Mefedroni lisäsi merkittävästi amfetamiinin (p < 0.01) tai MDMA: n (p < 0.01) aiheuttamia DA-vähennyksiä. Kuva 5b osoittaa samanlaiset vaikutukset yhdistelmälääkehoitojen DAT-tasoihin striatumissa. Lääkkeen päävaikutus (F4,49 = 42.63, p < 0.0001) oli erittäin merkittävä yksisuuntaisella ANOVA: lla DAT: lle. Kuvasta 5b voidaan myös nähdä, että kaikki amfetamiini- tai MDMA-käsittelyt olivat merkittävästi (p < 0,0001 kaikille) alhaisempia verrattuna kontrolliin. Mefedroni paransi myös merkittävästi joko amfetamiinin tai MDMA:n aiheuttamia DAT-reduktioita (p < 0.0001 molemmissa tapauksissa). Lopuksi kuvio 5c osoittaa, että lääkkeen päävaikutus (F4,50 = 75.06, p < 0.0001) oli erittäin merkittävä yksisuuntaisella ANOVA: lla TH: n vähennysten osalta. Kuvasta 5c voidaan myös nähdä, että kaikki amfetamiini- tai MDMA-käsittelyt olivat merkittävästi (p < 0,0001 kaikille) alhaisempia verrattuna kontrolliin. Mefedroni lisäsi myös merkittävästi joko amfetamiinin tai MDMA:n aiheuttamia TH:n vähennyksiä (p < 0,0001 molemmissa tapauksissa).
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/onvypkgxvn-jpg.4800/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Kuva 5.
Mefedronin vaikutukset amfetamiinin tai MDMA:n aiheuttamaan DA-hermopäätteiden neurotoksisuuteen. Hiiriä käsiteltiin 20 mg/kg mefedronilla (MEPH) 30 minuuttia ennen kutakin 5,0 mg/kg amfetamiinin (AMPH) tai 20 mg/kg MDMA:n injektiota, ja ne uhrattiin 2d hoidon jälkeen striataalisten (a) DA-pitoisuuksien määrittämiseksi HPLC:llä. (b) DAT ja (c) TH määritettiin immunoblottaamalla ja blotit kvantifioitiin ImageJ: n avulla. DAT:n ja TH:n edustavat immunoblotsit ovat paneelien (b) ja (c) insertteinä, ja molempien paneelien käsittelyt on merkitty seuraavasti: 1,5: kontrolli; 2,6: MEPH; 3: AMPH; 4: AMPH + MEPH; 7: MDMA; ja 8: MDMA + MEPH. Tiedot ovat keskiarvoja ± SEM 5-12 hiirelle kussakin ryhmässä. **p < 0,001 tai ***p < 0,0001 vs. kontrolli ja #p < 0,01 tai ###p < 0,0001 vs. AMPH tai MDMA (Tukeyn moninkertainen vertailutesti).
Nomifensiinin vaikutukset metamfetamiinin aiheuttamaan neurotoksisuuteen
Nomifensiini, voimakas DAT-salpaaja, jolla ei ole tunnettua väärinkäyttö- tai neurotoksista potentiaalia, testattiin sen kyvyn suojata metamfetamiinin aiheuttamalta neurotoksisuudelta ja vastakohtana mefedronin vaikutuksille metamfetamiinin, amfetamiinin ja MDMA:n aiheuttamaan DA-hermopäätteiden toksisuuteen. Kuvassa 6a esitetyt tulokset osoittavat, että lääkkeen päävaikutus (F3,16 = 63,39, p < 0,0001) DA-tasoihin oli erittäin merkittävä yksisuuntaisella ANOVA:lla. Nomifensiini yksinään ei muuttanut DA-tasoja, mutta metamfetamiinin aiheuttama vähennys (p < 0.0001) kumoutui hieman mutta merkittävästi nomifensiinilla (p < 0.01). Lääkkeen päävaikutus (F3,20 = 16.78, p < 0.0001) DAT-tasoihin oli erittäin merkittävä yksisuuntaisella ANOVA: lla, kuten kuvassa 6b on esitetty. Nomifensiini ei muuttanut DAT-tasoja, mutta tarjosi merkittävää suojaa (p < 0.001) metamfetamiinin (p < 0.0001) aiheuttamaa striatumin DAT: n vähenemistä vastaan kontrolliin verrattuna. Lopuksi Kuva 6c osoittaa, että lääkkeen päävaikutus (F3,15 = 14.10, p < 0.0001) TH-tasoihin oli erittäin merkittävä yksisuuntaisella ANOVA: lla. Kuten DA: n ja DAT: n kohdalla nähtiin, metamfetamiinin aiheuttama TH: n väheneminen (p < 0.0001) estettiin hieman mutta merkittävästi nomifensiinillä (p < 0.01).
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/daczg9cwfv-jpg.4801/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Kuva 6.
Nomifensiinin vaikutukset metamfetamiinin aiheuttamaan DA-hermopäätteen neurotoksisuuteen. Hiiriä käsiteltiin 5,0 mg / kg nomifensiinillä (NOM) 30 minuuttia ennen kutakin 5,0 mg / kg metamfetamiinin (METH) injektiota, ja ne uhrattiin 2d myöhemmin striatumin (a) DA-pitoisuuksien määrittämiseksi HPLC: llä. (b) DAT ja (c) TH määritettiin immunoblottaamalla ja blotit kvantifioitiin ImageJ: n avulla. DAT:n ja TH:n edustavat immunoblotsit ovat mukana paneelien (b) ja (c) insertteinä. Tiedot ovat keskiarvoja plus SEM 5-7 hiirelle ryhmää kohti. ***p < 0,0001 vs. kontrolli (C) ja #p < 0,01 tai ##p < 0,001 vs. metamfetamiini yksinään (Tukeyn moninkertainen vertailutesti).
Keskustelu
Tämän tutkimuksen tavoitteena oli selvittää, estäisikö mefedroni metamfetamiinin aiheuttamaa DA-hermopäätteiden toksisuutta. Sen kemiallisen samankaltaisuuden perusteella metamfetamiinin ja MDMA:n kanssa odotettiin aluksi, että mefedronilla olisi haitallisia vaikutuksia DA-neuronijärjestelmään. Useissa tutkimuksissa todettiin kuitenkin lähes samanaikaisesti, että mefedroni ei ollut myrkyllistä DA-hermopäätteille (Angoa-Perez ym. 2012, Baumann ym. 2012, Hadlock ym. 2011). Kysymys siitä, aiheuttaako tämä lääke vaurioita 5-HT-neuronaaliselle järjestelmälle, on edelleen avoin. Yhdessä tutkimuksessa raportoitiin 5-HT-hermopäätteiden toiminnan pysyvistä vähenemisistä (Hadlock et al. 2011), kun taas toisessa tutkimuksessa todettiin, että mefedroni ei aiheuttanut vahinkoa (Baumann et al. 2012). Mefedroni on vuorovaikutuksessa DA-hermopäätteen kanssa tavalla, joka viittaa siihen, että se todellakin stimuloi vapautumista ja estää DA:n takaisinottoa vuorovaikutustensa kautta DAT:n kanssa. Metamfetamiinin neurotoksisen vaikutusmekanismin keskeinen puoli on sen kyky päästä DAT:n kautta DA-hermopäätteisiin ja häiritä DA-homeostaasia (Sulzer 2011). Jos tämä metamfetamiinin neurotoksisen kaskadin varhainen vaihe estetään DAT:n estolla, toksisuus estyy (Pu ym. 1994, Poth ym. 2012, Marek ym. 1990, Schmidt ja Gibb 1985). Päättelimme, että mefedronilla voisi olla tämä sama suojaava ominaisuus kuin muilla DAT:n estäjillä, mutta havaitsimme sen sijaan toksisuuden merkittävän lisääntymisen. Tämä vuorovaikutus havaittiin käyttämällä kahta eri metamfetamiiniannosta, jotka aiheuttavat kohtalaisia tai vakavia vaurioita DA-hermopäätteille (4X 2.5 tai 5.0 mg/kg). Tämä mefedronin voimistava vaikutus ei rajoittunut vain metamfetamiiniin, vaan se ulottui myös amfetamiiniin ja MDMA:han, kahteen lääkkeeseen, joita käytetään usein yhdessä mefedronin ja muiden β-ketoamfetamiinien kanssa (Feyissa ja Kelly 2008, Schifano et al. 2011, Kelly 2011). Vaikka mefedroni ei siis aiheuta myrkyllisyyttä ainakaan striatumin DA-hermopäätteille, se voimistaa muiden väärinkäyttöhuumeiden neurotoksisia vaikutuksia. Tämän uuden havainnon pitäisi asettaa mefedronin väärinkäyttö entistäkin jyrkempään valoon, koska sen luontaisen neurotoksisuuden puute saattaa saada sen näyttämään vaarattomalta.
Hypertermia on yleisesti raportoitu metamfetamiinin (Greene ym. 2008) ja β-ketoamfetamiinin nauttimisen akuutti haittavaikutus ihmisillä (Borek ja Holstege 2012, Prosser ja Nelson 2012). Kuten metamfetamiini, myös monet β-ketoamfetamiinihuumeet aiheuttavat jyrsijöillä merkittäviä ydinlämmön kohoamisia (Angoa-Perez ym. 2012, Hadlock ym. 2011, Baumann ym. 2012, Rockhold ym. 1997). Vaikka metamfetamiinin aiheuttama hypertermia voi osaltaan vaikuttaa sen morfologisiin ja hermosoluja vahingoittaviin vaikutuksiin, hypertermia ei välttämättä ole näiden vaikutusten suora syy (Kiyatkin ja Sharma 2009). Mefedronilla ja metamfetamiinilla hoidettujen hiirten kehon sisälämpötilat mitattiin ja havaittiin, että yhdistelmähoito ei nostanut lämpötiloja enempää kuin jommankumman lääkkeen yksinään aiheuttama maksimilämpötilan nousu. Metamfetamiini aiheutti annoksesta riippuvan ruumiinlämmön nousun, ja tämä hypertermia oli muuttumaton koko testatulla mefedroniannosalueella. Itse asiassa mefedronihoidon (Angoa-Perez ym. 2012) jälkeen havaittu ruumiinlämmön lasku injektion jälkeen säilyi mefedronin ja metamfetamiinin suuremmilla annoksilla. Vaikka lääkkeen aiheuttamaa hypertermiaa ei tehostettu yhdistelmähoidolla, neurotoksiset vaikutukset olivat additiivisia. Näin ollen ainakin tässä tapauksessa näyttää siltä, että mefedroni voi tehostaa metamfetamiinin neurotoksisia vaikutuksia tavalla, joka on riippumaton hypertermiasta.
Mefedroni estää selvästi DAT:n toimintaa ja estää DA:n takaisinottoa in vitro (Lopez-Arnau ym. 2012, Hadlock ym. 2011, Kehr ym. 2011, Martinez-Clemente ym. 2012, Cozzi ym. 1999). Mefedroni syrjäyttää WIN-35,428:n DAT:n sitoutumiskohdasta, mikä viittaa siihen, että se on DA:n takaisinoton kilpaileva estäjä (Martinez-Clemente et ai. 2012, Lopez-Arnau et ai. 2012). Mefedronin teho tässä suhteessa on hyvin samankaltainen kuin metamfetamiinin (Cozzi ym. 1999) ja MDMA:n (Escubedo ym. 2011). Ei tiedetä, kulkeutuuko mefedroni DAT:n kautta, mutta metkatinoni kulkeutuu (Cozzi ja Foley 2003). Nomifensiini ja amfoneelihappo, jotka sitoutuvat DAT:hen ja estävät DA:n ottoa, antavat merkittävän suojan metamfetamiinin aiheuttamaa neurotoksisuutta vastaan (Pu ym. 1994, Marek ym. 1990, Schmidt ja Gibb 1985, Poth ym. 2012), ja hiiret, joilta DAT puuttuu, ovat vastustuskykyisiä metamfetamiinin hermostotoksisuudelle (Fumagalli ym. 1998). Tieto siitä, että mefedroni ei ole neurotoksinen ja DAT:n salpaaja, johtaa ennusteeseen, että sen pitäisi estää toksisuutta. Testasimme nomifensiinia tässä suhteessa positiivisena kontrollina ja vahvistimme, että se suojaa metamfetamiinin aiheuttamalta DA:n, DAT:n ja TH:n ehtymiseltä. Nomifensiini estää myös noradrenaliinin kuljettajaa (Brogden ym. 1979), mutta tämä ominaisuus ei voi selittää näitä tuloksia, koska useimmat β-ketoamfetamiinit, mukaan lukien mefedroni, estävät noradrenaliinin kuljettajaa ja estävät noradrenaliinin ottoa (Kelly 2011, Rothman ym. 2003, Cozzi ym. 1999, Sogawa ym. 2011, Lopez-Arnau ym. 2012). 5-HT-neuronaalisen järjestelmän rooli joissakin mefedronin farmakologisissa vaikutuksissa on mahdollinen, kun otetaan huomioon tämän lääkkeen, kuten MDMA:n (Yamamoto et al. 1995), kyky aiheuttaa striatumin DA:n ulosvirtausta vuorovaikutustensa kautta 5-HT2A-reseptorien kanssa (Lopez-Arnau et al. 2012, Martinez-Clemente et al. 2012). Mefedronin aiheuttama hyper-locomotion on riippuvainen endogeenisesta 5-HT:stä (Lopez-Arnau et al. 2012), ja tämä lääke stimuloi myös 5-HT:n vapautumista ja estää sen imeytymistä in vitro (Sogawa et al. 2011, Cozzi et al. 1999, Nagai et al. 2007, Hadlock et al. 2011, Lopez-Arnau et al. 2012, Martinez-Clemente et al. 2012) ja in vivo (Baumann et al. 2012, Kehr et al. 2011). Voimme kuitenkin sulkea pois endogeenisen 5-HT:n roolin ainakin metamfetamiinin DA-neurotoksisuudessa osoittamalla, että 5-HT:n geneettisesti köyhdytetyt hiiret säilyttävät herkkyytensä neurotoksisuudelle (Thomas et ai. 2010).
Mefedroni voisi lisätä metamfetamiinin neurotoksisuutta useilla mahdollisilla mekanismeilla. Ensinnäkin mefedroni voisi olla vuorovaikutuksessa VMAT:n kanssa ja aiheuttaa DA:n vuotoa presynaptisen hermopäätteen sytoplasmaan. Hoidot, jotka lisäävät DA:n sytoplasmallista poolia (eli lääkkeen vapautuvaa), lisäävät metamfetamiinin neurotoksisuutta (Thomas ym. 2008, Thomas ym. 2009, Schmidt ym. 1985). Tämä mekanismi ei ole todennäköinen, koska metkatinoni on vain heikosti vuorovaikutuksessa VMAT:n kanssa (Cozzi ym. 1999). Toiseksi mefedronin ja metamfetamiinin yhdistelmällä voisi olla synergistinen vaikutus DA: n ei-vesikulaariseen vapautumiseen, mutta tämä mahdollisuus vaikuttaa myös epätodennäköiseltä, kun otetaan huomioon tulokset, jotka osoittavat, että DAT- tai SERT-ekspressoivien CHO-solujen käsittelyllä mefedronilla ja metamfetamiinilla ei ole additiivista vaikutusta DA: n tai 5-HT: n vapautumiseen (Sogawa et ai. 2011). Kolmanneksi mefedroni voisi olla vuorovaikutuksessa DAT:n kanssa uudella tavalla, joka edistää additiivista toksisuutta. On osoitettu, että mefedroni yhdessä metamfetamiinin kanssa aiheuttaa synergististä sytotoksisuutta CHO-soluissa, jotka ilmentävät DAT:ää tai SERT:iä, mutta ei villityyppisissä CHO-soluissa, joista puuttuvat transporterit (Sogawa et ai. 2011). Näissä tutkimuksissa viljellyissä soluissa havaittu sytotoksisuus (eli LDH:n vapautuminen) on hyvin erilainen kuin metamfetamiinin aiheuttamat vauriot DA-hermopäätteille, mutta tämä mekanismi viittaa DAT:n mielenkiintoiseen, mutta määrittelemättömään rooliin lisääntyneessä sytotoksisuudessa. Lopuksi mefedroni voisi muuttaa metamfetamiinin metaboliaa. Mefedroni metaboloituu ensisijaisesti N-demetyloitumalla (Meyer ja Maurer 2010), kuten metamfetamiini ja MDMA (Caldwell 1976). Tätä mekanismia tukee osoitus siitä, että metamfetamiini ja MDMA estävät vastavuoroisesti ensisijaisten metaboliittiensa tuotantoa ja nostavat huumeiden plasmapitoisuuksia korkeammiksi kuin ne, jotka havaitaan kumman tahansa huumeen antamisen jälkeen yksinään (Kuwayama ym. 2012). Nyt ja aiemmassa tutkimuksessamme (Angoa-Perez ym. 2012) käytetyt mefedroniannokset ovat suuria, mutta ne eivät ole neurotoksisia ja kuuluvat ihmisten väärinkäytön piiriin (McErath ja O'Neill 2011). Siksi mefedroni saattaa MDMA:n tavoin nostaa metamfetamiinin plasmapitoisuuksia estämällä sen aineenvaihduntaa. Tämän jälkimmäisen mahdollisuuden vahvistamiseksi tarvitaan perusteellinen farmakokineettinen analyysi.
β-ketoamfetamiinien väärinkäyttö lisääntyy hälyttävää vauhtia, ja mefedroni on nyt yksi yleisimmin käytetyistä huumeista kannabiksen, MDMA:n ja kokaiinin jälkeen (Morris 2010, Winstock ym. 2011b). Lisäksi mefedroni aiheuttaa ihmisissä voimakkaamman himon tunteen verrattuna MDMA:han (Brunt ym. 2011), ja mefedronia nuuskaavat käyttäjät pitävät sitä kokaiinia riippuvuutta aiheuttavampana (Winstock ym. 2011b). Ihmiset käyttävät mefedronia humalahakuisesti (eli "pinoamalla"), ja sitä käytetään usein muiden huumeiden, kuten kannabiksen ja amfetamiinipsykostimulanttien, kanssa (Schifano ym. 2011, Fass ym. 2012, Winstock ym. 2011a, Kelly 2011, Torrance ja Cooper 2010). Mefedronia esiintyy yhä useammin MDMA:na myytävissä tableteissa (Brunt ym. 2011), ja sen käyttö ylittää todennäköisesti MDMA:n käytön, kun jälkimmäisen huumeen puhtausaste laskee edelleen (Brunt ym. 2011, Tanner-Smith 2006, Teng ym. 2006). Mefedronin ja muiden "kylpysuolojen" ainesosien yleisten väärinkäyttömallien perusteella on tärkeää pohtia, aiheutuuko ihmisille lisää terveysriskejä, kun näitä huumeita yhdistetään amfetamiinien kanssa tarkoituksellisesti tai tahattomasti. Tuloksemme, jotka osoittavat, että ainakin mefedroni lisää merkittävästi metamfetamiinin, amfetamiinin ja MDMA:n aiheuttamaa striatumin DA-hermopäätteiden neurotoksisuutta, paljastavat tämän β-ketoamfetamiinin erityisen vaarallisen ja odottamattoman ominaisuuden.
Käytetyt lyhenteet
5-HT serotoniini
DA dopamiini
DAT DA DA-siirtäjä
MDMA 3,4-metyleenidioksimetamfetamiini
TH tyrosiinihydroksylaasi
VMAT vesicular monoamine transporter