- Joined
- Mar 27, 2022
- Messages
- 47
- Reaction score
- 27
- Points
- 8
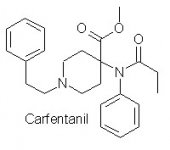
Synthèse du carfentanil
"Par exemple, le carfentanil est environ 4 000 fois plus puissant que l'héroïne et possède un index thérapeutique extrêmement favorable [...]. Par conséquent, une semaine de travail facile pour deux chimistes pourrait fournir 1 (un) kilogramme de carfentanil, ce qui équivaudrait à quatre tonnes métriques d'héroïne pure"
A un mélange de 102 parties de phénéthyl-pipéridone-4, 47 parties d'aniline et 370 parties d'acide acétique, on ajoute goutte à goutte une solution de 36 parties de KCN dans 100 parties d'eau, à une température comprise entre 35 et 45°C (réaction exothermique). Une fois l'addition terminée, le bain de refroidissement est retiré et le tout est agité pendant 20 heures à température ambiante. Le mélange réactionnel est versé dans 650 parties d'hydroxyde d'ammonium et 500 parties de glace pilée sont ajoutées. Le mélange est extrait avec du chloroforme. L'extrait organique est séché sur carbonate de potassium, filtré et évaporé. Le résidu (solide) est trituré dans de l'éther diisopropylique (DIPE). Après maintien à température ambiante, on obtient la 4-anilino-4-cyano-1-(2-phényléthyl)-pipéridine (I) ; mp 120-121°C.
A 4500 parties de H2SO4 conc. sont ajoutées par portions 710 parties de (I), tout en maintenant la température en dessous de 25°C. Une fois l'opération terminée, l'agitation est poursuivie pendant une nuit à température ambiante. Le mélange réactionnel est versé sur un mélange de 10.000 parties de glace pilée et 3600 parties d'hydroxyde d'ammonium. Le produit est extrait avec du chloroforme, l'extrait est séché, filtré et évaporé. Le résidu est agité dans 140 parties de DIPE, refroidi, le produit est filtré et séché, ce qui donne le 4-(phénylamino)-1-(2-phényléthyl)-4-pipéridinecarboxamide (II), mp 182,5°C.
Un mélange de 105 parties de (II), 53,7 parties de KOH et 275 parties d'éthylène glycol est agité et porté à reflux pendant 20 heures. Après refroidissement, le RM est versé sur 1000 parties d'eau et le tout est filtré. Le filtrat est fortement acidifié avec une solution de HCl jusqu'à ce que le précipité formé entre en solution. Ensuite, la solution est fortement alcalinisée avec une solution concomitante de NaOH (exotermic rxn) et filtrée à chaud. Il est filtré et recristallisé à partir d'eau, ce qui donne l'acide 4-(phénylamino)-1-(2-phényléthyl)-4-pipéridinecarboxylique, sel de sodium (III), mp >300°C (déc).
Une solution de 62,3 parties de (III) dans 340 parties de HMPA (triamide hexaméthylphosphorique, peut être remplacé par du DMSO) est agitée et chauffée à 100°C. Après refroidissement à 10°C, on ajoute goutte à goutte 28,4 parties d'iodométhane (réaction légèrement exothermique). Après achèvement, l'agitation est poursuivie pendant 24 heures à température ambiante. Le mélange réactionnel est ensuite versé sur de l'eau (800 parties) et le produit est extrait avec du toluène. L'extrait est lavé à l'eau, séché, filtré et évaporé. Le résidu huileux se solidifie après trituration dans le DIPA, donnant le 4-(phénylamino)- 1-(2-phénéthyl)-4-pipéridinecarboxylate de méthyle (IV), mp 94,9 C.
Un mélange de 33,8 parties de (IV) et de 100 parties d'anhydride propionique est agité et porté à reflux pendant 6,5 heures. Le mélange réactionnel est laissé refroidir pendant une nuit jusqu'à la température de référence tout en agitant et versé sur de l'eau glacée. Le produit est extrait avec du toluène, l'extrait est lavé avec de l'eau, séché, filtré et évaporé. Le résidu est converti en sel de citrate dans l'IPA et l'éther diéthylique. Le sel huileux est trituré dans un mélange d'IPA et d'éther, le produit solide est filtré et recristallisé deux fois, d'abord dans l'IPA, puis dans l'acétone, séché sous vide à 100 C, ce qui donne le citrate de carfentanil, mp 151-154°C. Pour le sel d'oxalate, la DE50 = 0,0006 mg/kg i/v, ce qui signifie que pour un corps de 100 kg, il ne faut que 0,06 mg.
Pour information, pour le 3-méthylfentanyl (ED50=0,00058 mg/kg i.v.), voir sa synthèse dans J. Med. Chem. vol 17, No. 10, p. 1047 (1974).
Une solution de 60,5 g (0,929 mole) de cyanure de potassium dans 181 ml d'eau a été ajoutée lentement à une solution agitée de 127 g (0,625 mole) de 1-(bêta-phénéthyl)-4-pipéridone et de 87,1 g (0,935 mole) d'aniline dans 635 ml d'acide acétique glacial à 25°-30°C. Après 45 heures d'agitation à température ambiante, le mélange réactionnel a été versé dans un mélange de 900 g de glace et de 1 610 ml d'hydroxyde d'ammonium concentré, sous agitation pendant deux heures, au cours desquelles un solide brun a précipité. Le solide a été filtré et lavé à l'eau. La recristallisation à partir d'isopropanol a donné un total de 125 g (66% de rendement) de produit, 1-(bêta-phénéthyl)- 4-((N-phénylamino)-4-pipéridine carbonitrile, sous forme de cristaux de couleur beige, p.m. 119°-120°C.
De l'acide formique (600 ml) a été ajouté à 600 ml d'anhydride acétique à une vitesse telle que la température du mélange ne dépasse pas 42°C. A cette solution ont été ajoutés 119 g (0,39 mole) de 1-(beta-phenethyl)- 4-(N-phenylamino)-4-piperidine carbonitrile à 5-10°C. sous agitation. Après avoir reposé à température ambiante pendant une nuit, le mélange réactionnel a été versé dans de l'eau glacée et alcalinisé jusqu'à un pH de 7,4 à l'aide d'une solution d'hydroxyde de sodium diluée, ce qui a entraîné la précipitation d'un solide beige. Le solide a été filtré et lavé à l'eau. La recristallisation à partir de méthanol a donné 100,4 g (rendement de 77,3 %) du produit 1-(bêta-phénéthyl)-4-(N-formyl- N-phénylamino)-pipéridine carbonitrile, sous forme de cristaux blancs, p.m. 136-138°C.
A une suspension de 100 g (0,30 mole) de 1-(bêta-phénéthyl)-4-(N-formyl-N-phénylamino)-carbonitrile de pipéridine dans 1,0 L de méthanol anhydre, on a ajouté lentement une solution de 670 g (18,4 mole) de chlorure d'hydrogène dans 2,0 L de méthanol anhydre à une température de 3 à 10°C. La solution jaune résultante a été portée à reflux pendant deux heures, puis le méthanol a été distillé jusqu'à ce que 1,7 L soit recueilli au cours des trois heures suivantes. Pendant ce temps, un solide blanc a précipité. Le mélange réactionnel a été refroidi et filtré, ce qui a permis d'obtenir 79 g (rendement de 64,2 %) de produit, le dihydrochlorure de méthyle 1-(bêta-phénéthyl)-4-(N-phénylamino)-4-pipéridineimidate, sous forme de solide blanc, p.m. 196-198°C (déc).
Une suspension de 79 g (0,19 mole) de dichlorhydrate de méthyle 1-(bêta-phénéthyl)-4-(N-phénylamino)-pipéridineimidate dans 675 ml d'eau a été alcalinisée jusqu'à un pH de 9 avec une solution diluée d'hydroxyde de sodium. Le solide a été filtré et lavé à l'eau. Le solide a été séché dans un dessiccateur sous vide pour donner 61,5 g (98,8 % de rendement) de produit, 1-(bêta-phénéthyl)-4-(phénylamino)-pipéridine carboxamide, sous forme de solide blanc, p.m. 181-183°.
Une solution de 28,4 g (0,088 mole) de 1-(bêta-phénéthyl)-4-(N-phénylamino)-4-pipéridine carboxamide et de 17 g d'hydroxyde de potassium dans 114 ml d'éthylène glycol a été portée à reflux pendant 3 heures. Le mélange réactionnel a été versé dans 228 ml d'eau glacée et rendu acide jusqu'à un pH de 6-6,5 avec de l'acide chlorhydrique concentré, ce qui a entraîné la précipitation d'un solide de couleur beige. Le solide a été filtré et lavé à l'eau froide. Le solide a été suspendu dans du benzène et l'eau a été éliminée par distillation azéotropique. Le mélange a été refroidi et filtré, ce qui a donné 28 g (98,3 % de rendement) de produit, l'acide 1-(bêta-phénéthyl)-(N-phénylamino)-pipéridinecarboxylique, sous la forme d'un solide blanc, p.m. 254-255°C (déc).
De l'acide sulfurique concentré (12 ml) a été ajouté lentement à une suspension agitée de 25,6 g (0,079 mole) d'acide 1-(bêta-phénéthyl)-4-(N-phénylamino)-4-pipéridine carboxylique dans 95 ml de méthanol anhydre. La solution résultante a été portée à reflux pendant 73 heures au total. Le mélange réactionnel a été refroidi et versé dans 1 L d'eau glacée, ce qui a entraîné la précipitation d'un solide brun gommeux. Le mélange a été rendu basique à un pH de 7,4 avec une solution diluée d'hydroxyde de sodium et extrait avec du chlorure de méthylène. Les extraits ont été séchés sur sulfate de magnésium et évaporés pour donner 21 g de produit brut qui a été recristallisé à partir de N-hexane pour donner 19,0 g (71,1% de rendement) du produit désiré, le 1-(bêta-phénéthyl)-4-(N-phénylamino)-4-pipéridine carboxylate de méthyle, sous forme de cristaux blancs, p.m. 92-93°C.
Un mélange de 10,0 g (0,03 mole) de 1-(bêta-phénéthyl)-(N-phénylamino)-pipéridine carboxylate de méthyle et de 100 g (0,77 mole) d'anhydride propionique a été chauffé à reflux pendant 6 heures. La majeure partie de l'anhydride propionique a ensuite été éliminée par distillation sous pression réduite. Le résidu a été mélangé à environ 100 ml d'eau glacée et alcalinisé jusqu'à un pH de 8 avec de l'hydroxyde d'ammonium. Le mélange a été extrait avec du chloroforme et les extraits ont été séchés sur du sulfate de magnésium et évaporés sous pression réduite. Le résidu, qui pesait environ 12 g, a été dissous dans 50 ml d'isopropanol et traité avec une solution de 3,8 g (0,03 mole) d'acide oxalique dissous dans 50 ml d'isopropanol. Le produit a été cristallisé pendant une nuit à température ambiante. Après filtration et séchage, on a obtenu 12,2 g (rendement de 85 %) d'oxalate de carfentanil, ou oxalate de méthyle 1-(bêta-phénéthyl)-(N- propionyl-N-phénylamino)-4-pipéridine carboxylate, p.m. 183-185°C.