- Joined
- Apr 10, 2022
- Messages
- 297
- Reaction score
- 161
- Points
- 43
Source : https://www.nature.com/articles/s41...rgM-fPwO6Nyexx4DSgugk0ki8Kdlc3KmylHUUO0jEpFro
Le microdosage implique l'auto-administration régulière de substances psychédéliques à des doses suffisamment faibles pour ne pas altérer le fonctionnement cognitif normal6. Les substances les plus couramment utilisées pour le microdosage sont les champignons psilocybine et le LSD et, dans une moindre mesure, d'autres substances psychédéliques telles que la mescaline et le 2-CB7. Les enquêtes sur le microdosage de psilocybine ont mis en évidence des pratiques diverses, mais convergent généralement vers l'auto-administration, 3 à 5 fois par semaine, de 0,1 à 0,3 g de champignons séchés7,8,9,10,11,12. Les améliorations de l'humeur, du bien-être émotionnel et de la cognition ont été signalées parmi les principales motivations pour le microdosage13, et plusieurs études transversales ont identifié des associations entre le microdosage et les améliorations perçues de l'humeur13,14,15,16,17 et du fonctionnement cognitif10,11,16, les réductions du stress7, de la dépression7,9,16 et de l'anxiété7,9,14,18.
Relativement peu d'études prospectives ont évalué le microdosage. La première étude longitudinale sur le microdosage a analysé les évaluations quotidiennes de 98 microdoseurs pendant 6 semaines et a constaté des améliorations transitoires aiguës dans de vastes domaines du fonctionnement psychologique les jours de microdosage, ainsi que des réductions du stress, de la dépression et de la distractibilité entre le début et la fin de l'étude. En outre, bien que les conclusions de cette étude soient limitées par l'absence d'un groupe de contrôle ne pratiquant pas le microdosage, des examens complémentaires ont conclu que les effets observés ne correspondaient pas à ce que l'on pouvait attendre sur la base des attentes courantes liées au microdosage7. Une étude prospective ultérieure, qui a suivi 81 microdoseurs pendant quatre semaines, a également fait état d'améliorations dans plusieurs domaines du bien-être psychologique, notamment une meilleure stabilité émotionnelle et une diminution de l'anxiété et de la dépression. Cependant, des analyses complémentaires ont suggéré que ces effets positifs pouvaient être attribués aux attentes et ont souligné la nécessité de poursuivre les recherches avec des participants témoins non microdosés afin de mieux distinguer les effets du microdosage des effets placebo et d'autres facteurs de confusion longitudinaux18.
L'utilisation efficace du placebo a représenté un défi dans les quelques études publiées qui ont tenté une telle conception dans le contexte du microdosage psychédélique17,19,20. Plus précisément, une étude prospective du microdosage qui a utilisé une intervention en auto-aveugle pour approximer le contrôle du placebo parmi 191 participants pendant 4 semaines a identifié des améliorations du bien-être émotionnel parmi les microdoseurs, mais a noté que l'identification correcte de la condition a été rapportée par 72% des participants, ce qui complique la capacité à estimer de manière concluante l'influence des effets du placebo sur les changements observés. De même, une étude croisée en double aveugle contre placebo portant sur 30 personnes suivies pendant huit semaines a mis en évidence des niveaux plus élevés d'émerveillement autodéclaré en réponse à des expériences esthétiques chez les microdosseurs par rapport aux témoins. Néanmoins, les auteurs ont reconnu les effets confondants potentiels de la rupture de l'aveugle, puisque deux tiers des participants ont deviné avec précision leur condition19. Une analyse plus poussée du même groupe de participants n'a pas permis d'identifier de différences dans les symptômes d'anxiété et de dépression chez les microdoseurs par rapport aux placebos20. Cependant, l'étude a noté que l'expérience antérieure des participants avec les psychédéliques, en plus de faibles niveaux de dépression et d'anxiété, peut avoir atténué les effets du microdosage. En outre, une proportion significative de participants ont correctement deviné leur état dans la moitié des blocs d'essai, mais les effets nuls apparents dans l'étude peuvent rendre l'influence potentielle du placebo moins pertinente.
La rupture de l'aveugle et la catégorie plus large des effets d'attente ou de placebo sont des défis identifiés pour l'interprétation des études sur les doses régulières de psychédéliques21, et peuvent également compliquer l'interprétation de la recherche sur le microdosage. Par exemple, l'étude longitudinale qui a tenté d'ajuster les attentes en contrôlant les scores sur une mesure modifiée des attentes de microdosage18 a noté que plus de 80% des participants ont déclaré avoir déjà utilisé des psychédéliques, ce qui rend probable que les scores sur la mesure des attentes ont été influencés par des expériences antérieures d'effets directs de la drogue. Les différences individuelles dans la réponse aux médicaments dues au métabolisme et à de nombreux autres facteurs font que les effets pharmacologiques antérieurs des médicaments sont susceptibles d'être fortement corrélés avec les effets pharmacologiques directs ultérieurs et, en tant que tels, la partialisation (c'est-à-dire le contrôle) des attentes peut sous-estimer les effets pharamacologiques directs22,23. En résumé, les études longitudinales existantes ont observé des effets positifs associés au microdosage, mais n'ont pas été en mesure d'estimer avec confiance les contributions pharmacologiques directes à ces effets. De manière plus générale, l'analyse des effets directs des psychédéliques à partir de facteurs indirects tels que le contexte, les différences individuelles et les attentes présente des défis épistémologiques et pratiques, et l'étude des psychédéliques pourrait être mieux servie en allant au-delà de l'accent potentiellement Procruste sur l'aveuglement et d'autres approches visant à maximiser le contrôle24. Par exemple, l'examen naturaliste de grandes cohortes offre de puissantes opportunités d'examiner la cohérence des effets à travers les sous-groupes, et l'utilisation d'un groupe de comparaison sans la prémisse de l'aveuglement, mais avec des caractéristiques démographiques similaires et des niveaux à peu près équivalents d'activités liées à l'étude, permet l'évaluation de l'impact du microdosage comme distinct des effets indirects tels que l'engagement dans l'étude, les effets de la pratique, la régression à la moyenne, et d'autres artefacts potentiels communs à la recherche prospective.
Parallèlement à l'intérêt accru pour le microdosage de champignons contenant de la psilocybine, on observe une accélération de l'intérêt pour d'autres champignons supposés thérapeutiques. En particulier, la crinière de lion (Hericium erinaceus ; HE) a suscité un intérêt considérable pour le traitement proposé de la dépression25 et des troubles cognitifs légers26, ainsi que pour les preuves précliniques de la facilitation de la neurogenèse, avec des implications pour le traitement des troubles neurodégénératifs27,28. Des preuves récentes suggèrent que certains microdoseurs combinent la psilocybine avec l'HE dans un processus appelé "stacking "8. Une étude transversale portant sur plus de 4 000 microdoseurs, dont l'échantillon recoupe en partie celui de la présente étude, a révélé que plus de 50 % des microdoseurs de psilocybine combinaient la psilocybine avec diverses substances, et que l'HE était l'ajout le plus courant, suivi d'une combinaison de niacine (vitamine B3) et d'HE8. Comme il s'agit de la seule étude portant sur l'empilage, on ne sait pas si ces résultats peuvent être généralisés. La combinaison d'HE, de B3 et de psilocybine a été popularisée dans les réseaux informels d'information sur le microdosage, sur la base de l'hypothèse selon laquelle la B3 pourrait faciliter la biodisponibilité de la psilocybine et de l'HE par le biais de la vasodilatation29. Il a été proposé que les effets salutaires de la psilocybine et de l'HE passent par des processus liés au BDNF, ce qui soulève la possibilité d'effets super-additifs30,31. Cependant, les effets potentiels de la psilocybine et de l'HE - avec ou sans B3 - n'ont pas encore été formellement étudiés, et la popularité de l'empilage découle probablement de l'auto-expérimentation et de rapports anecdotiques.
En résumé, malgré des résultats suggestifs et un intérêt croissant de la part du public, la littérature empirique reste équivoque sur les conséquences du microdosage. Des recherches supplémentaires avec des groupes de contrôle et des échantillons de grande taille permettant d'examiner les modérateurs potentiels tels que l'état de santé mentale, l'âge et le sexe sont nécessaires pour mieux apprécier les conséquences de ce phénomène émergent sur la santé. Dans la présente étude, nous visons à étendre cette littérature en examinant les changements prospectifs associés au microdosage de psilocybine par rapport à un groupe de contrôle non microdosé dans les domaines de la santé mentale, de l'humeur et du fonctionnement cognitif et psychomoteur. À notre connaissance, il s'agit de la plus grande étude prospective à ce jour sur le microdosage de psilocybine, la première à faire la distinction entre les mélanges de microdosage (c'est-à-dire l'empilage), et parmi les rares études prospectives à désagréger systématiquement les analyses en fonction de l'âge et des préoccupations en matière de santé mentale.
Tableau 1 Caractéristiques des participants.
Tableau complet
L'étude consistait en une évaluation de base réalisée au début de l'étude et en une évaluation de suivi réalisée 22 à 35 jours plus tard ; les calendriers d'évaluation étaient équivalents pour les microdoseurs et les non-microdoseurs. Les évaluations portaient sur les pratiques psychédéliques du mois précédent, l'humeur et la santé mentale, et présentaient des tâches testant le traitement cognitif et psychomoteur. Chaque évaluation a duré de 20 à 30 minutes, avec une variabilité due à l'embranchement, de sorte que de nombreux éléments n'ont été présentés qu'à un sous-ensemble de participants. Le consentement éclairé de tous les participants a été obtenu, l'étude a été approuvée par le comité d'éthique de la recherche de l'université de Colombie-Britannique (H19-03051) et toutes les méthodes ont été appliquées conformément à ses directives et règlements. Les hypothèses et les résultats n'ont pas été enregistrés au préalable.
Les données descriptives figurent dans le tableau 1. L'âge a été évalué de manière catégorique et dichotomisé en 55 ans et plus et moins de 55 ans pour évaluer les différences potentielles entre les groupes tout en tenant compte de la taille des groupes pour maintenir la puissance statistique. La présence de problèmes de santé mentale a été évaluée à l'aide de la question suivante : "Avez-vous actuellement des problèmes psychologiques, de santé mentale ou de toxicomanie? L'humeur a été évaluée à l'aide du Positive And Negative Affect Schedule (PANAS)33, une mesure d'auto-évaluation de 20 items avec des sous-échelles de 10 items qui évaluent l'affect positif et négatif. En raison d'une erreur technique, un élément de la sous-échelle négative a été exclu ; pour remédier à ce problème, les scores ont été convertis en pourcentages. La dépression, l'anxiété et le stress ont été mesurés à l'aide de l'échelle DASS-21 (Depression Anxiety Stress Scale-21)34, qui comporte trois sous-échelles de 7 items notés sur une échelle de 4 points. Les tâches cognitives et psychomotrices ont été adaptées de l'Apple Research Kit, qui a été utilisé et validé dans plusieurs grandes études35,36. La capacité psychomotrice a été mesurée à l'aide d'une version adaptée de la tâche de tapotement du doigt37, dans laquelle les participants tapotaient deux cercles adjacents sur l'écran d'un appareil iOS en alternance pendant 10 s à l'aide de l'index et du majeur de leur main dominante. Des protocoles similaires de tapotement des doigts sur smartphone ont démontré une bonne validité prédictive et discriminante pour les troubles neurodégénératifs37,38. L'empan de mémoire spatiale a été évalué à l'aide d'une version adaptée de la tâche de Corsi Block-Tapping39, dans laquelle les participants se souviennent de l'emplacement des stimuli sur une grille carrée au cours d'une série limitée dans le temps de tours de difficulté croissante40,41. Le critère utilisé dans cette étude était le nombre de réponses correctes. La vitesse de traitement a été évaluée à l'aide d'un test adapté, le Paced Auditory Serial Addition Test (PASAT)42,43, qui consiste à additionner de manière itérative des nombres entiers alternés ; le critère était le nombre total de réponses correctes.
Les modèles ont été construits de telle sorte que les variables ont été retenues si elles prédisaient le résultat du modèle ou si elles étaient un élément constitutif d'une interaction significative de niveau supérieur. Pour les résultats pour lesquels une interaction Microdose*Temps a été identifiée, des modèles factoriels complets ont été construits, incluant l'interaction à trois voies Microdose*Temps*Genre, et soit Microdose*Temps*Age, soit Microdose*Temps*Préoccupations de santé mentale, ainsi que tous les effets principaux de niveau inférieur et les effets d'interaction à deux voies. Les analyses supplémentaires ont éliminé les réponses aberrantes qui s'écartaient de plus de deux écarts-types de la moyenne de leur groupe respectif. Une deuxième série d'analyses supplémentaires a exclu les participants ayant déclaré un microdosage avant le début de l'étude afin de contrôler les effets de report potentiels associés aux antécédents de microdosage. Plus précisément, les participants ayant déclaré une pratique active du microdosage lors de l'évaluation de référence ont été retirés ; nous avons donc comparé les microdoseurs qui ont commencé leur pratique après l'évaluation de référence et l'évaluation de suivi à ceux qui n'ont pas pratiqué de microdosage au cours de cette période. Pour évaluer l'empilement, nous avons suivi ces analyses avec jusqu'à trois séries d'analyses supplémentaires dans le groupe des microdoseurs. Ces analyses supplémentaires ont été limitées aux résultats qui ont mis en évidence un effet Microdose*Temps afin d'éviter l'inflation de l'erreur de type I due aux tests multiples. Dans la première de ces analyses, lesmicrodoseurs Psilocybine+HE ont été comparés aux microdoseurs Psilocybine seule. Une deuxième série d'analyses a comparé lesmicrodoseurs de Psilocybine+HE+B3 aux microdoseurs de Psilocybine seule. Comme dans les analyses primaires, nous avons également examiné les effets modérateurs de l'âge ou des problèmes de santé mentale. Dans les cas où l'une ou l'autre de ces deux analyses complémentaires a révélé des effets d'interaction significatifs à deux ou trois voies, elles ont été suivies d'une dernière analyse complémentaire comparant lesmicrodoseurs de Psilocybine+HE à ceux de Psilocybine+HE+B3. Les analyses du chi-carré ont évalué l'équivalence des sous-groupes en fonction de l'âge, du nombre de jours de microdose au cours du mois écoulé et de la dose de microdose ; les différences dans ces facteurs ont été contrôlées en éliminant au hasard des participants du sous-groupe qui était disproportionné jusqu'à ce que les proportions des groupes soient considérées comme statistiquement équivalentes45. Le d de Cohen a été calculé pour les effets afin de faciliter l'interprétation et de permettre la comparaison des tailles d'effet entre les groupes et avec les recherches antérieures (tableau 2).
Tableau 2 Microdoseurs et non-microdoseurs sur une période d'un mois.
Tableau complet
Les analyses préliminaires ont permis d'identifier les différences attendues en fonction de l'âge; le groupe des moins de 55 ans a affiché des performances supérieures à celles du groupe des 55 ans et plus dans toutes les tâches cognitives ; pour le test de tapotement (moyenne = 70,48 (33,18) contre 52,60 (29.99) ; t (1, 863) = 5.05, p< 0.01) ; pour le PASAT (moyenne = 33.67(14.21) contre 30.37 (12.92) t (1, 772) = 2.08, p< 0.05) et l'espacement (moyenne = 236.25 (51.02) contre 176.88 (58.80) ; t (1, 943) = 11.00, p< 0.01). Les différences de base en fonction de l'âge ont été identifiées pour l'humeur négative (moyenne = 46,89 (16,13) contre 40,64 (16,06) ; t (1, 1048) = 3,96, p< 0,01) mais pas pour l'humeur positive (moyenne = 55% (16) contre 55,03% (15,01) ; t (1, 1048) = - 0,018, p= 0,99). Comme on pouvait s'y attendre, les participants qui ont fait état de problèmes de santé mentale ont obtenu des scores plus élevés sur les trois sous-échelles du DASS : Dépression (moyenne = 10,44 (9,72) contre 18,92 (12) ; t (1, 1010) = - 11,81, p< 0,01) ; Anxiété (moyenne = 6,38 (6,36) contre 11.38 (8,74) ; t (1, 1010) = 10,09, p< 0,01) et Stress (moyenne = 13,84 (9,1) contre 20,04 (9,8) ; t (1, 1010) = 9,61, p< 0,01). L'analyse par sexe n'a révélé aucun effet principal du sexe au fil du temps dans aucun des domaines de la DASS (tous les F < 1,6, p> 0,20).
Figure 1
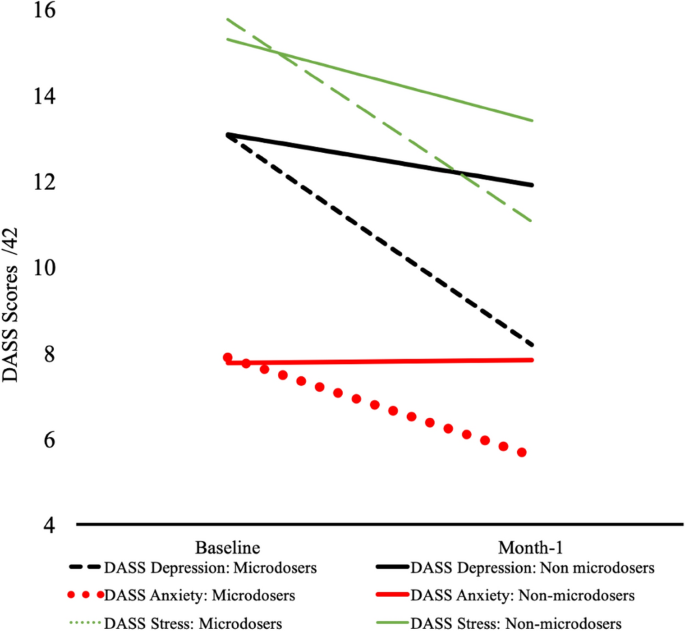
Microdosage et santé mentale. Les valeurs de "base" reflètent les réponses moyennes des participants recueillies entre 0 et 7 jours après le début de l'étude. Les valeurs du "mois 1" reflètent les réponses moyennes des participants recueillies entre 22 et 35 jours après le début de l'étude.
Agrandir l'image
Les interactions entre les groupes " santé mentale" et "microdose " n'étaient significatives pour aucun des domaines(tous les FsMicrodose*Santé mentale*Temps < 1,16 ; p> 0,10), ce qui indique que les effets principaux du microdosage étaient cohérents entre les personnes interrogées présentant ou non des troubles de la santé mentale. Parmi les microdoseurs ayant des problèmes de santé mentale , les scores de dépression sont passés de 18,85 (12,03) à l'inclusion à 11,73 (9,85) au mois 1 ; pour l'anxiété, de 11,04 (8,48) à l'inclusion à 7,46 (6,68) au mois 1 ; et pour le stress, de 19,93 (9,71) à l'inclusion à 13,91 (9,02) au mois 1. Parmi les répondants sans antécédents de problèmes de santé mentale, les scores de dépression sont passés de 10,40 (9,78) au départ à 6,65 (7,60) au mois 1 ; pour l'anxiété, de 6,53 (6,50) au départ à 4,81 (5,57) au mois 1 ; et pour le stress, de 13,96 (9,12) au départ à 9,78 (7,50) au mois 1. Des analyses supplémentaires ont comparé les conditions d'empilage sur les changements dans les scores de dépression, d'anxiété et de stress du DASS de la ligne de base au mois 1. Aucune différence entre les microdoseurs Psilocybine seule et lesmicrodoseurs Psilocybine+HE (tous F < 0,70 ; p> 0,10) n'a été notée. De même, aucune différence entre les microdoseurs de psilocybine seule et lesmicrodoseurs de psilocybine+HE+B3 n'a été identifiée (tous F < 0,77 ; p> 0,10).
L'interaction entre l'âge, l'état de la microdose et le temps n'était pas significative pour l'humeur positive(F (1, 1058) = 0,21, b= - 0,05, p= 0,65) ou l'humeur négative(F (1, 1059) = 1,38, b= 0,13 p= 0,24), ce qui indique l'équivalence des effets sur l'humeur en fonction de l'âge. Les analyses de suivi n'ont pas identifié de différences significatives dans les changements de l'humeur positive ou négative au fil du temps entre les microdoseurs Psilocybine seule et lesmicrodoseurs Psilocybine+HE (tous F < 0,52, p> 0,47) ou lesmicrodoseurs Psilocybine+HE+B3 (tous F < 2,44, p> 0,12).
Les analyses de l'empilement entre les microdoseurs (Fig. 2) n'ont révélé aucune interaction entre Psilocybine seule et psilocybine+HE*Temps, ce qui suggère que l'ajout de HE n'a pas eu d'impact sur l'effet de la psilocybine sur le tapotement des doigts (F (1, 524) = 0,284, b= 0,12, p= 0,67). En revanche, l'interaction Psilocybine seule vs psilocybine+HE+B3*Temps a indiqué une amélioration relativement plus importante des scores de tapotement avec l'ajout de HE et de B3 à la psilocybine (F (1, 732) = 3,93, b= - 0,51, p< 0,05). Ce résultat a été suivi par l'examen de l'effet modérateur de l'âge, qui a identifié une interaction Psilocybine seule vs psilocybine+HE+B3 * Temps *Age (F (1, 732) = 8,4, b= 0,6, p= 0,04), ce qui reflète que l'ajout de HE et de B3 a eu un impact chez les répondants plus âgés, mais pas chez les plus jeunes. Les analyses supplémentaires de Psilocybine+HE vs psilocybine+HE+B3 * Temps ont révélé une tendance à la signification (F (1, 427) = 3,26, b= - 0,56, p= 0,07), et l'interaction tripartite Psilocybine+HE vs psilocybine+HE+B3 *Temps*Age a été identifiée (F (1, 427) = 6,71, b= 0,66, p= 0,01), ce qui indique que les effets étaient plus prononcés chez les répondants plus âgés. Des analyses complémentaires de suivi ont indiqué que ces résultats étaient robustes après avoir contrôlé les différences entre les sous-groupes en termes d'âge, de fréquence des microdoses et de dosage des microdoses (toutes les interactions à trois voies Fs > 6,20, p< 0,05).
Figure 2
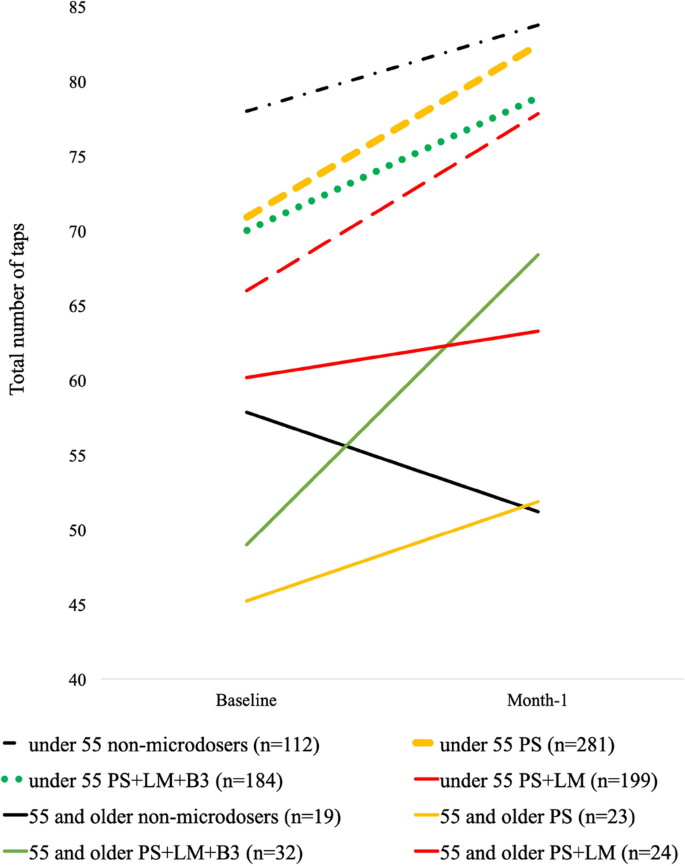
Microdosage et scores au test du doigt. Les valeurs "de base" reflètent les réponses moyennes des participants recueillies entre 0 et 7 jours après le début de l'étude. Les valeurs du "mois 1" reflètent les réponses moyennes des participants recueillies entre 22 et 35 jours après le début de l'étude. PS fait référence aux participants qui ont reçu une microdose de psilocybine en l'absence de Lion's Mane (HE). PS + HE se réfère aux participants qui ont microdosé la psilocybine et l'HE en l'absence de niacine (B3). PS + HE + B3 microdoseurs se réfère aux participants qui microdosent la psilocybine avec HE et B3. Les différences dans les pentes des conditions de groupe ont fait l'objet d'analyses d'interaction Microdose*Temps.
Agrandir l'image
Les comparaisons entre les microdoseurs et les non-microdoseurs en ce qui concerne le changement entre la ligne de base et le mois 1 n'ont indiqué aucune différence pour la tâche d'empan spatial (F (1, 944) = 0,24, b= - 0,07, p= 0,63) ou le PASAT (F (1, 775) = 0,21, b= 0,02, p= 0,65). Compte tenu de cette absence d'effets principaux, aucune analyse de suivi n'a été effectuée.
Une contribution potentielle de la recherche future avec des modèles contrôlés par placebo serait la capacité de désagréger les contributions des attentes positives et des effets placebo. Bien que notre utilisation d'un groupe de non-microdoseurs qui était équivalent aux microdoseurs en ce qui concerne les données démographiques et l'engagement dans les procédures de l'étude soit une force évidente, les microdoseurs et les non-microdoseurs de notre étude étaient conscients de leur statut dès le début de l'étude, ce qui rend impossible d'exclure les contributions d'attentes plus importantes dans le groupe de microdoseurs par rapport au groupe de non-microdoseurs. Toutefois, compte tenu des difficultés associées à la réalisation d'essais contrôlés randomisés dans l'environnement réglementaire restrictif actuel et des difficultés plus générales liées à l'aveuglement efficace d'un médicament de recherche ayant des effets psychoactifs bien connus et distinctifs, nous encourageons la recherche à adopter une perspective élargie sur les effets putatifs des placebos24. Plus précisément, le réexamen clinique et l'étude des psychédéliques offrent l'occasion de réévaluer la mesure dans laquelle les attentes et les effets psychoactifs francs peuvent se combiner pour influencer le bien-être subjectif de manière potentiellement significative19.
L'impact du microdosage sur les tests de fonctionnement cognitif et psychomoteur était mitigé et limité aux performances psychomotrices, sans impact apparent sur la mémoire spatiale ou la vitesse de traitement. En outre, l'ampleur de ces effets semblait dépendre de l'âge et de la combinaison de psilocybine avec HE et B3. Cette spécificité pour les performances psychomotrices et la dépendance à la combinaison des composants justifient une interprétation prudente, car la littérature sur le microdosage et les performances cognitives est peu abondante18 et aucune étude antérieure ne s'est concentrée sur la combinaison de la psilocybine avec d'autres substances supposées actives. En effet, bien que notre large échantillon ait permis un nouveau niveau de granularité dans notre examen des pratiques distinctes parmi les sous-groupes de microdoseurs liés à l'âge, ces groupes étaient néanmoins relativement petits, ce qui augmente la possibilité que nos résultats de facilitation des tests de tap chez les personnes de plus de 55 ans qui microdosent la combinaison de psilocybine, HE et B3 puissent être anormaux. En outre, en raison du petit nombre de participants prenant du B3 sans psilocybine ni HE, nous n'avons pas eu la puissance nécessaire pour étudier dans quelle mesure ces résultats étaient dus à la combinaison de psilocybine, B3 et HE, par opposition au B3 seul. De plus, l'âge a été collecté de manière catégorique et l'âge limite de 55 ans a été choisi par commodité en fonction de la puissance, ce qui nous empêche de déterminer dans quelle mesure les effets observés seraient maintenus si d'autres seuils d'âge étaient utilisés. Nous ne sommes donc pas en mesure de déterminer dans quelle mesure les effets observés se maintiendraient si l'on utilisait d'autres seuils pour l'âge. Néanmoins, si ces résultats s'avèrent robustes dans divers échantillons et chez divers chercheurs, ils pourraient représenter une première étape importante dans le développement de nouveaux traitements pour les troubles neurologiques répandus et réfractaires. Enfin, bien que ces résultats puissent être décrits comme suggestifs, ils ajoutent néanmoins une crédibilité préliminaire aux rapports anecdotiques sur les bienfaits de la combinaison spécifique de psilocybine, d'HE et de B330.
En plus des petits échantillons dans les sous-groupes, de la conception observationnelle et d'une approche généralement exploratoire, l'interprétation est également limitée par un biais de réponse potentiel lié à l'autosélection des participants et au recrutement dans des lieux favorables à l'utilisation de psychédéliques, ce qui peut avoir entraîné une surreprésentation dans notre échantillon des personnes qui réagissent favorablement au microdosage. De plus, l'indisponibilité d'une version Android OS de l'application au moment de l'étude a limité la participation aux personnes ayant accès à des appareils Apple. Cette étude n'a pas non plus examiné l'influence de la dose et des pratiques de dosage sur les résultats. De futures études avec des conceptions permettant une évaluation minutieuse de la puissance, de la composition et de la quantité des matériaux microdosés seront nécessaires pour affiner notre compréhension de l'influence de ces facteurs clés. De même, les effets indésirables et les interactions avec les antidépresseurs et les anxiolytiques habituels n'ont pas été évalués ; ces données seront nécessaires pour mieux comprendre la sécurité et l'acceptabilité du microdosage. À la lumière de ces limites, nous encourageons les recherches futures qui utilisent une approche de recrutement plus systématique et des modèles qui évaluent le dosage optimal, les meilleures pratiques et les effets indésirables associés au microdosage psychédélique.
Joseph Rootman a reçu des fonds de recherche de Quantified Citizen Technologies, une société qui produit des logiciels pour la recherche mobile décentralisée et qui a fourni la plateforme de collecte de données pour cette étude. Maggie Kiraga est une employée de Quantified Citizen. Kalin Harvey est cofondateur et directeur technique de Quantified Citizen, cofondateur du Psychedelic Data Project, cofondateur et directeur de la Ketamine Assisted Therapy Association of Canada, et il est également investisseur dans MycoMedica Life Sciences. Pamela Kryskow est membre du comité consultatif clinique de Numinus Wellness, une société qui propose des services de psychothérapie psychédélique. Pamela Kryskow est rémunérée pour ce rôle par des actions de Numinus. Elle est consultante bénévole pour Nectara. Elle est cofondatrice de MycoMedica Life Sciences et fait partie du conseil consultatif scientifique et médical. Paul Stamets est un investisseur dans Quantified Citizen, MycoMedica Life Sciences, PBC et possède Fungi Perfecti, LLC qui vend des suppléments Lion Mane. Il est demandeur de brevets en instance combinant les champignons à psilocybine, les champignons Lions Mane et la niacine. Eesmyal Santos-Brault est cofondateur et PDG de Quantified Citizen, cofondateur du Psychedelic Data Project et investisseur dans MycoMedica Life Sciences. Kim PC Kuypers est chercheur principal dans des projets de recherche, dont la présente étude ne fait pas partie, qui sont sponsorisés par Mindmed et Silopharma, des entreprises qui développent des médicaments psychédéliques, et elle est membre rémunéré du conseil scientifique de Clerkenwell Health. Zach Walsh est en relation de conseil rémunéré avec Numinus Wellness et Entheotech BioMedical en ce qui concerne le développement médical des psychédéliques, et il est membre du conseil consultatif de la Multidisciplinary Association for Psychedelic Studies (MAPS) Canada et de MycoMedica Life Sciences.
Résumé
Le microdosage de psilocybine implique l'auto-administration répétée de champignons contenant de la psilocybine à des doses suffisamment faibles pour ne pas avoir d'impact sur le fonctionnement normal. Les pratiques de microdosage sont diverses et incluent la combinaison de psilocybine avec des substances telles que les champignons à crinière de lion (Hericium erinaceus ; HE) et la niacine (vitamine B3). L'engouement du public pour le microdosage a été plus rapide que les preuves, ce qui nécessite de nouvelles recherches prospectives. En utilisant un modèle d'observation naturaliste, nous avons suivi des microdoseurs de psilocybine(n= 953) et des comparateurs non microdoseurs(n= 180) pendant environ 30 jours et avons identifié des améliorations petites à moyennes de l'humeur et de la santé mentale qui étaient généralement cohérentes en fonction du sexe, de l'âge et de la présence de problèmes de santé mentale, ainsi que des améliorations de la performance psychomotrice qui étaient spécifiques aux adultes plus âgés. Des analyses supplémentaires ont indiqué que la combinaison de la psilocybine avec HE et B3 n'a pas eu d'impact sur les changements de l'humeur et de la santé mentale. Cependant, chez les microdoseurs plus âgés, la combinaison de psilocybine, HE et B3 a été associée à des améliorations psychomotrices par rapport à la psilocybine seule et à la psilocybine et HE. Nos résultats concernant les améliorations de l'humeur et de la santé mentale associées au microdosage de psilocybine complètent les études précédentes sur le microdosage psychédélique en utilisant un groupe de comparaison et en examinant la cohérence des effets en fonction de l'âge, du sexe et de la santé mentale. Les résultats concernant la combinaison de psilocybine, HE et B3 sont nouveaux et soulignent le besoin de recherches supplémentaires pour confirmer et élucider ces effets apparents.Introduction
L'utilisation de champignons contenant de la psilocybine pour améliorer la santé et le bien-être a une longue histoire dans diverses cultures1. Après des siècles de répression coloniale agressive, dont la manifestation la plus récente est la "guerre contre la drogue" menée par les États-Unis, la psilocybine est réapparue en dehors de ses contextes indigènes traditionnels, en tant qu'agent thérapeutique pour traiter les maladies mentales et améliorer le bien-être. En effet, les discussions sur les propriétés médicinales des champignons à psilocybine ont proliféré dans la culture nord-américaine et européenne au cours des dernières années2,3. Cet intérêt s'est surtout concentré sur les doses suffisantes pour provoquer des altérations spectaculaires de la conscience ; cependant, l'utilisation de "microdoses" plus petites est également devenue un sujet d'intérêt public et scientifique important4,5.Le microdosage implique l'auto-administration régulière de substances psychédéliques à des doses suffisamment faibles pour ne pas altérer le fonctionnement cognitif normal6. Les substances les plus couramment utilisées pour le microdosage sont les champignons psilocybine et le LSD et, dans une moindre mesure, d'autres substances psychédéliques telles que la mescaline et le 2-CB7. Les enquêtes sur le microdosage de psilocybine ont mis en évidence des pratiques diverses, mais convergent généralement vers l'auto-administration, 3 à 5 fois par semaine, de 0,1 à 0,3 g de champignons séchés7,8,9,10,11,12. Les améliorations de l'humeur, du bien-être émotionnel et de la cognition ont été signalées parmi les principales motivations pour le microdosage13, et plusieurs études transversales ont identifié des associations entre le microdosage et les améliorations perçues de l'humeur13,14,15,16,17 et du fonctionnement cognitif10,11,16, les réductions du stress7, de la dépression7,9,16 et de l'anxiété7,9,14,18.
Relativement peu d'études prospectives ont évalué le microdosage. La première étude longitudinale sur le microdosage a analysé les évaluations quotidiennes de 98 microdoseurs pendant 6 semaines et a constaté des améliorations transitoires aiguës dans de vastes domaines du fonctionnement psychologique les jours de microdosage, ainsi que des réductions du stress, de la dépression et de la distractibilité entre le début et la fin de l'étude. En outre, bien que les conclusions de cette étude soient limitées par l'absence d'un groupe de contrôle ne pratiquant pas le microdosage, des examens complémentaires ont conclu que les effets observés ne correspondaient pas à ce que l'on pouvait attendre sur la base des attentes courantes liées au microdosage7. Une étude prospective ultérieure, qui a suivi 81 microdoseurs pendant quatre semaines, a également fait état d'améliorations dans plusieurs domaines du bien-être psychologique, notamment une meilleure stabilité émotionnelle et une diminution de l'anxiété et de la dépression. Cependant, des analyses complémentaires ont suggéré que ces effets positifs pouvaient être attribués aux attentes et ont souligné la nécessité de poursuivre les recherches avec des participants témoins non microdosés afin de mieux distinguer les effets du microdosage des effets placebo et d'autres facteurs de confusion longitudinaux18.
L'utilisation efficace du placebo a représenté un défi dans les quelques études publiées qui ont tenté une telle conception dans le contexte du microdosage psychédélique17,19,20. Plus précisément, une étude prospective du microdosage qui a utilisé une intervention en auto-aveugle pour approximer le contrôle du placebo parmi 191 participants pendant 4 semaines a identifié des améliorations du bien-être émotionnel parmi les microdoseurs, mais a noté que l'identification correcte de la condition a été rapportée par 72% des participants, ce qui complique la capacité à estimer de manière concluante l'influence des effets du placebo sur les changements observés. De même, une étude croisée en double aveugle contre placebo portant sur 30 personnes suivies pendant huit semaines a mis en évidence des niveaux plus élevés d'émerveillement autodéclaré en réponse à des expériences esthétiques chez les microdosseurs par rapport aux témoins. Néanmoins, les auteurs ont reconnu les effets confondants potentiels de la rupture de l'aveugle, puisque deux tiers des participants ont deviné avec précision leur condition19. Une analyse plus poussée du même groupe de participants n'a pas permis d'identifier de différences dans les symptômes d'anxiété et de dépression chez les microdoseurs par rapport aux placebos20. Cependant, l'étude a noté que l'expérience antérieure des participants avec les psychédéliques, en plus de faibles niveaux de dépression et d'anxiété, peut avoir atténué les effets du microdosage. En outre, une proportion significative de participants ont correctement deviné leur état dans la moitié des blocs d'essai, mais les effets nuls apparents dans l'étude peuvent rendre l'influence potentielle du placebo moins pertinente.
La rupture de l'aveugle et la catégorie plus large des effets d'attente ou de placebo sont des défis identifiés pour l'interprétation des études sur les doses régulières de psychédéliques21, et peuvent également compliquer l'interprétation de la recherche sur le microdosage. Par exemple, l'étude longitudinale qui a tenté d'ajuster les attentes en contrôlant les scores sur une mesure modifiée des attentes de microdosage18 a noté que plus de 80% des participants ont déclaré avoir déjà utilisé des psychédéliques, ce qui rend probable que les scores sur la mesure des attentes ont été influencés par des expériences antérieures d'effets directs de la drogue. Les différences individuelles dans la réponse aux médicaments dues au métabolisme et à de nombreux autres facteurs font que les effets pharmacologiques antérieurs des médicaments sont susceptibles d'être fortement corrélés avec les effets pharmacologiques directs ultérieurs et, en tant que tels, la partialisation (c'est-à-dire le contrôle) des attentes peut sous-estimer les effets pharamacologiques directs22,23. En résumé, les études longitudinales existantes ont observé des effets positifs associés au microdosage, mais n'ont pas été en mesure d'estimer avec confiance les contributions pharmacologiques directes à ces effets. De manière plus générale, l'analyse des effets directs des psychédéliques à partir de facteurs indirects tels que le contexte, les différences individuelles et les attentes présente des défis épistémologiques et pratiques, et l'étude des psychédéliques pourrait être mieux servie en allant au-delà de l'accent potentiellement Procruste sur l'aveuglement et d'autres approches visant à maximiser le contrôle24. Par exemple, l'examen naturaliste de grandes cohortes offre de puissantes opportunités d'examiner la cohérence des effets à travers les sous-groupes, et l'utilisation d'un groupe de comparaison sans la prémisse de l'aveuglement, mais avec des caractéristiques démographiques similaires et des niveaux à peu près équivalents d'activités liées à l'étude, permet l'évaluation de l'impact du microdosage comme distinct des effets indirects tels que l'engagement dans l'étude, les effets de la pratique, la régression à la moyenne, et d'autres artefacts potentiels communs à la recherche prospective.
Parallèlement à l'intérêt accru pour le microdosage de champignons contenant de la psilocybine, on observe une accélération de l'intérêt pour d'autres champignons supposés thérapeutiques. En particulier, la crinière de lion (Hericium erinaceus ; HE) a suscité un intérêt considérable pour le traitement proposé de la dépression25 et des troubles cognitifs légers26, ainsi que pour les preuves précliniques de la facilitation de la neurogenèse, avec des implications pour le traitement des troubles neurodégénératifs27,28. Des preuves récentes suggèrent que certains microdoseurs combinent la psilocybine avec l'HE dans un processus appelé "stacking "8. Une étude transversale portant sur plus de 4 000 microdoseurs, dont l'échantillon recoupe en partie celui de la présente étude, a révélé que plus de 50 % des microdoseurs de psilocybine combinaient la psilocybine avec diverses substances, et que l'HE était l'ajout le plus courant, suivi d'une combinaison de niacine (vitamine B3) et d'HE8. Comme il s'agit de la seule étude portant sur l'empilage, on ne sait pas si ces résultats peuvent être généralisés. La combinaison d'HE, de B3 et de psilocybine a été popularisée dans les réseaux informels d'information sur le microdosage, sur la base de l'hypothèse selon laquelle la B3 pourrait faciliter la biodisponibilité de la psilocybine et de l'HE par le biais de la vasodilatation29. Il a été proposé que les effets salutaires de la psilocybine et de l'HE passent par des processus liés au BDNF, ce qui soulève la possibilité d'effets super-additifs30,31. Cependant, les effets potentiels de la psilocybine et de l'HE - avec ou sans B3 - n'ont pas encore été formellement étudiés, et la popularité de l'empilage découle probablement de l'auto-expérimentation et de rapports anecdotiques.
En résumé, malgré des résultats suggestifs et un intérêt croissant de la part du public, la littérature empirique reste équivoque sur les conséquences du microdosage. Des recherches supplémentaires avec des groupes de contrôle et des échantillons de grande taille permettant d'examiner les modérateurs potentiels tels que l'état de santé mentale, l'âge et le sexe sont nécessaires pour mieux apprécier les conséquences de ce phénomène émergent sur la santé. Dans la présente étude, nous visons à étendre cette littérature en examinant les changements prospectifs associés au microdosage de psilocybine par rapport à un groupe de contrôle non microdosé dans les domaines de la santé mentale, de l'humeur et du fonctionnement cognitif et psychomoteur. À notre connaissance, il s'agit de la plus grande étude prospective à ce jour sur le microdosage de psilocybine, la première à faire la distinction entre les mélanges de microdosage (c'est-à-dire l'empilage), et parmi les rares études prospectives à désagréger systématiquement les analyses en fonction de l'âge et des préoccupations en matière de santé mentale.
Méthodes
Conception et participants
Nous avons recueilli des données longitudinales entre novembre 2019 et mai 2021 auprès de répondants auto-sélectionnés (tableau 1) tirés d'une étude plus large sur le microdosage psychédélique. L'échantillon recoupe partiellement un échantillon beaucoup plus large décrit dans une étude transversale antérieure8; mais ajoute les participants recrutés après cette analyse, et exclut les participants qui n'ont pas complété l'évaluation de suivi à un mois et dont le microdosage ne comprenait pas de psilocybine. Le matériel de l'étude a été intégré dans une application disponible pour les utilisateurs d'Apple iOS32 qui répondaient aux critères d'inclusion, à savoir être âgé de 18 ans ou plus, savoir lire en anglais et avoir accès à un appareil iOS. Les microdoseurs et les personnes ne pratiquant pas le microdosage étaient éligibles pour participer à l'étude et ont été recrutés simultanément par le biais des médias liés à l'utilisation des psychédéliques et par des présentations lors d'événements de recherche et d'éducation sur les psychédéliques.Tableau 1 Caractéristiques des participants.
Tableau complet
L'étude consistait en une évaluation de base réalisée au début de l'étude et en une évaluation de suivi réalisée 22 à 35 jours plus tard ; les calendriers d'évaluation étaient équivalents pour les microdoseurs et les non-microdoseurs. Les évaluations portaient sur les pratiques psychédéliques du mois précédent, l'humeur et la santé mentale, et présentaient des tâches testant le traitement cognitif et psychomoteur. Chaque évaluation a duré de 20 à 30 minutes, avec une variabilité due à l'embranchement, de sorte que de nombreux éléments n'ont été présentés qu'à un sous-ensemble de participants. Le consentement éclairé de tous les participants a été obtenu, l'étude a été approuvée par le comité d'éthique de la recherche de l'université de Colombie-Britannique (H19-03051) et toutes les méthodes ont été appliquées conformément à ses directives et règlements. Les hypothèses et les résultats n'ont pas été enregistrés au préalable.
Les données descriptives figurent dans le tableau 1. L'âge a été évalué de manière catégorique et dichotomisé en 55 ans et plus et moins de 55 ans pour évaluer les différences potentielles entre les groupes tout en tenant compte de la taille des groupes pour maintenir la puissance statistique. La présence de problèmes de santé mentale a été évaluée à l'aide de la question suivante : "Avez-vous actuellement des problèmes psychologiques, de santé mentale ou de toxicomanie? L'humeur a été évaluée à l'aide du Positive And Negative Affect Schedule (PANAS)33, une mesure d'auto-évaluation de 20 items avec des sous-échelles de 10 items qui évaluent l'affect positif et négatif. En raison d'une erreur technique, un élément de la sous-échelle négative a été exclu ; pour remédier à ce problème, les scores ont été convertis en pourcentages. La dépression, l'anxiété et le stress ont été mesurés à l'aide de l'échelle DASS-21 (Depression Anxiety Stress Scale-21)34, qui comporte trois sous-échelles de 7 items notés sur une échelle de 4 points. Les tâches cognitives et psychomotrices ont été adaptées de l'Apple Research Kit, qui a été utilisé et validé dans plusieurs grandes études35,36. La capacité psychomotrice a été mesurée à l'aide d'une version adaptée de la tâche de tapotement du doigt37, dans laquelle les participants tapotaient deux cercles adjacents sur l'écran d'un appareil iOS en alternance pendant 10 s à l'aide de l'index et du majeur de leur main dominante. Des protocoles similaires de tapotement des doigts sur smartphone ont démontré une bonne validité prédictive et discriminante pour les troubles neurodégénératifs37,38. L'empan de mémoire spatiale a été évalué à l'aide d'une version adaptée de la tâche de Corsi Block-Tapping39, dans laquelle les participants se souviennent de l'emplacement des stimuli sur une grille carrée au cours d'une série limitée dans le temps de tours de difficulté croissante40,41. Le critère utilisé dans cette étude était le nombre de réponses correctes. La vitesse de traitement a été évaluée à l'aide d'un test adapté, le Paced Auditory Serial Addition Test (PASAT)42,43, qui consiste à additionner de manière itérative des nombres entiers alternés ; le critère était le nombre total de réponses correctes.
Analyses statistiques
Des modèles d'effets linéaires mixtes ont été générés pour 8 résultats : DASS dépression, DASS anxiété, DASS stress, PANAS positif, PANAS négatif, nombre de tapotements au test du doigt, score à l'empan spatial et score au PASAT. La modélisation multiniveau a été choisie pour l'analyse en raison de sa capacité à tester simultanément les différences entre les groupes et à l'intérieur des groupes, à intégrer des observations inégalement espacées entre les participants, comme c'était souvent le cas dans la présente étude, et à résister à l'inflation des erreurs de type I résultant des tests multiples44. Tous les modèles comprenaient l'effet continu du temps (jours depuis la réponse de base) et le facteur dichotomique du groupe demicrodose (non-microdoseurs codés 0, microdoseurs codés 1). Pour construire des modèles parcimonieux et maintenir des sous-groupes de taille adéquate, un seul modérateur supplémentaire a été inclus dans les modèles. L'âge a été examiné en tant que modérateur pour les tests de fonctionnement cognitif et d'humeur, tandis que, compte tenu de sa pertinence pour les domaines DASS de la dépression, de l'anxiété et du stress, la présence de problèmes de santé mentale a été examinée au lieu de l'âge en tant que modérateur dans les trois modèles qui examinaient les scores DASS. Plus précisément, l'âge a été introduit comme une variable dichotomique entre les personnes dans les modèles avec le PANAS, le finger tap, le PASAT et les tests d'empan spatial, et les problèmes de santé mentale ont été inclus dans les modèles avec les domaines de la DASS.Les modèles ont été construits de telle sorte que les variables ont été retenues si elles prédisaient le résultat du modèle ou si elles étaient un élément constitutif d'une interaction significative de niveau supérieur. Pour les résultats pour lesquels une interaction Microdose*Temps a été identifiée, des modèles factoriels complets ont été construits, incluant l'interaction à trois voies Microdose*Temps*Genre, et soit Microdose*Temps*Age, soit Microdose*Temps*Préoccupations de santé mentale, ainsi que tous les effets principaux de niveau inférieur et les effets d'interaction à deux voies. Les analyses supplémentaires ont éliminé les réponses aberrantes qui s'écartaient de plus de deux écarts-types de la moyenne de leur groupe respectif. Une deuxième série d'analyses supplémentaires a exclu les participants ayant déclaré un microdosage avant le début de l'étude afin de contrôler les effets de report potentiels associés aux antécédents de microdosage. Plus précisément, les participants ayant déclaré une pratique active du microdosage lors de l'évaluation de référence ont été retirés ; nous avons donc comparé les microdoseurs qui ont commencé leur pratique après l'évaluation de référence et l'évaluation de suivi à ceux qui n'ont pas pratiqué de microdosage au cours de cette période. Pour évaluer l'empilement, nous avons suivi ces analyses avec jusqu'à trois séries d'analyses supplémentaires dans le groupe des microdoseurs. Ces analyses supplémentaires ont été limitées aux résultats qui ont mis en évidence un effet Microdose*Temps afin d'éviter l'inflation de l'erreur de type I due aux tests multiples. Dans la première de ces analyses, lesmicrodoseurs Psilocybine+HE ont été comparés aux microdoseurs Psilocybine seule. Une deuxième série d'analyses a comparé lesmicrodoseurs de Psilocybine+HE+B3 aux microdoseurs de Psilocybine seule. Comme dans les analyses primaires, nous avons également examiné les effets modérateurs de l'âge ou des problèmes de santé mentale. Dans les cas où l'une ou l'autre de ces deux analyses complémentaires a révélé des effets d'interaction significatifs à deux ou trois voies, elles ont été suivies d'une dernière analyse complémentaire comparant lesmicrodoseurs de Psilocybine+HE à ceux de Psilocybine+HE+B3. Les analyses du chi-carré ont évalué l'équivalence des sous-groupes en fonction de l'âge, du nombre de jours de microdose au cours du mois écoulé et de la dose de microdose ; les différences dans ces facteurs ont été contrôlées en éliminant au hasard des participants du sous-groupe qui était disproportionné jusqu'à ce que les proportions des groupes soient considérées comme statistiquement équivalentes45. Le d de Cohen a été calculé pour les effets afin de faciliter l'interprétation et de permettre la comparaison des tailles d'effet entre les groupes et avec les recherches antérieures (tableau 2).
Tableau 2 Microdoseurs et non-microdoseurs sur une période d'un mois.
Tableau complet
Résultats
Les microdosseurs étaient plus susceptibles que les non-microdosseurs d'être plus âgés(x2(2, N = 1133) = 22,13, p< 0,01), d'être de race blanche(x2(1, N = 1133) = 4,62, p= 0.03) et de déclarer un emploi à temps plein(x2(3, N = 1122) = 11,83, p< 0,01) ; les groupes étaient équivalents dans tous les autres domaines démographiques (tous les x2<6,03, tous les p> 0,05 ; voir tableau 1). Les comparaisons entre les microdoseurs de la posologie et des jours de microdose du mois précédent n'ont révélé aucune différence en fonction de l'âge (jours : x2(2, N = 953) = 3,37, p= 0,19 ; dose : x2(2, N = 953) = 3,31, p= 0,19) et des préoccupations en matière de santé mentale (jours : x2(2, N = 931) = 0,71, p= 0,70 ; dose : x2(2, N = 931) = 0,21, p= 0,90).Les analyses préliminaires ont permis d'identifier les différences attendues en fonction de l'âge; le groupe des moins de 55 ans a affiché des performances supérieures à celles du groupe des 55 ans et plus dans toutes les tâches cognitives ; pour le test de tapotement (moyenne = 70,48 (33,18) contre 52,60 (29.99) ; t (1, 863) = 5.05, p< 0.01) ; pour le PASAT (moyenne = 33.67(14.21) contre 30.37 (12.92) t (1, 772) = 2.08, p< 0.05) et l'espacement (moyenne = 236.25 (51.02) contre 176.88 (58.80) ; t (1, 943) = 11.00, p< 0.01). Les différences de base en fonction de l'âge ont été identifiées pour l'humeur négative (moyenne = 46,89 (16,13) contre 40,64 (16,06) ; t (1, 1048) = 3,96, p< 0,01) mais pas pour l'humeur positive (moyenne = 55% (16) contre 55,03% (15,01) ; t (1, 1048) = - 0,018, p= 0,99). Comme on pouvait s'y attendre, les participants qui ont fait état de problèmes de santé mentale ont obtenu des scores plus élevés sur les trois sous-échelles du DASS : Dépression (moyenne = 10,44 (9,72) contre 18,92 (12) ; t (1, 1010) = - 11,81, p< 0,01) ; Anxiété (moyenne = 6,38 (6,36) contre 11.38 (8,74) ; t (1, 1010) = 10,09, p< 0,01) et Stress (moyenne = 13,84 (9,1) contre 20,04 (9,8) ; t (1, 1010) = 9,61, p< 0,01). L'analyse par sexe n'a révélé aucun effet principal du sexe au fil du temps dans aucun des domaines de la DASS (tous les F < 1,6, p> 0,20).
Dépression, anxiété, stress
Les comparaisons entre les microdoseurs et les non-microdoseurs en ce qui concerne le changement entre la ligne de base et le mois 1(Microdose*temps) ont indiqué des améliorations plus importantes chez les microdoseurs dans les domaines DASS de la dépression(F (1, 1019) = 17.91, b= 0,12, p< 0,01), de l'anxiété(F (1, 1017) = 18,33, b= 0,08, p< 0,01) et du stress(F (1, 1016) = 15,60, b= 0,08, p< 0,01) (Fig. 1; Tableau 2). Ces effets sont restés constants après l'élimination de 124, 82 et 75 valeurs aberrantes dans les domaines de la dépression, de l'anxiété et du stress respectivement pour les scores dépassant 2 écarts-types de la moyenne(tous les FMicrodose*temps > 7,99 p< 0,01), et dans les analyses parallèles restreintes aux 594 participants qui n'ont pas signalé de microdosage avant la ligne de base(tous les FMicrodose*temps > 4,17, p< 0,05). Nous avons identifié une interaction Microdose*Genre*Temps de sorte que l'effet du microdosage dans le temps s'est avéré être modéré par le genre dans la dépression DASS. Plus précisément, les réductions de la dépression liées au microdosage étaient plus fortes chez les femmes que chez les hommes(F (1, 1016) = 6,61, b= 0,17, p= 0,01). Aucune interaction microdose* sexe*temps n'a été identifiée pour l'anxiété DASS(F (1, 1024) = 1,14, b= 0,46, p= 0,29) ou le stress DASS(F (1, 1023) = 0,90, b= 0,05, p= 0,34).Figure 1

Microdosage et santé mentale. Les valeurs de "base" reflètent les réponses moyennes des participants recueillies entre 0 et 7 jours après le début de l'étude. Les valeurs du "mois 1" reflètent les réponses moyennes des participants recueillies entre 22 et 35 jours après le début de l'étude.
Agrandir l'image
Les interactions entre les groupes " santé mentale" et "microdose " n'étaient significatives pour aucun des domaines(tous les FsMicrodose*Santé mentale*Temps < 1,16 ; p> 0,10), ce qui indique que les effets principaux du microdosage étaient cohérents entre les personnes interrogées présentant ou non des troubles de la santé mentale. Parmi les microdoseurs ayant des problèmes de santé mentale , les scores de dépression sont passés de 18,85 (12,03) à l'inclusion à 11,73 (9,85) au mois 1 ; pour l'anxiété, de 11,04 (8,48) à l'inclusion à 7,46 (6,68) au mois 1 ; et pour le stress, de 19,93 (9,71) à l'inclusion à 13,91 (9,02) au mois 1. Parmi les répondants sans antécédents de problèmes de santé mentale, les scores de dépression sont passés de 10,40 (9,78) au départ à 6,65 (7,60) au mois 1 ; pour l'anxiété, de 6,53 (6,50) au départ à 4,81 (5,57) au mois 1 ; et pour le stress, de 13,96 (9,12) au départ à 9,78 (7,50) au mois 1. Des analyses supplémentaires ont comparé les conditions d'empilage sur les changements dans les scores de dépression, d'anxiété et de stress du DASS de la ligne de base au mois 1. Aucune différence entre les microdoseurs Psilocybine seule et lesmicrodoseurs Psilocybine+HE (tous F < 0,70 ; p> 0,10) n'a été notée. De même, aucune différence entre les microdoseurs de psilocybine seule et lesmicrodoseurs de psilocybine+HE+B3 n'a été identifiée (tous F < 0,77 ; p> 0,10).
Humeur
Les résultats des deux sous-échelles du PANAS reflètent ceux du DASS. Par rapport aux non-microdoseurs, les microdoseurs ont montré des augmentations plus importantes de l'humeur positive de la ligne de base au mois 1 (F (1, 1058) = 59,98, b= - 0,32, p< 0,01) et des diminutions plus importantes de l'humeur négative pendant la durée de l'étude (F (1, 1059) = 33,76, b= 0,23, p< 0,01). Ces effets sont restés constants après l'élimination de 75 et 76 réponses aberrantes dans les domaines de l'humeur positive et négative respectivement pour les scores qui dépassaient deux écarts-types au-dessus ou au-dessous de la moyenne(tous les Microdose*time F > 26,32 ; p< 0,01), et parmi les 479 participants qui pratiquaient le microdosage au moment du début de l'étude(tous les Microdose*time F > 22,05 ; p< 0,01). En outre, les analyses modératrices ont indiqué que ces effets restaient stables en fonction du sexe(tous les Microdose*Genre*Temps F < 1,94 ; p> 0,05).L'interaction entre l'âge, l'état de la microdose et le temps n'était pas significative pour l'humeur positive(F (1, 1058) = 0,21, b= - 0,05, p= 0,65) ou l'humeur négative(F (1, 1059) = 1,38, b= 0,13 p= 0,24), ce qui indique l'équivalence des effets sur l'humeur en fonction de l'âge. Les analyses de suivi n'ont pas identifié de différences significatives dans les changements de l'humeur positive ou négative au fil du temps entre les microdoseurs Psilocybine seule et lesmicrodoseurs Psilocybine+HE (tous F < 0,52, p> 0,47) ou lesmicrodoseurs Psilocybine+HE+B3 (tous F < 2,44, p> 0,12).
Performances psychomotrices et cognitives
Les analyses du test du doigt ont identifié un effet principal pour le microdosage, de sorte que les microdoseurs ont démontré un changement plus positif dans la performance que les non-microdoseurs (F (1, 886) = 9,09, b= - 0,24, p= 0,03; Tableau 2). Les analyses supplémentaires n'ont pas révélé d'interaction significative à trois voies entre la microdose, le sexe et le temps, ce qui indique que les effets du microdosage étaient cohérents entre les sexes(F= 0,26, b= 0,94, p= 0,61). L'effet du microdosage sur le score du tap au fil du temps était robuste après l'élimination de 16 réponses aberrantes avec des scores à 2 écarts types de la moyenne(Microdose*Temps F= 7,23, b= - 0,21, p= 0,07), et les effets du traitement sont restés cohérents lorsque l'échantillon de l'étude a été limité aux 515 participants qui ne prenaient pas de microdosage au début de l'étude(Microdose*Temps F= 5,07, b= 0,22, p= 0,03). Enfin, l'interaction entre Microdose*Temps*Age n'était pas significative(F= 3,41, b= 0,43, p= 0,06), ce qui indique que l'effet du microdosage était cohérent en fonction de l'âge.Les analyses de l'empilement entre les microdoseurs (Fig. 2) n'ont révélé aucune interaction entre Psilocybine seule et psilocybine+HE*Temps, ce qui suggère que l'ajout de HE n'a pas eu d'impact sur l'effet de la psilocybine sur le tapotement des doigts (F (1, 524) = 0,284, b= 0,12, p= 0,67). En revanche, l'interaction Psilocybine seule vs psilocybine+HE+B3*Temps a indiqué une amélioration relativement plus importante des scores de tapotement avec l'ajout de HE et de B3 à la psilocybine (F (1, 732) = 3,93, b= - 0,51, p< 0,05). Ce résultat a été suivi par l'examen de l'effet modérateur de l'âge, qui a identifié une interaction Psilocybine seule vs psilocybine+HE+B3 * Temps *Age (F (1, 732) = 8,4, b= 0,6, p= 0,04), ce qui reflète que l'ajout de HE et de B3 a eu un impact chez les répondants plus âgés, mais pas chez les plus jeunes. Les analyses supplémentaires de Psilocybine+HE vs psilocybine+HE+B3 * Temps ont révélé une tendance à la signification (F (1, 427) = 3,26, b= - 0,56, p= 0,07), et l'interaction tripartite Psilocybine+HE vs psilocybine+HE+B3 *Temps*Age a été identifiée (F (1, 427) = 6,71, b= 0,66, p= 0,01), ce qui indique que les effets étaient plus prononcés chez les répondants plus âgés. Des analyses complémentaires de suivi ont indiqué que ces résultats étaient robustes après avoir contrôlé les différences entre les sous-groupes en termes d'âge, de fréquence des microdoses et de dosage des microdoses (toutes les interactions à trois voies Fs > 6,20, p< 0,05).
Figure 2

Microdosage et scores au test du doigt. Les valeurs "de base" reflètent les réponses moyennes des participants recueillies entre 0 et 7 jours après le début de l'étude. Les valeurs du "mois 1" reflètent les réponses moyennes des participants recueillies entre 22 et 35 jours après le début de l'étude. PS fait référence aux participants qui ont reçu une microdose de psilocybine en l'absence de Lion's Mane (HE). PS + HE se réfère aux participants qui ont microdosé la psilocybine et l'HE en l'absence de niacine (B3). PS + HE + B3 microdoseurs se réfère aux participants qui microdosent la psilocybine avec HE et B3. Les différences dans les pentes des conditions de groupe ont fait l'objet d'analyses d'interaction Microdose*Temps.
Agrandir l'image
Les comparaisons entre les microdoseurs et les non-microdoseurs en ce qui concerne le changement entre la ligne de base et le mois 1 n'ont indiqué aucune différence pour la tâche d'empan spatial (F (1, 944) = 0,24, b= - 0,07, p= 0,63) ou le PASAT (F (1, 775) = 0,21, b= 0,02, p= 0,65). Compte tenu de cette absence d'effets principaux, aucune analyse de suivi n'a été effectuée.
Discussion
Les résultats de cette étude contribuent à la littérature croissante sur le microdosage de plusieurs façons. Tout d'abord, bien que notre modèle d'étude diffère considérablement des modèles des études longitudinales antérieures relativement peu nombreuses sur le microdosage de psychédéliques - en particulier en ce qui concerne les tentatives de prise en compte de l'influence potentielle des attentes - nos résultats d'amélioration de l'humeur et de réduction des symptômes de dépression, d'anxiété et de stress sont néanmoins généralement similaires en direction et en taille aux effets positifs faibles à moyens non ajustés rapportés dans ces études7,17,18. À notre connaissance, il s'agit de la plus grande étude longitudinale à ce jour sur le microdosage de psilocybine et l'une des rares études à faire appel à un groupe témoin17,18,19,20. À la lumière de ces atouts méthodologiques, la comparabilité de nos résultats avec ceux d'études antérieures menées dans divers endroits et avec des méthodologies différentes suggère une association relativement cohérente entre le microdosage et l'amélioration de la santé mentale. Notamment, le sous-groupe de personnes interrogées qui ont signalé des problèmes de santé mentale au moment de l'évaluation de base a montré une réduction moyenne des symptômes dépressifs qui a entraîné un changement de dépression modérée à légère après environ 30 jours de microdosage de psychédéliques46. Compte tenu des coûts de santé considérables et de l'omniprésence de la dépression, ainsi que de la proportion importante de patients qui ne répondent pas aux traitements existants, le potentiel d'une autre approche pour traiter ce trouble mortel mérite d'être pris en considération. La possibilité que le microdosage de psilocybine puisse fournir un moyen d'améliorer la dépression et l'anxiété souligne clairement la nécessité de poursuivre les recherches pour établir plus fermement la nature de la relation entre le microdosage, l'humeur et la santé mentale, et la mesure dans laquelle ces effets sont directement attribuables à la psilocybine.Une contribution potentielle de la recherche future avec des modèles contrôlés par placebo serait la capacité de désagréger les contributions des attentes positives et des effets placebo. Bien que notre utilisation d'un groupe de non-microdoseurs qui était équivalent aux microdoseurs en ce qui concerne les données démographiques et l'engagement dans les procédures de l'étude soit une force évidente, les microdoseurs et les non-microdoseurs de notre étude étaient conscients de leur statut dès le début de l'étude, ce qui rend impossible d'exclure les contributions d'attentes plus importantes dans le groupe de microdoseurs par rapport au groupe de non-microdoseurs. Toutefois, compte tenu des difficultés associées à la réalisation d'essais contrôlés randomisés dans l'environnement réglementaire restrictif actuel et des difficultés plus générales liées à l'aveuglement efficace d'un médicament de recherche ayant des effets psychoactifs bien connus et distinctifs, nous encourageons la recherche à adopter une perspective élargie sur les effets putatifs des placebos24. Plus précisément, le réexamen clinique et l'étude des psychédéliques offrent l'occasion de réévaluer la mesure dans laquelle les attentes et les effets psychoactifs francs peuvent se combiner pour influencer le bien-être subjectif de manière potentiellement significative19.
L'impact du microdosage sur les tests de fonctionnement cognitif et psychomoteur était mitigé et limité aux performances psychomotrices, sans impact apparent sur la mémoire spatiale ou la vitesse de traitement. En outre, l'ampleur de ces effets semblait dépendre de l'âge et de la combinaison de psilocybine avec HE et B3. Cette spécificité pour les performances psychomotrices et la dépendance à la combinaison des composants justifient une interprétation prudente, car la littérature sur le microdosage et les performances cognitives est peu abondante18 et aucune étude antérieure ne s'est concentrée sur la combinaison de la psilocybine avec d'autres substances supposées actives. En effet, bien que notre large échantillon ait permis un nouveau niveau de granularité dans notre examen des pratiques distinctes parmi les sous-groupes de microdoseurs liés à l'âge, ces groupes étaient néanmoins relativement petits, ce qui augmente la possibilité que nos résultats de facilitation des tests de tap chez les personnes de plus de 55 ans qui microdosent la combinaison de psilocybine, HE et B3 puissent être anormaux. En outre, en raison du petit nombre de participants prenant du B3 sans psilocybine ni HE, nous n'avons pas eu la puissance nécessaire pour étudier dans quelle mesure ces résultats étaient dus à la combinaison de psilocybine, B3 et HE, par opposition au B3 seul. De plus, l'âge a été collecté de manière catégorique et l'âge limite de 55 ans a été choisi par commodité en fonction de la puissance, ce qui nous empêche de déterminer dans quelle mesure les effets observés seraient maintenus si d'autres seuils d'âge étaient utilisés. Nous ne sommes donc pas en mesure de déterminer dans quelle mesure les effets observés se maintiendraient si l'on utilisait d'autres seuils pour l'âge. Néanmoins, si ces résultats s'avèrent robustes dans divers échantillons et chez divers chercheurs, ils pourraient représenter une première étape importante dans le développement de nouveaux traitements pour les troubles neurologiques répandus et réfractaires. Enfin, bien que ces résultats puissent être décrits comme suggestifs, ils ajoutent néanmoins une crédibilité préliminaire aux rapports anecdotiques sur les bienfaits de la combinaison spécifique de psilocybine, d'HE et de B330.
En plus des petits échantillons dans les sous-groupes, de la conception observationnelle et d'une approche généralement exploratoire, l'interprétation est également limitée par un biais de réponse potentiel lié à l'autosélection des participants et au recrutement dans des lieux favorables à l'utilisation de psychédéliques, ce qui peut avoir entraîné une surreprésentation dans notre échantillon des personnes qui réagissent favorablement au microdosage. De plus, l'indisponibilité d'une version Android OS de l'application au moment de l'étude a limité la participation aux personnes ayant accès à des appareils Apple. Cette étude n'a pas non plus examiné l'influence de la dose et des pratiques de dosage sur les résultats. De futures études avec des conceptions permettant une évaluation minutieuse de la puissance, de la composition et de la quantité des matériaux microdosés seront nécessaires pour affiner notre compréhension de l'influence de ces facteurs clés. De même, les effets indésirables et les interactions avec les antidépresseurs et les anxiolytiques habituels n'ont pas été évalués ; ces données seront nécessaires pour mieux comprendre la sécurité et l'acceptabilité du microdosage. À la lumière de ces limites, nous encourageons les recherches futures qui utilisent une approche de recrutement plus systématique et des modèles qui évaluent le dosage optimal, les meilleures pratiques et les effets indésirables associés au microdosage psychédélique.
Références
- Carod-Artal, F. J. Hallucinogenic drugs in pre-Columbian Mesoamerican cultures (édition anglaise). (Neurolia, 2015).
- Nye, B. C. Microdosing : Les gens qui prennent du LSD au petit-déjeuner. BBC News. BBC News (2017). Disponible à l'adresse : https://www.bbc.com/news/health-39516345.
- Williams, A. Comment le LSD a sauvé le mariage d'une femme. New York Times (2017).
- Fadiman, J. & Korb, S. Le microdosage de psychédéliques peut-il être sûr et bénéfique ? An initial exploration. J. Psychoactive Drugs https://doi.org/10.1080/02791072.2019.1593561 (2019).
Article PubMed Google Scholar - Ona, G. & Bouso, J. C. Sécurité potentielle, bénéfices et influence de l'effet placebo dans le microdosage des drogues psychédéliques : A systematic review. Neurosci. Biobehav. Rev. https://doi.org/10.1016/j.neubiorev.2020.09.035 (2020).
Article PubMed Google Scholar - Kuypers, K. P. C. et al. Microdosing psychedelics : Plus de questions que de réponses ? An overview and suggestions for future research. J. Psychopharmacol. https://doi.org/10.1177/0269881119857204 (2019).
Article PubMed PubMed Central Google Scholar - Polito, V. & Stevenson, R. J. A systematic study of microdosing psychedelics. PLoS ONE https://doi.org/10.1371/journal.pone.0211023 (2019).
Article PubMed PubMed Central Google Sch olar - Rootman, J., Kryskow, P., Harvey, K., Stamets, P., Santos-Brauls, E., Kupers, K. P. C., Polito, V., Bourzat, F., & Walsh, Z. Adults who microdose psychedelics report health related motivations and lower levels of anxiety and depression compared to non-microdosers. Nature : Sci. Rep. https://doi. org/10.1038/s41598-021-01811-4 (2021).
- Cameron, L. P., Nazarian, A. & Olson, D. E. Psychedelic microdosing : Prevalence and subjective effects. J. Psychoactive Drugs https://doi.org/10.1080/02791072.2020.1718250 (2020).
Article PubMed PubMed Central Google Scholar - Lea, T., Amada, N. & Jungaberle, H. Microdosage psychédélique : A subreddit analysis. J. Psychoactive Drugs https://doi.org/10.1080/02791072.2019.1683260 (2020).
Article PubMed Google Scholar - Rosenbaum, D. et al. Microdosing psychedelics : Demographics, practices, and psychiatric comorbidities. J. Psychopharmacol. https://doi.org/10.1177/0269881120908004 (2020).
Article PubMed Google Scholar - Hutten, N. R. P. W., Mason, N. L., Dolder, P. C. & Kuypers, K. P. C. Motifs et effets secondaires du microdosage de psychédéliques chez les utilisateurs. Int. J. Neuropsychopharmacol. https://doi.org/10.1093/ijnp/pyz029 (2019).
Article PubMed PubMed Central Google Scholar - Anderson, T. et al. Microdosing psychedelics : Personality, mental health, and creativity differences in microdosers. Psychopharmacology https://doi.org/10.1007/s00213-018-5106-2 (2019).
Article PubMed Google Scholar - Lea, T. et al. Perceived outcomes of psychedelic microdosing as self-managed therapies for mental and substance use disorders. Psychopharmacology https://doi.org/10.1007/s00213-020-05477-0 (2020).
Article PubMed Google Scholar - Johnstad, P. G. Powerful substances in tiny amounts : An interview study of psychedelic microdosing. NAD Nord. Stud. Alcohol Drugs https://doi.org/10.1177/1455072517753339 (2018).
Article Google Scholar - Webb, M., Copes, H. & Hendricks, P. S. Narrative identity, rationality, and microdosing classic psychedelics. Int. J. Drug Policy https://doi.org/10.1016/j.drugpo.2019.04.013 (2019).
Article PubMed Google Scholar - Szigeti, B. et al. Self-blinding citizen science to explore psychedelic microdosing. Elife 10, e62878. https://doi.org/10.7554/eLife.62878 (2021).
CAS Article PubMed PubMed Central Google Scholar - Kaertner, L. S. et al. Positive expectations predict improved mental-health outcomes linked to psychedelic microdosing. Sci. Rep. https://doi. org/10.1038/s41598-021-81446-7 (2021).
Article PubMed PubMed Central Google Scholar - Van Elk, M. et al. Effects of psilocybin microdosing on awe and aesthetic experiences : A preregistered field and lab-based study. Psychopharmacology https://doi.org/10.1007/s00213-021-05857-0 (2021).
Article PubMed PubMed Central Google Scholar - Marschall, J. et al. Psilocybin microdosing does not affect emotion-related symptoms and processing : A preregistered field and lab-based study. J. Psychopharmacol. 36(1), 97 (2022).
Article Google Scholar - Muthukumaraswamy, S. D., Forsyth, A. & Lumley, T. Blinding and expectancy confounds in psychedelic randomized controlled trials. Expert. Rev. Clin. Pharmacol. https://doi.org/10.1080/17512433.2021.1933434 (2021).
Article PubMed Google Scholar - Sleep, C. E., Lynam, D. R., Hyatt, C. S. & Miller, J. D. Perils of partialing redux : The case of the dark triad. J. Abnorm. Psychol. https://doi.org/10.1037/abn0000278 (2017).
Article PubMed Google Scholar - Lynam, D. R., Hoyle, R. H. & Newman, J. P. The perils of partialling : cautionary tales from aggression and psychopathy. Assessment 13(3), 328-341. https://doi.org/10.1177/1073191106290562 (2006).
Article PubMed PubMed Central Google Scholar - Schenberg, E. E. Qui est aveugle dans la recherche psychédélique ? Letter to the editor regarding : blinding and expectancy confounds in psychedelic randomized controlled trials. Expert. Rev. Clin. Pharmacol. https://doi.org/10.1080/17512433.2021.1951473 (2021).
Article PubMed Google Scholar - Nagano, M. et al. Reduction of depression and anxiety by 4 weeks Hericium erinaceus intake. Biomed. Res. https://doi. org/10.2220/biomedres.31.231 (2010).
Article PubMed Google Scholar - Mori, K., Inatomi, S., Ouchi, K., Azumi, Yo. & Tuchida, T. Improving Effects of the Mushroom Yamabushitake on Mild Cognitiv Impairment. Zhongguo Zhong Yao Za Z hi (2009).
- Tsai-Teng, T. et al. Erinacine A-enriched Hericium erinaceus mycelium ameliorates Alzheimer's disease-related pathologies in APPswe/PS1dE9 transgenic mice. J. Biomed. Sci. https://doi. org/10.1186/s12929-016-0266-z (2016).
Article PubMed PubMed Central Google Scholar - Yang, P. P., Lin, C. Y., Lin, T. Y. & Chiang, W. C. Hericium erinaceus mycelium exerts neuroprotective effect in Parkinson's disease-in vitro and in vivo models. J. Drug Res. Dev. https://doi.org/10.16966/2470-1009.150 (2020).
Article Google Scholar - Stamets, P. Psilocybin mushrooms and the mycology of consciousness. (Exposé invité à Psychedelic Science, 2017).
- de Vos, C. M. H., Mason, N. L. & Kuypers, K. P. C. Psychédéliques et neuroplasticité : A systematic review unraveling the biological underpinnings of psychedelics. Front. Psychiatry https://doi.org/10.3389/fpsyt.2021.724606 (2021).
Article PubMed PubMed Central Google Scholar - Vigna, L. et al. Hericium erinaceus améliore les troubles de l'humeur et du sommeil chez les patients souffrant de surpoids ou d'obésité : Could circulating pro-BDNF and BDNF Be potential biomarkers ? Evidence-based Complement. Altern. Med. https://doi.org/10.1155/2019/7861297 (2019).
Article Google Scholar - Quantified Citizen. Quantified Citizen (Versions 1.1.-1.2.1.) [Mobile app]. Apple App store. (2019). https://apps.apple.com/us/app/quantified-citizen/id1485884140
- Watson, D., Clark, L. A. & Tellegen, A. Development and validation of brief measures of positive and negative affect : The PANAS scales. J. Pers. Soc. Psychol. https://doi. org/10.1037//0022-3514.54.6.1063 (1988).
Article PubMed Google Scholar - Lovibond, P. F. & Lovibond, S. H. La structure des états émotionnels négatifs : Comparison of the Depression Anxiety Stress Scales (DASS) with the Beck Depression and Anxiety Inventories. Behav. Res. Ther. https://doi. org/10.1016/0005-7967(94)00075-U (1995).
Article PubMed Google Scholar - Bot, B. M. et al. The mPower study, Parkinson disease mobile data collected using ResearchKit. Sci. Data https://doi.org/10.1038/sdata.2016.11 (2016).
Article PubMed PubMed Central Google Scholar - Zens, M., Woias, P., Suedkamp, N. P. & Niemeyer, P. 'Back on track' : A mobile app observational study using apple's researchkit framework. JMIR mHealth uHealth https://doi.org/10.2196/mhealth.6259 (2017).
Article PubMed PubMed Central Google Scholar - Lee, C. Y. et al. A validation study of a smartphone-based finger tapping application for quantitative assessment of bradykinesia in Parkinson's disease. PLoS ONE https://doi.org/10.1371/journal.pone.0158852 (2016).
Article PubMed PubMed Central Google Scholar - Boukhvalova, A. K. et al. Identifier et quantifier le handicap neurologique via un smartphone. Front. Neurol. https://doi.org/10.3389/fneur.2018.00740 (2018).
Article PubMed PubMed Central Google Sch olar - Corsi, P. M. La mémoire humaine et la région temporale médiane du cerveau. Dissertatopm Abstracts International (1973).
- Farrell Pagulayan, K., Busch, R., Medina, K., Bartok, J. & Krikorian, R. Developmental normative data for the Corsi Block-Tapping task. J. Clin. Exp. Neuropsychol. https://doi.org/10.1080/13803390500350977 (2006).
Article PubMed Google Scholar - Brunetti, R., Del Gatto, C. & Delogu, F. eCorsi : Implementation and testing of the Corsi block-tapping task for digital tablets. Front. Psychol. https://doi.org/10.3389/fpsyg.2014.00939 (2014).
Article PubMed PubMed Central Google Scholar - Gronwall, D., & Sampson, H. The Psychological Effects of Concussion. Auckland University Press, 1974.
- Tombaugh, T. N. A comprehensive review of the Pacedory Auditory Serial Addition Test (PASAT). Arch. Clin. Neuropsychol. https://doi.org/10.1016/j.acn.2005.07.006 (2006).
Article PubMed Google Scholar - Gelman, A., Hill, J. & Yajima, M. Why we (usually) don't have to worry about multiple comparisons. J. Res. Educ. Eff. https://doi. org/10.1080/19345747.2011.618213 (2012).
Article Google Scholar - Rosenbaum, P. R. & Rubin, D. B. Reducing bias in observational studies using subclassification on the propensity score. J. Am. Stat. Assoc. https://doi. org/10.1080/01621459.1984 (1984).
Article Google Scholar - Lovibond, S. H. & Lovibond, P. F. Manual for the Depression Anxiety Stress Scales 2nd edn. (Psychology Foundation of Australia, 1995).
Google Scholar
Remerciements
Nous tenons à remercier Jim Fadiman pour ses conseils sur ce projet et son travail de pionnier sur le microdosage en général. Nous souhaitons également remercier l'ensemble de l'équipe de Quantified Citizen pour son soutien technique, en particulier Delano Mandelbaum. En outre, nous apprécions les conseils de Renee Davis, Zolton Bair et Chase Beathard de Fungi Perfecti. Enfin, nous tenons à remercier l'auteur principal, Joseph Rootman, pour son soutien financier, grâce à une subvention cofinancée par Mitacs et Quantified Citizen.Informations sur les auteurs
Auteurs et affiliations
- Département de psychologie, Université de la Colombie-Britannique, Kelowna, BC, Canada
Joseph M. Rootman et Zach Walsh - Quantified Citizen Technologies Inc, Vancouver, BC, Canada
Maggie Kiraga, Kalin Harvey & Eesmyal Santos-Brault - Département de médecine familiale, Université de la Colombie-Britannique, Vancouver, C.-B., Canada
Pamela Kryskow - Fungi Perfecti, LLC, MycoMedica Life Sciences, Olympia, WA, USA
Paul Stamets - Département de neuropsychologie et de psychopharmacologie, Faculté de psychologie et de neurosciences, Université de Maastricht, Maastricht, Pays-Bas
Maggie Kiraga et Kim P. C. Kuypers
Contributions
J.R. a conçu l'étude, analysé les données, rédigé en partie la première version du manuscrit, créé les références et édité le manuscrit. M.K. a participé à l'analyse des données, a partiellement rédigé la première version du manuscrit et a édité le manuscrit. P.K. a conçu l'étude, a partiellement rédigé la première version du manuscrit et a édité le manuscrit. K.H. a conçu l'étude, orchestré la collecte des données, rédigé partiellement la première version du manuscrit et édité le manuscrit. P.S. a conçu l'étude, a partiellement rédigé la première version du manuscrit et a édité le manuscrit. E.S.B. a conçu l'étude, orchestré la collecte des données, rédigé partiellement la première version du manuscrit et édité le manuscrit. K.P.C.K. a partiellement rédigé la première version du manuscrit et a édité le manuscrit. Z.W. a conçu l'étude, rédigé partiellement la première version du manuscrit et édité le manuscrit.Auteur correspondant
Correspondance à Joseph M. Rootman.Déclarations d'éthique
Intérêts concurrents
Joseph Rootman a reçu des fonds de recherche de Quantified Citizen Technologies, une société qui produit des logiciels pour la recherche mobile décentralisée et qui a fourni la plateforme de collecte de données pour cette étude. Maggie Kiraga est une employée de Quantified Citizen. Kalin Harvey est cofondateur et directeur technique de Quantified Citizen, cofondateur du Psychedelic Data Project, cofondateur et directeur de la Ketamine Assisted Therapy Association of Canada, et il est également investisseur dans MycoMedica Life Sciences. Pamela Kryskow est membre du comité consultatif clinique de Numinus Wellness, une société qui propose des services de psychothérapie psychédélique. Pamela Kryskow est rémunérée pour ce rôle par des actions de Numinus. Elle est consultante bénévole pour Nectara. Elle est cofondatrice de MycoMedica Life Sciences et fait partie du conseil consultatif scientifique et médical. Paul Stamets est un investisseur dans Quantified Citizen, MycoMedica Life Sciences, PBC et possède Fungi Perfecti, LLC qui vend des suppléments Lion Mane. Il est demandeur de brevets en instance combinant les champignons à psilocybine, les champignons Lions Mane et la niacine. Eesmyal Santos-Brault est cofondateur et PDG de Quantified Citizen, cofondateur du Psychedelic Data Project et investisseur dans MycoMedica Life Sciences. Kim PC Kuypers est chercheur principal dans des projets de recherche, dont la présente étude ne fait pas partie, qui sont sponsorisés par Mindmed et Silopharma, des entreprises qui développent des médicaments psychédéliques, et elle est membre rémunéré du conseil scientifique de Clerkenwell Health. Zach Walsh est en relation de conseil rémunéré avec Numinus Wellness et Entheotech BioMedical en ce qui concerne le développement médical des psychédéliques, et il est membre du conseil consultatif de la Multidisciplinary Association for Psychedelic Studies (MAPS) Canada et de MycoMedica Life Sciences.
