- Joined
- Apr 10, 2022
- Messages
- 297
- Reaction score
- 161
- Points
- 43
Fonte : https://www.nature.com/articles/s41...rgM-fPwO6Nyexx4DSgugk0ki8Kdlc3KmylHUUO0jEpFro
Il microdosaggio prevede l'autosomministrazione regolare di sostanze psichedeliche in dosi sufficientemente piccole da non compromettere il normale funzionamento cognitivo6. Le sostanze più utilizzate per il microdosaggio sono i funghi psilocibinici e l'LSD, e in misura minore altre sostanze psichedeliche come la mescalina e la 2-CB7. Le indagini sul microdosaggio di psilocibina hanno individuato pratiche diverse, ma in generale convergono sull'autosomministrazione, da 3 a 5 volte alla settimana, di 0,1-0,3 g di funghi essiccati7,8,9,10,11,12. I miglioramenti dell'umore, del benessere emotivo e della cognizione sono stati segnalati tra le principali motivazioni per il microdosaggio13 e diversi studi trasversali hanno identificato associazioni tra il microdosaggio e i miglioramenti percepiti dell'umore13,14,15,16,17 e del funzionamento cognitivo10,11,16, la riduzione dello stress7, della depressione7,9,16 e dell'ansia7,9,14,18.
Sono relativamente pochi gli studi prospettici che hanno valutato il microdosaggio. Il primo studio longitudinale sul microdosaggio ha analizzato le valutazioni giornaliere di 98 microdosatori per 6 settimane e ha riscontrato miglioramenti transitori acuti in ampi domini del funzionamento psicologico nei giorni di microdosaggio e riduzioni dello stress, della depressione e della distraibilità dal basale alla conclusione dello studio. Inoltre, sebbene le conclusioni di questo studio siano limitate dalla mancanza di un gruppo di controllo non microdosatore, gli esami supplementari hanno concluso che gli effetti osservati non erano coerenti con quanto si sarebbe potuto prevedere sulla base delle aspettative comuni legate al microdosaggio7. Anche un successivo studio prospettico che ha seguito 81 microdosatori per quattro settimane ha riportato miglioramenti in diversi domini del benessere psicologico, tra cui una maggiore stabilità emotiva e una diminuzione di ansia e depressione. Tuttavia, analisi supplementari hanno suggerito che questi effetti positivi possono essere attribuiti alle aspettative e hanno evidenziato la necessità di ulteriori ricerche con partecipanti di controllo non microdosatori per distinguere meglio gli effetti del microdosaggio dagli effetti placebo e da altri fattori di confondimento longitudinali18.
L'uso efficace del placebo ha rappresentato una sfida nei pochi studi pubblicati che hanno tentato un disegno di questo tipo nel contesto del microdosaggio di psichedelici17,19,20. In particolare, uno studio prospettico sul microdosaggio che ha utilizzato un intervento di auto-accecamento per approssimare il controllo del placebo tra 191 partecipanti per 4 settimane ha identificato miglioramenti nel benessere emotivo tra i microdosatori, ma ha notato che la corretta identificazione della condizione è stata riportata dal 72% dei partecipanti, complicando la capacità di stimare in modo definitivo l'influenza degli effetti del placebo sui cambiamenti osservati. Analogamente, uno studio crossover in doppio cieco con controllo placebo su 30 intervistati seguiti per otto settimane ha identificato livelli più elevati di stupore auto-riferito in risposta alle esperienze estetiche tra i microdosatori rispetto ai controlli. Tuttavia, gli autori hanno riconosciuto i potenziali effetti confondenti della rottura del cieco, poiché due terzi dei partecipanti hanno indovinato accuratamente la loro condizione19. Un'ulteriore analisi dello stesso gruppo di partecipanti non ha individuato differenze nei sintomi di ansia e depressione tra i microdosatori rispetto al placebo20. Tuttavia, lo studio ha osservato che la precedente esperienza dei partecipanti con gli psichedelici, oltre ai bassi livelli di depressione e ansia, potrebbe aver attenuato gli effetti del microdosaggio. Inoltre, una percentuale significativa di partecipanti ha indovinato la propria condizione nella metà dei blocchi di prove, tuttavia gli effetti nulli apparenti dello studio possono rendere meno rilevante la potenziale influenza del placebo.
La rottura del cieco e la categoria più ampia degli effetti aspettativa o placebo sono sfide identificate per l'interpretazione degli studi sulle dosi regolari di psichedelici21 e possono complicare anche l'interpretazione della ricerca sul microdosaggio. Per esempio, lo studio longitudinale che ha tentato di aggiustare le aspettative controllando i punteggi di una misura modificata delle aspettative di microdosaggio18 ha notato che più dell'80% dei partecipanti ha riferito di aver avuto esperienze precedenti di uso di psichedelici, il che rende probabile che i punteggi della misura delle aspettative siano stati influenzati da esperienze passate di effetti diretti della droga. Le differenze individuali nella risposta alle droghe, dovute al metabolismo e a numerosi altri fattori, fanno sì che gli effetti farmacologici passati possano essere fortemente correlati con i successivi effetti farmacologici diretti e, pertanto, la parzializzazione (cioè il controllo per) delle aspettative può sottostimare gli effetti farmacologici diretti22,23. In sintesi, gli studi longitudinali esistenti hanno osservato effetti positivi associati al microdosaggio, ma non sono stati in grado di stimare con sicurezza i contributi farmacologici diretti a tali effetti. Più in generale, separare gli effetti diretti degli psichedelici da fattori indiretti come il set, il setting, le differenze individuali e le aspettative presenta sfide epistemologiche e pratiche, e lo studio degli psichedelici potrebbe essere meglio servito andando oltre l'enfasi potenzialmente procustea sul blinding e altri approcci per massimizzare il controllo24. Per esempio, l'esame naturalistico di ampie coorti offre potenti opportunità di esaminare la coerenza degli effetti tra i vari sottogruppi, e l'uso di un gruppo di confronto senza la premessa del cecità, ma con caratteristiche demografiche simili e livelli approssimativamente equivalenti di attività legate allo studio, consente di valutare l'impatto del microdosaggio in modo distinto dagli effetti indiretti come l'impegno nello studio, gli effetti della pratica, la regressione verso la media e altri potenziali artefatti comuni alla ricerca prospettica.
In concomitanza con l'aumento dell'interesse per il microdosaggio di funghi contenenti psilocibina, si registra un'accelerazione dell'interesse per altri funghi presumibilmente terapeutici. In particolare, la criniera di leone (Hericium erinaceus; HE) ha suscitato un notevole interesse per la sua proposta di trattamento della depressione25 e del lieve deterioramento cognitivo26 e per l'evidenza preclinica di una facilitazione della neurogenesi con implicazioni per il trattamento dei disturbi neurodegenerativi27,28. Recenti evidenze suggeriscono che alcuni microdosatori combinano la psilocibina con l'HE in un processo definito stacking8. Un'indagine trasversale su oltre 4.000 microdosatori, che ha utilizzato un campione parzialmente sovrapponibile a quello del presente studio, ha rilevato che oltre il 50% dei microdosatori di psilocibina combinava la psilocibina con diverse sostanze, e che l'HE era l'aggiunta più diffusa, seguita da una combinazione di niacina (vitamina-B3) e HE8. Poiché questo è l'unico studio che riporta lo stacking, la generalizzabilità di questi risultati è sconosciuta. La combinazione di HE, B3 e psilocibina è stata resa popolare nelle reti informali di informazione sul microdosaggio, sulla base dell'ipotesi che la B3 possa facilitare la biodisponibilità di psilocibina e HE attraverso la vasodilatazione29. È stato proposto che gli effetti salutari della psilocibina e dell'HE operino attraverso processi legati al BDNF, sollevando la possibilità di effetti super-additivi30,31. Tuttavia, i potenziali effetti della psilocibina e dell'HE, con e senza B3, non sono ancora stati studiati formalmente e la popolarità dell'accatastamento deriva probabilmente dalla sperimentazione autonoma e da rapporti aneddotici.
In sintesi, nonostante i risultati suggestivi e l'interesse crescente del pubblico, la letteratura empirica rimane equivoca sulle conseguenze del microdosaggio. Per valutare meglio le conseguenze sulla salute di questo fenomeno emergente sono necessarie ulteriori ricerche con gruppi di controllo e campioni ampi che consentano di esaminare potenziali moderatori come lo stato di salute mentale, l'età e il sesso. Nel presente studio, ci proponiamo di ampliare la letteratura esaminando i cambiamenti prospettici associati al microdosaggio di psilocibina rispetto a un gruppo di controllo non microdosatore su domini di salute mentale, umore e funzionamento cognitivo e psicomotorio. A nostra conoscenza, questo è il più grande studio prospettico finora condotto sul microdosaggio di psilocibina, il primo a distinguere tra le miscele di microdosaggio (cioè l'accatastamento) e tra i pochi studi prospettici a disaggregare sistematicamente le analisi in base all'età e ai problemi di salute mentale.
Tabella 1 Caratteristiche dei partecipanti.
Tabella a grandezza naturale
Lo studio consisteva in una valutazione di base completata all'inizio dello studio e in una valutazione di follow-up completata 22-35 giorni dopo; i programmi di valutazione erano equivalenti sia per i microdosatori che per i non microdosatori. Le valutazioni hanno riguardato le pratiche psichedeliche dell'ultimo mese, l'umore e la salute mentale e hanno presentato compiti di elaborazione cognitiva e psicomotoria. Ogni valutazione ha richiesto 20-30 minuti per essere completata, con una variabilità dovuta alla ramificazione, per cui molti elementi sono stati presentati solo a un sottoinsieme di partecipanti. Il consenso informato è stato ottenuto da tutti i partecipanti, lo studio è stato approvato dal Research Ethics Board dell'Università della British Columbia (H19-03051) e tutti i metodi sono stati eseguiti in conformità con le linee guida e i regolamenti. Le ipotesi e i risultati non sono stati pre-registrati.
I dati descrittivi sono riportati nella Tabella 1. L'età è stata valutata categoricamente e dicotomizzata in 55 anni e oltre e meno di 55 anni per valutare le potenziali differenze di gruppo, tenendo conto delle dimensioni del gruppo per mantenere la potenza statistica. La presenza di problemi di salute mentale è stata interrogata con l'item "Attualmente ha problemi psicologici, di salute mentale o di dipendenza?". L 'umore è stato valutato con la Positive And Negative Affect Schedule (PANAS)33, una misura self-report di 20 item con sottoscale di 10 item che valutano gli affetti positivi e negativi. A causa di un errore tecnico, è stato escluso un item della sottoscala negativa; per ovviare a questo inconveniente, i punteggi sono stati convertiti in percentuali. La depressione, l'ansia e lo stress sono stati misurati con la Depression Anxiety Stress Scale-21 (DASS-21)34, che presenta tre sottoscale con 7 item valutati su una scala a 4 punti. I compiti cognitivi e psicomotori sono stati adattati dall'Apple Research Kit, utilizzato e convalidato in diversi studi di grandi dimensioni35,36. L'abilità psicomotoria è stata misurata utilizzando una versione adattata del compito "finger tap "37, in cui i partecipanti hanno toccato due cerchi adiacenti sullo schermo di un dispositivo iOS in modo alternato per 10 s utilizzando l'indice e il medio della mano dominante. Protocolli simili di finger tap su smartphone hanno dimostrato una buona validità predittiva e discriminante per i disturbi neurodegenerativi37,38. La capacità di memoria spaziale è stata valutata con una versione adattata del compito Corsi Block-Tapping39, in cui i partecipanti ricordano la collocazione di stimoli su una griglia quadrata in una serie limitata di turni di difficoltà crescente40,41. Il criterio utilizzato in questo studio era il numero di risposte corrette. La velocità di elaborazione è stata valutata con un test adattato di addizione seriale uditiva (Paced Auditory Serial Addition Test, PASAT)42,43, che prevede la somma iterativa di numeri interi alternati; il criterio era il numero totale di risposte corrette.
I modelli sono stati costruiti in modo che le variabili venissero mantenute se prevedevano l'esito del modello o erano un componente di un'interazione significativa di livello superiore. Per gli esiti in cui è stata identificata un'interazione Microdose*Tempo, sono stati costruiti modelli fattoriali completi che includevano l'interazione a tre vie Microdose*Tempo*Genere e Microdose*Tempo*Età o Microdose*Tempo*Preoccupazioni per la salute mentale e tutti gli effetti principali e di interazione a due vie di livello inferiore. Le analisi supplementari hanno eliminato le risposte anomale che superavano le due deviazioni standard dalla media del rispettivo gruppo. Una seconda serie di analisi supplementari ha escluso i partecipanti che hanno riferito di aver praticato il microdosaggio prima dell'inizio dello studio, per controllare i potenziali effetti di carry over associati alla storia del microdosaggio. In particolare, sono stati eliminati i partecipanti che hanno riferito una pratica attiva di microdosaggio alla valutazione basale; abbiamo quindi confrontato i microdosatori che hanno iniziato la loro pratica dopo la valutazione basale e di follow-up con quelli che non hanno effettuato microdosaggi durante questo periodo. Per valutare la sovrapposizione, abbiamo seguito queste analisi con fino a tre serie di analisi supplementari nel gruppo dei microdosatori. Queste analisi supplementari sono state limitate agli esiti che hanno evidenziato un effetto microdose*tempo per evitare l'inflazione dell'errore di tipo I dovuto ai test multipli. Nella prima di queste analisi, imicrodosatori Psilocibina+HE sono stati confrontati con i microdosatori di sola Psilocibina. Una seconda serie di analisi ha confrontatoi microdosatori di Psilocibina+HE+B3 con quelli di sola Psilocibina. Come nelle analisi primarie, abbiamo esaminato anche gli effetti moderatori dell'età o delle preoccupazioni per la salute mentale. Nei casi in cui una di queste due analisi supplementari ha rilevato effetti significativi di interazione a due o tre vie, sono state seguite da un'analisi supplementare finale che ha confrontato imicrodosatori di Psilocibina+HE con quelli di Psilocibina+HE+B3. Le analisi del chi-quadro hanno valutato l'equivalenza dei sottogruppi in base all'età, ai giorni di microdose nell'ultimo mese e al dosaggio della microdose; le differenze in questi fattori sono state controllate tagliando a caso i partecipanti dal sottogruppo che risultava sproporzionatamente alto fino a quando le proporzioni dei gruppi non sono risultate statisticamente equivalenti45. La d di Cohen è stata calcolata per gli effetti per facilitare l'interpretazione e consentire il confronto delle dimensioni degli effetti tra i gruppi e con le ricerche precedenti (Tabella 2).
Tabella 2 Microdosatori contro non microdosatori in un mese.
Tabella a grandezza naturale
Le analisi preliminari hanno identificato le differenze attese in base all'età; il gruppo sotto i 55 anni ha dimostrato prestazioni superiori al gruppo 55+ in tutti i compiti cognitivi; per il Tap Test (media = 70,48 (33,18) contro 52,60 (29.99); t (1, 863) = 5,05, p< 0,01); per il PASAT (media = 33,67(14,21) contro 30,37 (12,92) t (1, 772) = 2,08, p< 0,05) e Spatial Span (media = 236,25 (51,02) contro 176,88 (58,80); t (1, 943) = 11,00, p< 0,01). Le differenze al basale per età sono state identificate per l'umore negativo (media = 46,89 (16,13) contro 40,64 (16,06); t (1, 1048) = 3,96, p< 0,01) ma non per l'umore positivo (media = 55% (16) contro 55,03% (15,01); t (1, 1048) = - 0,018, p= 0,99). Come previsto, i partecipanti che hanno riferito preoccupazioni per la salute mentale hanno ottenuto punteggi più elevati in tutte e tre le scale DASS: Depressione (media = 10.44 (9.72) contro 18.92 (12); t (1, 1010) = - 11.81, p< 0.01); Ansia (media = 6.38 (6.36) contro 11.38 (8.74); t (1, 1010) = - 0.018, p= 0.99). 38 (8,74); t (1, 1010) = 10,09, p< 0,01) e stress (media = 13,84 (9,1) contro 20,04 (9,8); t (1, 1010) = 9,61, p< 0,01). L'analisi del genere non ha rivelato alcun effetto principale del genere nel tempo in nessuno dei domini DASS (tutti F < 1,6, p> 0,20).
Figura 1
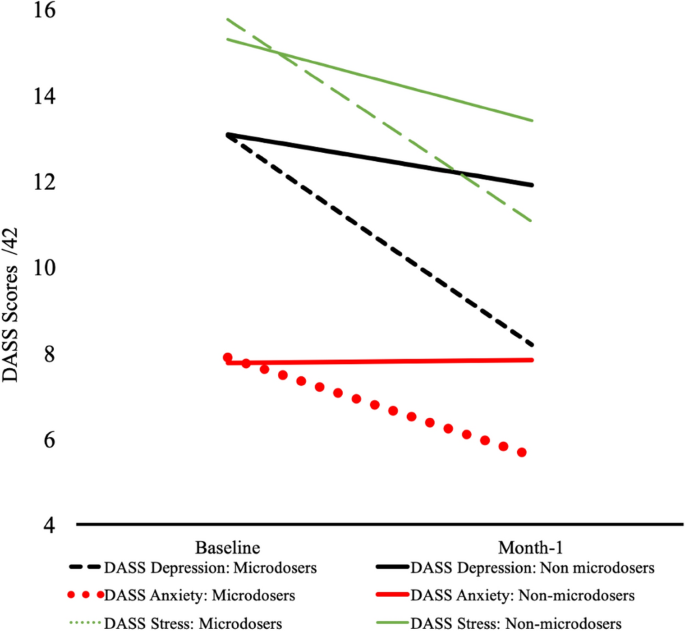
Microdosaggio e salute mentale. I valori "basali" riflettono le risposte medie dei partecipanti raccolte a 0-7 giorni dall'inizio dello studio. I valori del "mese 1" riflettono le risposte medie dei partecipanti raccolte 22-35 giorni dopo l'inizio dello studio.
Immagine a grandezza naturale
Le interazioni tra i gruppi di problemi di salute mentale e di microdosaggio non sono risultate significative per nessuno dei domini(tutti i FsMicrodose*Mental Health Concerns*Time < 1,16; p> 0,10), indicando che gli effetti principali del microdosaggio erano coerenti tra gli intervistati con e senza condizioni di salute mentale. Tra i microdosatori con problemi di salute mentale, i punteggi relativi alla depressione sono passati da 18,85 (12,03) al basale a 11,73 (9,85) al mese 1; per l'ansia, da 11,04 (8,48) al basale a 7,46 (6,68) al mese 1; e per lo stress, da 19,93 (9,71) al basale a 13,91 (9,02) al mese 1. Tra gli intervistati senza una storia di problemi di salute mentale, i punteggi relativi alla depressione sono passati da 10,40 (9,78) al basale a 6,65 (7,60) al Mese-1; per l'ansia, da 6,53 (6,50) al basale a 4,81 (5,57) al Mese-1; e per lo stress, da 13,96 (9,12) al basale a 9,78 (7,50) al Mese-1. Le analisi supplementari hanno confrontato le condizioni di impilamento sui cambiamenti nei punteggi di depressione, ansia e stress del DASS dal basale al mese-1. Non sono state rilevate differenze tra i microdosatori di sola psilocibina e imicrodosatori di psilocibina+HE (tutti F < 0,70; p> 0,10). Allo stesso modo, non sono state individuate differenze tra i microdosatori di sola psilocibina e imicrodosatori di psilocibina+HE+B3 (tutti F < 0,77; p> 0,10).
L'interazione tra età, stato della microdose e tempo non è risultata significativa né per l'umore positivo(F (1, 1058) = 0,21, b= - 0,05, p= 0,65) né per l'umore negativo(F (1, 1059) = 1,38, b= 0,13 p= 0,24), indicando l'equivalenza degli effetti sull'umore tra le diverse età. Le analisi di follow-up non hanno identificato differenze significative nei cambiamenti dell'umore positivo o negativo nel tempo tra i microdosatori di sola psilocibina e imicrodosatori di psilocibina+HE (tutti F < 0,52, p> 0,47) o imicrodosatori di psilocibina+HE+B3 (tutti F < 2,44, p> 0,12).
L'analisi dell'impilamento tra i microdosatori (Fig. 2) non ha rilevato alcuna interazione tra Psilocibina soltanto e Psilocibina+HE*Tempo, suggerendo che l'aggiunta di HE non ha influito sull'effetto della psilocibina sul tocco delle dita (F (1, 524) = 0,284, b= 0,12, p= 0,67). Al contrario, l'interazione solo psilocibina vs psilocibina+HE+B3*Tempo ha indicato un miglioramento relativamente maggiore nei punteggi di tocco con l'aggiunta di HE e B3 alla psilocibina (F (1, 732) = 3,93, b= - 0,51, p< 0,05). Questo risultato è stato seguito dall'esame dell'effetto moderatore dell'età, che ha identificato un'interazione Psilocibina solo vs Psilocibina+HE+B3 * Tempo * Età (F (1, 732) = 8,4, b= 0,6, p= 0,04), che riflette che l'aggiunta di HE e B3 ha avuto un impatto tra gli intervistati più anziani ma non tra quelli più giovani. Le analisi supplementari di Psilocibina+HE vs psilocibina+HE+B3 * Tempo hanno rivelato una tendenza alla significatività (F (1, 427) = 3,26, b= - 0,56, p= 0,07) e l'interazione a tre vie Psilocibina+HE vs psilocibina+HE+B3 *Tempo*Età è stata identificata (F (1, 427) = 6,71, b= 0,66, p= 0,01), indicando che gli effetti erano più pronunciati tra gli intervistati più anziani. Le analisi supplementari successive hanno indicato che questi risultati erano solidi dopo aver controllato le differenze tra i sottogruppi per quanto riguarda l'età, la frequenza delle microdosi e il dosaggio delle microdosi (tutte le interazioni a 3 vie Fs > 6,20, p< 0,05).
Figura 2
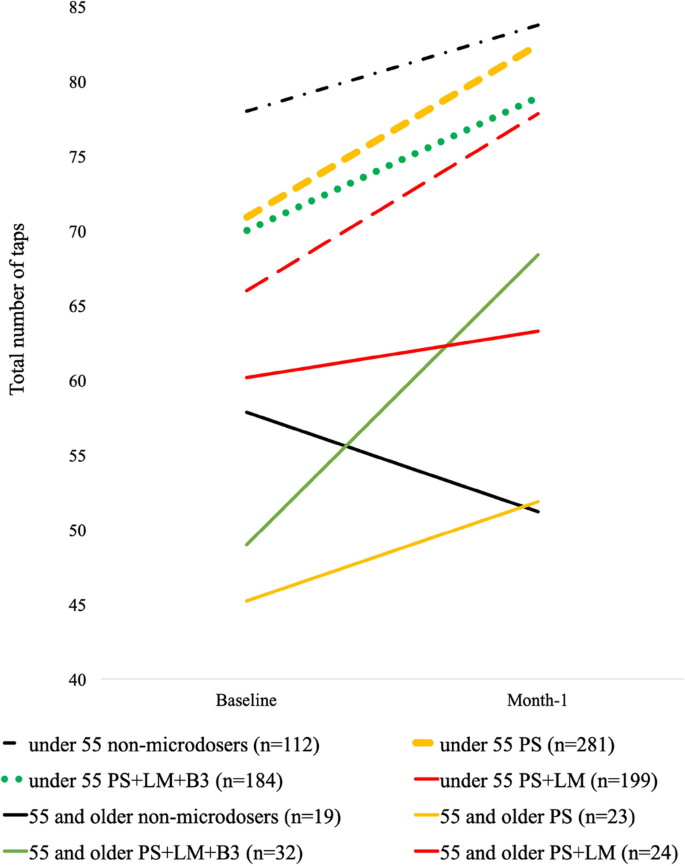
Punteggi del test di microdosaggio e Finger tap. I valori "Baseline" riflettono le risposte medie dei partecipanti raccolte a 0-7 giorni dall'inizio dello studio. I valori "Mese-1" riflettono le risposte medie dei partecipanti raccolte 22-35 giorni dopo l'inizio dello studio. PS si riferisce ai partecipanti che hanno effettuato microdosi di psilocibina in assenza di Lion's Mane (HE). PS + HE si riferisce ai partecipanti che hanno effettuato microdosaggi con psilocibina e HE in assenza di niacina (B3). PS + HE + B3 microdosatori si riferisce ai partecipanti che microdosano psilocibina con HE e B3. Le differenze nelle pendenze delle condizioni di gruppo sono state oggetto di analisi di interazione Microdose*Tempo.
Immagine a grandezza naturale
Il confronto tra i microdosatori e i non microdosatori per quanto riguarda i cambiamenti dal basale al mese 1 non ha indicato differenze né per il compito spaziale (F (1, 944) = 0,24, b= - 0,07, p= 0,63) né per il PASAT (F (1, 775) = 0,21, b= 0,02, p= 0,65). Alla luce di questa assenza di effetti principali, non sono state condotte analisi di follow-up.
Un potenziale contributo di future ricerche con disegni controllati con placebo sarebbe la capacità di disaggregare i contributi delle aspettative positive e degli effetti placebo. Sebbene l'uso di un gruppo di non microdosatori equivalente a quello dei microdosatori per quanto riguarda i dati demografici e l'impegno nelle procedure dello studio sia un chiaro punto di forza, sia i microdosatori che i non microdosatori nel nostro studio erano consapevoli del loro stato fin dall'inizio dello studio, rendendo impossibile escludere il contributo di maggiori aspettative nel gruppo dei microdosatori rispetto a quello dei non microdosatori. Tuttavia, in considerazione delle sfide associate alla conduzione di RCT nell'attuale ambiente normativo restrittivo e riconoscendo le sfide più ampie per un efficace accecamento di un farmaco di ricerca con effetti psicoattivi ben noti e distintivi, incoraggiamo la ricerca ad adottare una prospettiva più ampia sui presunti effetti placebo24. In particolare, la riconsiderazione clinica e lo studio degli psichedelici rappresentano un'opportunità per rivalutare la misura in cui le aspettative e i franchi effetti psicoattivi potrebbero combinarsi per influenzare il benessere soggettivo in modi potenzialmente significativi19.
L'impatto del microdosaggio sui test di funzionamento cognitivo e psicomotorio è stato misto e limitato alle prestazioni psicomotorie, senza alcun impatto apparente sulla memoria spaziale o sulla velocità di elaborazione. Inoltre, l'entità di questi effetti sembrava dipendere dall'età e dalla combinazione della psilocibina con HE e B3. Questa specificità per le prestazioni psicomotorie e la dipendenza dalla combinazione dei costituenti giustificano una cauta interpretazione, poiché la letteratura sul microdosaggio e le prestazioni cognitive è scarsa18 e nessuno studio precedente si è concentrato sulla combinazione della psilocibina con altre sostanze putativamente attive. In effetti, sebbene il nostro ampio campione abbia permesso un nuovo livello di granularità nell'esame delle pratiche distinte tra i sottogruppi di microdosatori legati all'età, questi gruppi erano comunque relativamente piccoli, il che aumenta la possibilità che i nostri risultati di facilitazione del test del rubinetto tra gli individui di età superiore ai 55 anni che microdosano la combinazione di psilocibina, HE e B3 possano essere anomali. Inoltre, a causa dell'esiguo numero di partecipanti che assumevano B3 senza psilocibina o HE, non avevamo la possibilità di indagare in che misura questi risultati fossero dovuti alla combinazione di psilocibina, B3 e HE, rispetto alla sola B3. Inoltre, l'età è stata raccolta in modo categorico e il cut-off di 55 anni è stato scelto per convenienza in base alla potenza; non siamo quindi in grado di determinare in che misura gli effetti osservati sarebbero stati mantenuti se fossero stati utilizzati altri cut score per l'età. Pertanto, è necessaria una replica prima di stimare le potenziali implicazioni cliniche. Tuttavia, se questi risultati dovessero rivelarsi solidi in campioni e sperimentatori diversi, potrebbero rappresentare un primo passo importante nello sviluppo di nuovi trattamenti per disturbi neurologici prevalenti e refrattari. Infine, sebbene questi risultati possano essere meglio descritti come suggestivi, aggiungono comunque un credito preliminare alle segnalazioni aneddotiche di benefici derivanti dalla combinazione specifica di psilocibina, HE e B330.
Oltre ai piccoli campioni nei sottogruppi, al disegno osservazionale e all'approccio generalmente esplorativo, l'interpretazione è ulteriormente limitata da potenziali bias di risposta legati all'autoselezione dei partecipanti e al reclutamento attraverso luoghi favorevoli all'uso di psichedelici, che potrebbero aver portato a una sovrarappresentazione nel nostro campione di individui che rispondono favorevolmente al microdosaggio. Inoltre, l'indisponibilità di una versione del sistema operativo Android dell'applicazione al momento dello studio ha limitato la partecipazione a coloro che avevano accesso a dispositivi Apple. Questo studio non ha inoltre analizzato l'influenza della dose e delle pratiche di dosaggio sugli esiti. Per affinare la comprensione dell'influenza di questi fattori chiave, saranno necessari studi futuri con disegni che consentano un'attenta valutazione della potenza, della composizione e della quantità dei materiali microdosati. Allo stesso modo, non sono stati valutati gli effetti avversi e le interazioni con i tipici antidepressivi e ansiolitici; tali dati saranno necessari per informare la nostra comprensione della sicurezza e dell'accettabilità del microdosaggio. Alla luce di queste limitazioni, incoraggiamo ricerche future che impieghino un approccio di reclutamento più sistematico e disegni che valutino il dosaggio ottimale, le migliori pratiche e gli effetti avversi associati al microdosaggio di psichedelici.
Joseph Rootman ha ricevuto finanziamenti per la ricerca da Quantified Citizen Technologies, un'azienda che produce software per la ricerca mobile decentralizzata che ha fornito la piattaforma di raccolta dati per questo studio. Maggie Kiraga è una dipendente di Quantified Citizen. Kalin Harvey è cofondatore e CTO di Quantified Citizen, cofondatore dello Psychedelic Data Project, cofondatore e direttore della Ketamine Assisted Therapy Association of Canada e investitore di MycoMedica Life Sciences. Pamela Kryskow è membro del comitato di consulenza clinica di Numinus Wellness, un'azienda che fornisce servizi di psicoterapia psichedelica. Per questo ruolo, Pamela Kryskow viene retribuita con azioni Numinus. È consulente volontaria di Nectara. È cofondatrice di MycoMedica Life Sciences e fa parte del comitato consultivo medico-scientifico. Paul Stamets è un investitore di Quantified Citizen, MycoMedica Life Sciences, PBC e possiede Fungi Perfecti, LLC che vende integratori Lion Mane. È richiedente di brevetti in corso che combinano funghi psilocibina, funghi Lion Mane e niacina. Eesmyal Santos-Brault è cofondatore e CEO di Quantified Citizen, cofondatore dello Psychedelic Data Project e investitore di MycoMedica Life Sciences. Kim PC Kuypers è ricercatore principale in progetti di ricerca, il presente studio non è incluso, sponsorizzati da Mindmed e Silopharma, aziende che stanno sviluppando farmaci psichedelici, ed è membro retribuito del comitato scientifico consultivo di Clerkenwell Health. Zach Walsh ha un rapporto di consulenza retribuita con Numinus Wellness e Entheotech BioMedical per quanto riguarda lo sviluppo medico degli psichedelici, ed è membro del comitato consultivo della Multidisciplinary Association for Psychedelic Studies (MAPS) Canada e di MycoMedica Life Sciences.
Astratto
Il microdosaggio di psilocibina comporta l'autosomministrazione ripetuta di funghi contenenti psilocibina a dosi sufficientemente piccole da non avere un impatto sul funzionamento regolare. Le pratiche di microdosaggio sono diverse e includono la combinazione della psilocibina con sostanze come i funghi della criniera del leone (Hericium erinaceus; HE) e la niacina (vitamina B3). L'adozione del microdosaggio da parte del pubblico ha superato l'evidenza, rendendo necessarie ulteriori ricerche prospettiche. Utilizzando un disegno naturalistico e osservazionale, abbiamo seguito i microdosatori di psilocibina(n= 953) e i comparatori non microdosatori(n= 180) per circa 30 giorni e abbiamo identificato miglioramenti di piccola o media entità nell'umore e nella salute mentale che erano generalmente coerenti tra i sessi, l'età e la presenza di problemi di salute mentale, nonché miglioramenti nelle prestazioni psicomotorie che erano specifici degli adulti più anziani. Le analisi supplementari hanno indicato che la combinazione di psilocibina con HE e B3 non ha avuto alcun impatto sui cambiamenti dell'umore e della salute mentale. Tuttavia, tra i microdosatori anziani la combinazione di psilocibina, HE e B3 è stata associata a miglioramenti psicomotori rispetto alla sola psilocibina e alla psilocibina e HE. I nostri risultati sui miglioramenti dell'umore e della salute mentale associati al microdosaggio di psilocibina si aggiungono agli studi precedenti sul microdosaggio di psichedelici grazie all'utilizzo di un gruppo di confronto e all'esame della coerenza degli effetti tra età, sesso e salute mentale. I risultati relativi alla combinazione di psilocibina, HE e B3 sono nuovi ed evidenziano la necessità di ulteriori ricerche per confermare e chiarire questi effetti apparenti.Introduzione
L'uso di funghi contenenti psilocibina per migliorare la salute e il benessere ha una lunga storia in diverse culture1. Dopo secoli di aggressiva soppressione coloniale, manifestatasi di recente nella "guerra alle droghe" condotta dagli Stati Uniti, la psilocibina è riemersa al di fuori dei suoi contesti indigeni tradizionali, come agente terapeutico per il trattamento delle malattie mentali e il miglioramento del benessere. In effetti, negli ultimi anni le discussioni sulle proprietà medicinali dei funghi psilocibinici sono proliferate nella cultura mainstream nordamericana ed europea2,3. Questo interesse si è concentrato prevalentemente su dosi sufficienti a generare drammatiche alterazioni della coscienza; tuttavia, anche l'uso di "microdosi" più piccole è diventato un argomento di grande interesse pubblico e scientifico4,5.Il microdosaggio prevede l'autosomministrazione regolare di sostanze psichedeliche in dosi sufficientemente piccole da non compromettere il normale funzionamento cognitivo6. Le sostanze più utilizzate per il microdosaggio sono i funghi psilocibinici e l'LSD, e in misura minore altre sostanze psichedeliche come la mescalina e la 2-CB7. Le indagini sul microdosaggio di psilocibina hanno individuato pratiche diverse, ma in generale convergono sull'autosomministrazione, da 3 a 5 volte alla settimana, di 0,1-0,3 g di funghi essiccati7,8,9,10,11,12. I miglioramenti dell'umore, del benessere emotivo e della cognizione sono stati segnalati tra le principali motivazioni per il microdosaggio13 e diversi studi trasversali hanno identificato associazioni tra il microdosaggio e i miglioramenti percepiti dell'umore13,14,15,16,17 e del funzionamento cognitivo10,11,16, la riduzione dello stress7, della depressione7,9,16 e dell'ansia7,9,14,18.
Sono relativamente pochi gli studi prospettici che hanno valutato il microdosaggio. Il primo studio longitudinale sul microdosaggio ha analizzato le valutazioni giornaliere di 98 microdosatori per 6 settimane e ha riscontrato miglioramenti transitori acuti in ampi domini del funzionamento psicologico nei giorni di microdosaggio e riduzioni dello stress, della depressione e della distraibilità dal basale alla conclusione dello studio. Inoltre, sebbene le conclusioni di questo studio siano limitate dalla mancanza di un gruppo di controllo non microdosatore, gli esami supplementari hanno concluso che gli effetti osservati non erano coerenti con quanto si sarebbe potuto prevedere sulla base delle aspettative comuni legate al microdosaggio7. Anche un successivo studio prospettico che ha seguito 81 microdosatori per quattro settimane ha riportato miglioramenti in diversi domini del benessere psicologico, tra cui una maggiore stabilità emotiva e una diminuzione di ansia e depressione. Tuttavia, analisi supplementari hanno suggerito che questi effetti positivi possono essere attribuiti alle aspettative e hanno evidenziato la necessità di ulteriori ricerche con partecipanti di controllo non microdosatori per distinguere meglio gli effetti del microdosaggio dagli effetti placebo e da altri fattori di confondimento longitudinali18.
L'uso efficace del placebo ha rappresentato una sfida nei pochi studi pubblicati che hanno tentato un disegno di questo tipo nel contesto del microdosaggio di psichedelici17,19,20. In particolare, uno studio prospettico sul microdosaggio che ha utilizzato un intervento di auto-accecamento per approssimare il controllo del placebo tra 191 partecipanti per 4 settimane ha identificato miglioramenti nel benessere emotivo tra i microdosatori, ma ha notato che la corretta identificazione della condizione è stata riportata dal 72% dei partecipanti, complicando la capacità di stimare in modo definitivo l'influenza degli effetti del placebo sui cambiamenti osservati. Analogamente, uno studio crossover in doppio cieco con controllo placebo su 30 intervistati seguiti per otto settimane ha identificato livelli più elevati di stupore auto-riferito in risposta alle esperienze estetiche tra i microdosatori rispetto ai controlli. Tuttavia, gli autori hanno riconosciuto i potenziali effetti confondenti della rottura del cieco, poiché due terzi dei partecipanti hanno indovinato accuratamente la loro condizione19. Un'ulteriore analisi dello stesso gruppo di partecipanti non ha individuato differenze nei sintomi di ansia e depressione tra i microdosatori rispetto al placebo20. Tuttavia, lo studio ha osservato che la precedente esperienza dei partecipanti con gli psichedelici, oltre ai bassi livelli di depressione e ansia, potrebbe aver attenuato gli effetti del microdosaggio. Inoltre, una percentuale significativa di partecipanti ha indovinato la propria condizione nella metà dei blocchi di prove, tuttavia gli effetti nulli apparenti dello studio possono rendere meno rilevante la potenziale influenza del placebo.
La rottura del cieco e la categoria più ampia degli effetti aspettativa o placebo sono sfide identificate per l'interpretazione degli studi sulle dosi regolari di psichedelici21 e possono complicare anche l'interpretazione della ricerca sul microdosaggio. Per esempio, lo studio longitudinale che ha tentato di aggiustare le aspettative controllando i punteggi di una misura modificata delle aspettative di microdosaggio18 ha notato che più dell'80% dei partecipanti ha riferito di aver avuto esperienze precedenti di uso di psichedelici, il che rende probabile che i punteggi della misura delle aspettative siano stati influenzati da esperienze passate di effetti diretti della droga. Le differenze individuali nella risposta alle droghe, dovute al metabolismo e a numerosi altri fattori, fanno sì che gli effetti farmacologici passati possano essere fortemente correlati con i successivi effetti farmacologici diretti e, pertanto, la parzializzazione (cioè il controllo per) delle aspettative può sottostimare gli effetti farmacologici diretti22,23. In sintesi, gli studi longitudinali esistenti hanno osservato effetti positivi associati al microdosaggio, ma non sono stati in grado di stimare con sicurezza i contributi farmacologici diretti a tali effetti. Più in generale, separare gli effetti diretti degli psichedelici da fattori indiretti come il set, il setting, le differenze individuali e le aspettative presenta sfide epistemologiche e pratiche, e lo studio degli psichedelici potrebbe essere meglio servito andando oltre l'enfasi potenzialmente procustea sul blinding e altri approcci per massimizzare il controllo24. Per esempio, l'esame naturalistico di ampie coorti offre potenti opportunità di esaminare la coerenza degli effetti tra i vari sottogruppi, e l'uso di un gruppo di confronto senza la premessa del cecità, ma con caratteristiche demografiche simili e livelli approssimativamente equivalenti di attività legate allo studio, consente di valutare l'impatto del microdosaggio in modo distinto dagli effetti indiretti come l'impegno nello studio, gli effetti della pratica, la regressione verso la media e altri potenziali artefatti comuni alla ricerca prospettica.
In concomitanza con l'aumento dell'interesse per il microdosaggio di funghi contenenti psilocibina, si registra un'accelerazione dell'interesse per altri funghi presumibilmente terapeutici. In particolare, la criniera di leone (Hericium erinaceus; HE) ha suscitato un notevole interesse per la sua proposta di trattamento della depressione25 e del lieve deterioramento cognitivo26 e per l'evidenza preclinica di una facilitazione della neurogenesi con implicazioni per il trattamento dei disturbi neurodegenerativi27,28. Recenti evidenze suggeriscono che alcuni microdosatori combinano la psilocibina con l'HE in un processo definito stacking8. Un'indagine trasversale su oltre 4.000 microdosatori, che ha utilizzato un campione parzialmente sovrapponibile a quello del presente studio, ha rilevato che oltre il 50% dei microdosatori di psilocibina combinava la psilocibina con diverse sostanze, e che l'HE era l'aggiunta più diffusa, seguita da una combinazione di niacina (vitamina-B3) e HE8. Poiché questo è l'unico studio che riporta lo stacking, la generalizzabilità di questi risultati è sconosciuta. La combinazione di HE, B3 e psilocibina è stata resa popolare nelle reti informali di informazione sul microdosaggio, sulla base dell'ipotesi che la B3 possa facilitare la biodisponibilità di psilocibina e HE attraverso la vasodilatazione29. È stato proposto che gli effetti salutari della psilocibina e dell'HE operino attraverso processi legati al BDNF, sollevando la possibilità di effetti super-additivi30,31. Tuttavia, i potenziali effetti della psilocibina e dell'HE, con e senza B3, non sono ancora stati studiati formalmente e la popolarità dell'accatastamento deriva probabilmente dalla sperimentazione autonoma e da rapporti aneddotici.
In sintesi, nonostante i risultati suggestivi e l'interesse crescente del pubblico, la letteratura empirica rimane equivoca sulle conseguenze del microdosaggio. Per valutare meglio le conseguenze sulla salute di questo fenomeno emergente sono necessarie ulteriori ricerche con gruppi di controllo e campioni ampi che consentano di esaminare potenziali moderatori come lo stato di salute mentale, l'età e il sesso. Nel presente studio, ci proponiamo di ampliare la letteratura esaminando i cambiamenti prospettici associati al microdosaggio di psilocibina rispetto a un gruppo di controllo non microdosatore su domini di salute mentale, umore e funzionamento cognitivo e psicomotorio. A nostra conoscenza, questo è il più grande studio prospettico finora condotto sul microdosaggio di psilocibina, il primo a distinguere tra le miscele di microdosaggio (cioè l'accatastamento) e tra i pochi studi prospettici a disaggregare sistematicamente le analisi in base all'età e ai problemi di salute mentale.
Metodi
Disegno e partecipanti
Abbiamo raccolto dati longitudinali tra novembre 2019 e maggio 2021 da intervistati autoselezionati (Tabella 1), tratti da uno studio più ampio sul microdosaggio di psichedelici. Il campione si sovrappone parzialmente a un campione molto più ampio descritto in un precedente studio trasversale8, ma aggiunge i partecipanti reclutati successivamente a quell'analisi ed esclude i partecipanti che non hanno completato la valutazione di follow-up a un mese e il cui microdosaggio non includeva la psilocibina. I materiali dello studio sono stati integrati in un'applicazione disponibile per gli utenti di Apple iOS32 che soddisfacevano i criteri di inclusione di avere almeno 18 anni, saper leggere in inglese e avere accesso a un dispositivo iOS. Sia i microdosatori che le persone che non praticano la pratica delle microdosi erano idonei a partecipare allo studio e sono stati reclutati simultaneamente attraverso i media relativi all'uso di psichedelici e attraverso le presentazioni agli eventi di ricerca e formazione sugli psichedelici.Tabella 1 Caratteristiche dei partecipanti.
Tabella a grandezza naturale
Lo studio consisteva in una valutazione di base completata all'inizio dello studio e in una valutazione di follow-up completata 22-35 giorni dopo; i programmi di valutazione erano equivalenti sia per i microdosatori che per i non microdosatori. Le valutazioni hanno riguardato le pratiche psichedeliche dell'ultimo mese, l'umore e la salute mentale e hanno presentato compiti di elaborazione cognitiva e psicomotoria. Ogni valutazione ha richiesto 20-30 minuti per essere completata, con una variabilità dovuta alla ramificazione, per cui molti elementi sono stati presentati solo a un sottoinsieme di partecipanti. Il consenso informato è stato ottenuto da tutti i partecipanti, lo studio è stato approvato dal Research Ethics Board dell'Università della British Columbia (H19-03051) e tutti i metodi sono stati eseguiti in conformità con le linee guida e i regolamenti. Le ipotesi e i risultati non sono stati pre-registrati.
I dati descrittivi sono riportati nella Tabella 1. L'età è stata valutata categoricamente e dicotomizzata in 55 anni e oltre e meno di 55 anni per valutare le potenziali differenze di gruppo, tenendo conto delle dimensioni del gruppo per mantenere la potenza statistica. La presenza di problemi di salute mentale è stata interrogata con l'item "Attualmente ha problemi psicologici, di salute mentale o di dipendenza?". L 'umore è stato valutato con la Positive And Negative Affect Schedule (PANAS)33, una misura self-report di 20 item con sottoscale di 10 item che valutano gli affetti positivi e negativi. A causa di un errore tecnico, è stato escluso un item della sottoscala negativa; per ovviare a questo inconveniente, i punteggi sono stati convertiti in percentuali. La depressione, l'ansia e lo stress sono stati misurati con la Depression Anxiety Stress Scale-21 (DASS-21)34, che presenta tre sottoscale con 7 item valutati su una scala a 4 punti. I compiti cognitivi e psicomotori sono stati adattati dall'Apple Research Kit, utilizzato e convalidato in diversi studi di grandi dimensioni35,36. L'abilità psicomotoria è stata misurata utilizzando una versione adattata del compito "finger tap "37, in cui i partecipanti hanno toccato due cerchi adiacenti sullo schermo di un dispositivo iOS in modo alternato per 10 s utilizzando l'indice e il medio della mano dominante. Protocolli simili di finger tap su smartphone hanno dimostrato una buona validità predittiva e discriminante per i disturbi neurodegenerativi37,38. La capacità di memoria spaziale è stata valutata con una versione adattata del compito Corsi Block-Tapping39, in cui i partecipanti ricordano la collocazione di stimoli su una griglia quadrata in una serie limitata di turni di difficoltà crescente40,41. Il criterio utilizzato in questo studio era il numero di risposte corrette. La velocità di elaborazione è stata valutata con un test adattato di addizione seriale uditiva (Paced Auditory Serial Addition Test, PASAT)42,43, che prevede la somma iterativa di numeri interi alternati; il criterio era il numero totale di risposte corrette.
Analisi statistiche
Sono stati generati modelli a effetti lineari misti per 8 risultati: depressione DASS, ansia DASS, stress DASS, PANAS positivo, PANAS negativo, numero di tocchi del finger tap test, punteggio dello span spaziale e punteggio PASAT. La modellazione multilivello è stata scelta per l'analisi per la sua capacità di testare simultaneamente le differenze tra e all'interno del gruppo, di incorporare osservazioni non equamente distanziate tra i partecipanti, come era comune nel presente studio, e per la sua robustezza all'inflazione dell'errore di tipo I derivante dai test multipli44. Tutti i modelli includevano l'effetto continuo del tempo (giorni dalla risposta al basale) e il fattore dicotomico del gruppo di microdosi(non microdosatori codificati come 0, microdosatori codificati come 1). Per costruire modelli parsimoniosi e mantenere sottogruppi di dimensioni adeguate, nei modelli è stato incluso un solo moderatore aggiuntivo. L'età è stata esaminata come moderatore per i test del funzionamento cognitivo e dell'umore, mentre data la sua rilevanza per i domini DASS di depressione, ansia e stress, la presenza di problemi di salute mentale è stata esaminata al posto dell'età come moderatore nei tre modelli che hanno esaminato i punteggi DASS. In particolare, l'età è stata inserita come variabile dicotomica tra le persone nei modelli con PANAS, finger tap, PASAT e span test, mentre i problemi di salute mentale sono stati inclusi nei modelli con i domini DASS.I modelli sono stati costruiti in modo che le variabili venissero mantenute se prevedevano l'esito del modello o erano un componente di un'interazione significativa di livello superiore. Per gli esiti in cui è stata identificata un'interazione Microdose*Tempo, sono stati costruiti modelli fattoriali completi che includevano l'interazione a tre vie Microdose*Tempo*Genere e Microdose*Tempo*Età o Microdose*Tempo*Preoccupazioni per la salute mentale e tutti gli effetti principali e di interazione a due vie di livello inferiore. Le analisi supplementari hanno eliminato le risposte anomale che superavano le due deviazioni standard dalla media del rispettivo gruppo. Una seconda serie di analisi supplementari ha escluso i partecipanti che hanno riferito di aver praticato il microdosaggio prima dell'inizio dello studio, per controllare i potenziali effetti di carry over associati alla storia del microdosaggio. In particolare, sono stati eliminati i partecipanti che hanno riferito una pratica attiva di microdosaggio alla valutazione basale; abbiamo quindi confrontato i microdosatori che hanno iniziato la loro pratica dopo la valutazione basale e di follow-up con quelli che non hanno effettuato microdosaggi durante questo periodo. Per valutare la sovrapposizione, abbiamo seguito queste analisi con fino a tre serie di analisi supplementari nel gruppo dei microdosatori. Queste analisi supplementari sono state limitate agli esiti che hanno evidenziato un effetto microdose*tempo per evitare l'inflazione dell'errore di tipo I dovuto ai test multipli. Nella prima di queste analisi, imicrodosatori Psilocibina+HE sono stati confrontati con i microdosatori di sola Psilocibina. Una seconda serie di analisi ha confrontatoi microdosatori di Psilocibina+HE+B3 con quelli di sola Psilocibina. Come nelle analisi primarie, abbiamo esaminato anche gli effetti moderatori dell'età o delle preoccupazioni per la salute mentale. Nei casi in cui una di queste due analisi supplementari ha rilevato effetti significativi di interazione a due o tre vie, sono state seguite da un'analisi supplementare finale che ha confrontato imicrodosatori di Psilocibina+HE con quelli di Psilocibina+HE+B3. Le analisi del chi-quadro hanno valutato l'equivalenza dei sottogruppi in base all'età, ai giorni di microdose nell'ultimo mese e al dosaggio della microdose; le differenze in questi fattori sono state controllate tagliando a caso i partecipanti dal sottogruppo che risultava sproporzionatamente alto fino a quando le proporzioni dei gruppi non sono risultate statisticamente equivalenti45. La d di Cohen è stata calcolata per gli effetti per facilitare l'interpretazione e consentire il confronto delle dimensioni degli effetti tra i gruppi e con le ricerche precedenti (Tabella 2).
Tabella 2 Microdosatori contro non microdosatori in un mese.
Tabella a grandezza naturale
Risultati
I microdosatori avevano maggiori probabilità rispetto ai non microdosatori di essere più anziani(x2(2, N = 1133) = 22,13, p< 0,01), di etnia bianca(x2(1, N = 1133) = 4,62, p= 0,03) e di dichiarare un'occupazione a tempo pieno.03) e di avere un'occupazione a tempo pieno(x2(3, N = 1122) = 11,83, p< 0,01); i gruppi erano equivalenti in tutti gli altri ambiti demografici (tuttigli x2< 6,03, tutti i p> 0,05; vedere Tabella 1). Il confronto tra i microdosatori del dosaggio e dei giorni di microdosaggio nell'ultimo mese non ha rilevato differenze in base all'età (giorni: x2(2, N = 953) = 3,37, p= 0,19; dose: x2(2, N = 953) = 3,31, p= 0,19) e ai problemi di salute mentale (giorni: x2(2, N = 931) = 0,71, p= 0,70; dose: x2(2, N = 931) = 0,21, p= 0,90).Le analisi preliminari hanno identificato le differenze attese in base all'età; il gruppo sotto i 55 anni ha dimostrato prestazioni superiori al gruppo 55+ in tutti i compiti cognitivi; per il Tap Test (media = 70,48 (33,18) contro 52,60 (29.99); t (1, 863) = 5,05, p< 0,01); per il PASAT (media = 33,67(14,21) contro 30,37 (12,92) t (1, 772) = 2,08, p< 0,05) e Spatial Span (media = 236,25 (51,02) contro 176,88 (58,80); t (1, 943) = 11,00, p< 0,01). Le differenze al basale per età sono state identificate per l'umore negativo (media = 46,89 (16,13) contro 40,64 (16,06); t (1, 1048) = 3,96, p< 0,01) ma non per l'umore positivo (media = 55% (16) contro 55,03% (15,01); t (1, 1048) = - 0,018, p= 0,99). Come previsto, i partecipanti che hanno riferito preoccupazioni per la salute mentale hanno ottenuto punteggi più elevati in tutte e tre le scale DASS: Depressione (media = 10.44 (9.72) contro 18.92 (12); t (1, 1010) = - 11.81, p< 0.01); Ansia (media = 6.38 (6.36) contro 11.38 (8.74); t (1, 1010) = - 0.018, p= 0.99). 38 (8,74); t (1, 1010) = 10,09, p< 0,01) e stress (media = 13,84 (9,1) contro 20,04 (9,8); t (1, 1010) = 9,61, p< 0,01). L'analisi del genere non ha rivelato alcun effetto principale del genere nel tempo in nessuno dei domini DASS (tutti F < 1,6, p> 0,20).
Depressione, ansia, stress
Il confronto tra i microdosatori e i non microdosatori per quanto riguarda il cambiamento dal basale al mese-1(microdose*tempo) ha indicato miglioramenti maggiori tra i microdosatori nei domini DASS della depressione(F (1, 1019) = 17.91, b= 0,12, p< 0,01), Ansia(F (1, 1017) = 18,33, b= 0,08, p< 0,01) e Stress(F (1, 1016) = 15,60, b= 0,08, p< 0,01) (Fig. 1; Tabella 2). Questi effetti sono rimasti coerenti dopo la rimozione di 124, 82 e 75 outlier nei domini Depressione, Ansia e Stress rispettivamente per punteggi superiori a 2 deviazioni standard dalla media(tutti i Microdose*time F > 7,99 p< 0,01) e in analisi parallele ristrette ai 594 partecipanti che non hanno riferito il microdosaggio prima del basale(tutti i Microdose*time F > 4,17, p< 0,05). Abbiamo identificato un'interazione Microdose*Gender*Time tale per cui l'effetto del microdosaggio nel tempo è risultato moderato dal genere nella depressione DASS . In particolare, le riduzioni della depressione legate al microdosaggio erano più forti tra le donne che tra i maschi(F (1, 1016) = 6,61, b= 0,17, p= 0,01). Non è stata identificata alcuna interazione microdose*genere*tempo per l'ansia DASS(F (1, 1024) = 1,14, b= 0,46, p= 0,29) o lo stress DASS(F (1, 1023) = 0,90, b= 0,05, p= 0,34).Figura 1

Microdosaggio e salute mentale. I valori "basali" riflettono le risposte medie dei partecipanti raccolte a 0-7 giorni dall'inizio dello studio. I valori del "mese 1" riflettono le risposte medie dei partecipanti raccolte 22-35 giorni dopo l'inizio dello studio.
Immagine a grandezza naturale
Le interazioni tra i gruppi di problemi di salute mentale e di microdosaggio non sono risultate significative per nessuno dei domini(tutti i FsMicrodose*Mental Health Concerns*Time < 1,16; p> 0,10), indicando che gli effetti principali del microdosaggio erano coerenti tra gli intervistati con e senza condizioni di salute mentale. Tra i microdosatori con problemi di salute mentale, i punteggi relativi alla depressione sono passati da 18,85 (12,03) al basale a 11,73 (9,85) al mese 1; per l'ansia, da 11,04 (8,48) al basale a 7,46 (6,68) al mese 1; e per lo stress, da 19,93 (9,71) al basale a 13,91 (9,02) al mese 1. Tra gli intervistati senza una storia di problemi di salute mentale, i punteggi relativi alla depressione sono passati da 10,40 (9,78) al basale a 6,65 (7,60) al Mese-1; per l'ansia, da 6,53 (6,50) al basale a 4,81 (5,57) al Mese-1; e per lo stress, da 13,96 (9,12) al basale a 9,78 (7,50) al Mese-1. Le analisi supplementari hanno confrontato le condizioni di impilamento sui cambiamenti nei punteggi di depressione, ansia e stress del DASS dal basale al mese-1. Non sono state rilevate differenze tra i microdosatori di sola psilocibina e imicrodosatori di psilocibina+HE (tutti F < 0,70; p> 0,10). Allo stesso modo, non sono state individuate differenze tra i microdosatori di sola psilocibina e imicrodosatori di psilocibina+HE+B3 (tutti F < 0,77; p> 0,10).
Umore
I risultati di entrambe le scale PANAS rispecchiano quelli della DASS. Rispetto ai non microdosatori, i microdosatori hanno mostrato maggiori aumenti dell'umore positivo dal basale al mese-1 (F (1, 1058) = 59,98, b= - 0,32, p< 0,01) e maggiori diminuzioni dell'umore negativo nel corso della durata dello studio (F (1, 1059) = 33,76, b= 0,23, p< 0,01). Questi effetti sono rimasti coerenti dopo la rimozione di 75 e 76 risposte anomale nei domini dell'umore positivo e negativo, rispettivamente, per i punteggi che superavano due deviazioni standard al di sopra o al di sotto della media(tutti i Microdose*time F > 26,32; p< 0,01), e tra i 479 partecipanti che stavano effettuando il microdosaggio al momento dell'inizio dello studio(tutti i Microdose*time F > 22,05; p< 0,01). Inoltre, le analisi dei moderatori hanno indicato che questi effetti sono rimasti stabili tra i sessi(tutti Microdose*Gender*Time F < 1,94; p> 0,05).L'interazione tra età, stato della microdose e tempo non è risultata significativa né per l'umore positivo(F (1, 1058) = 0,21, b= - 0,05, p= 0,65) né per l'umore negativo(F (1, 1059) = 1,38, b= 0,13 p= 0,24), indicando l'equivalenza degli effetti sull'umore tra le diverse età. Le analisi di follow-up non hanno identificato differenze significative nei cambiamenti dell'umore positivo o negativo nel tempo tra i microdosatori di sola psilocibina e imicrodosatori di psilocibina+HE (tutti F < 0,52, p> 0,47) o imicrodosatori di psilocibina+HE+B3 (tutti F < 2,44, p> 0,12).
Prestazioni psicomotorie e cognizione
Le analisi del test del tocco delle dita hanno identificato un effetto principale per il microdosaggio, per cui i microdosatori hanno dimostrato un cambiamento più positivo nelle prestazioni rispetto ai non microdosatori (F (1, 886) = 9,09, b= - 0,24, p= 0,03; Tabella 2). Le analisi supplementari non hanno rivelato un'interazione significativa a tre vie tra microdosaggio, genere e tempo, indicando che gli effetti del microdosaggio erano coerenti tra i generi(F= 0,26, b= 0,94, p= 0,61). L'effetto del microdosaggio sul punteggio del rubinetto nel tempo è stato robusto alla rimozione di 16 risposte anomale con punteggi di 2 deviazioni standard dalla media(Microdose*Time F= 7,23, b= - 0,21, p= 0,07), e gli effetti del trattamento sono rimasti coerenti quando il campione dello studio è stato limitato ai 515 partecipanti che non erano in microdosaggio al basale(Microdose*Time F= 5,07, b= 0,22, p= 0,03). Infine, l'interazione tra Microdose*Tempo*Età non è risultata significativa(F= 3,41, b= 0,43, p= 0,06), indicando che l'effetto del microdosaggio era coerente con l'età.L'analisi dell'impilamento tra i microdosatori (Fig. 2) non ha rilevato alcuna interazione tra Psilocibina soltanto e Psilocibina+HE*Tempo, suggerendo che l'aggiunta di HE non ha influito sull'effetto della psilocibina sul tocco delle dita (F (1, 524) = 0,284, b= 0,12, p= 0,67). Al contrario, l'interazione solo psilocibina vs psilocibina+HE+B3*Tempo ha indicato un miglioramento relativamente maggiore nei punteggi di tocco con l'aggiunta di HE e B3 alla psilocibina (F (1, 732) = 3,93, b= - 0,51, p< 0,05). Questo risultato è stato seguito dall'esame dell'effetto moderatore dell'età, che ha identificato un'interazione Psilocibina solo vs Psilocibina+HE+B3 * Tempo * Età (F (1, 732) = 8,4, b= 0,6, p= 0,04), che riflette che l'aggiunta di HE e B3 ha avuto un impatto tra gli intervistati più anziani ma non tra quelli più giovani. Le analisi supplementari di Psilocibina+HE vs psilocibina+HE+B3 * Tempo hanno rivelato una tendenza alla significatività (F (1, 427) = 3,26, b= - 0,56, p= 0,07) e l'interazione a tre vie Psilocibina+HE vs psilocibina+HE+B3 *Tempo*Età è stata identificata (F (1, 427) = 6,71, b= 0,66, p= 0,01), indicando che gli effetti erano più pronunciati tra gli intervistati più anziani. Le analisi supplementari successive hanno indicato che questi risultati erano solidi dopo aver controllato le differenze tra i sottogruppi per quanto riguarda l'età, la frequenza delle microdosi e il dosaggio delle microdosi (tutte le interazioni a 3 vie Fs > 6,20, p< 0,05).
Figura 2

Punteggi del test di microdosaggio e Finger tap. I valori "Baseline" riflettono le risposte medie dei partecipanti raccolte a 0-7 giorni dall'inizio dello studio. I valori "Mese-1" riflettono le risposte medie dei partecipanti raccolte 22-35 giorni dopo l'inizio dello studio. PS si riferisce ai partecipanti che hanno effettuato microdosi di psilocibina in assenza di Lion's Mane (HE). PS + HE si riferisce ai partecipanti che hanno effettuato microdosaggi con psilocibina e HE in assenza di niacina (B3). PS + HE + B3 microdosatori si riferisce ai partecipanti che microdosano psilocibina con HE e B3. Le differenze nelle pendenze delle condizioni di gruppo sono state oggetto di analisi di interazione Microdose*Tempo.
Immagine a grandezza naturale
Il confronto tra i microdosatori e i non microdosatori per quanto riguarda i cambiamenti dal basale al mese 1 non ha indicato differenze né per il compito spaziale (F (1, 944) = 0,24, b= - 0,07, p= 0,63) né per il PASAT (F (1, 775) = 0,21, b= 0,02, p= 0,65). Alla luce di questa assenza di effetti principali, non sono state condotte analisi di follow-up.
Discussione
I risultati di questo studio contribuiscono alla crescente letteratura sul microdosaggio in diversi modi. In primo luogo, sebbene il disegno del nostro studio differisca sostanzialmente da quello dei relativamente pochi studi longitudinali precedenti sul microdosaggio di psichedelici - in particolare per quanto riguarda i tentativi di tenere conto della potenziale influenza delle aspettative - i nostri risultati di miglioramento dell'umore e di riduzione dei sintomi della depressione, dell'ansia e dello stress sono comunque generalmente simili, per direzione e dimensione, agli effetti positivi medio-piccoli non aggiustati riportati in quelle ricerche7,17,18. A nostra conoscenza, questo è il più grande studio longitudinale finora condotto sul microdosaggio di psilocibina e uno dei pochi studi che ha coinvolto un gruppo di controllo17,18,19,20. Alla luce di questi punti di forza metodologici, la comparabilità dei nostri risultati con quelli di ricerche precedenti condotte in luoghi diversi e con metodologie differenti suggerisce un'associazione relativamente coerente tra microdosaggio e miglioramento della salute mentale. In particolare, il sottogruppo di intervistati che ha riferito problemi di salute mentale al momento della valutazione iniziale ha mostrato una riduzione media dei sintomi depressivi che ha portato a un passaggio da depressione moderata a lieve dopo circa 30 giorni di microdosaggio di psichedelici46. Considerando gli enormi costi sanitari e l'ubiquità della depressione, nonché la considerevole percentuale di pazienti che non rispondono ai trattamenti esistenti, il potenziale di un altro approccio per affrontare questo disturbo mortale merita una considerazione sostanziale. La possibilità che il microdosaggio di psilocibina possa fornire un mezzo per migliorare la depressione e l'ansia indica chiaramente la necessità di ulteriori ricerche per stabilire con maggiore certezza la natura della relazione tra il microdosaggio, l'umore e la salute mentale e la misura in cui questi effetti sono direttamente attribuibili alla psilocibina.Un potenziale contributo di future ricerche con disegni controllati con placebo sarebbe la capacità di disaggregare i contributi delle aspettative positive e degli effetti placebo. Sebbene l'uso di un gruppo di non microdosatori equivalente a quello dei microdosatori per quanto riguarda i dati demografici e l'impegno nelle procedure dello studio sia un chiaro punto di forza, sia i microdosatori che i non microdosatori nel nostro studio erano consapevoli del loro stato fin dall'inizio dello studio, rendendo impossibile escludere il contributo di maggiori aspettative nel gruppo dei microdosatori rispetto a quello dei non microdosatori. Tuttavia, in considerazione delle sfide associate alla conduzione di RCT nell'attuale ambiente normativo restrittivo e riconoscendo le sfide più ampie per un efficace accecamento di un farmaco di ricerca con effetti psicoattivi ben noti e distintivi, incoraggiamo la ricerca ad adottare una prospettiva più ampia sui presunti effetti placebo24. In particolare, la riconsiderazione clinica e lo studio degli psichedelici rappresentano un'opportunità per rivalutare la misura in cui le aspettative e i franchi effetti psicoattivi potrebbero combinarsi per influenzare il benessere soggettivo in modi potenzialmente significativi19.
L'impatto del microdosaggio sui test di funzionamento cognitivo e psicomotorio è stato misto e limitato alle prestazioni psicomotorie, senza alcun impatto apparente sulla memoria spaziale o sulla velocità di elaborazione. Inoltre, l'entità di questi effetti sembrava dipendere dall'età e dalla combinazione della psilocibina con HE e B3. Questa specificità per le prestazioni psicomotorie e la dipendenza dalla combinazione dei costituenti giustificano una cauta interpretazione, poiché la letteratura sul microdosaggio e le prestazioni cognitive è scarsa18 e nessuno studio precedente si è concentrato sulla combinazione della psilocibina con altre sostanze putativamente attive. In effetti, sebbene il nostro ampio campione abbia permesso un nuovo livello di granularità nell'esame delle pratiche distinte tra i sottogruppi di microdosatori legati all'età, questi gruppi erano comunque relativamente piccoli, il che aumenta la possibilità che i nostri risultati di facilitazione del test del rubinetto tra gli individui di età superiore ai 55 anni che microdosano la combinazione di psilocibina, HE e B3 possano essere anomali. Inoltre, a causa dell'esiguo numero di partecipanti che assumevano B3 senza psilocibina o HE, non avevamo la possibilità di indagare in che misura questi risultati fossero dovuti alla combinazione di psilocibina, B3 e HE, rispetto alla sola B3. Inoltre, l'età è stata raccolta in modo categorico e il cut-off di 55 anni è stato scelto per convenienza in base alla potenza; non siamo quindi in grado di determinare in che misura gli effetti osservati sarebbero stati mantenuti se fossero stati utilizzati altri cut score per l'età. Pertanto, è necessaria una replica prima di stimare le potenziali implicazioni cliniche. Tuttavia, se questi risultati dovessero rivelarsi solidi in campioni e sperimentatori diversi, potrebbero rappresentare un primo passo importante nello sviluppo di nuovi trattamenti per disturbi neurologici prevalenti e refrattari. Infine, sebbene questi risultati possano essere meglio descritti come suggestivi, aggiungono comunque un credito preliminare alle segnalazioni aneddotiche di benefici derivanti dalla combinazione specifica di psilocibina, HE e B330.
Oltre ai piccoli campioni nei sottogruppi, al disegno osservazionale e all'approccio generalmente esplorativo, l'interpretazione è ulteriormente limitata da potenziali bias di risposta legati all'autoselezione dei partecipanti e al reclutamento attraverso luoghi favorevoli all'uso di psichedelici, che potrebbero aver portato a una sovrarappresentazione nel nostro campione di individui che rispondono favorevolmente al microdosaggio. Inoltre, l'indisponibilità di una versione del sistema operativo Android dell'applicazione al momento dello studio ha limitato la partecipazione a coloro che avevano accesso a dispositivi Apple. Questo studio non ha inoltre analizzato l'influenza della dose e delle pratiche di dosaggio sugli esiti. Per affinare la comprensione dell'influenza di questi fattori chiave, saranno necessari studi futuri con disegni che consentano un'attenta valutazione della potenza, della composizione e della quantità dei materiali microdosati. Allo stesso modo, non sono stati valutati gli effetti avversi e le interazioni con i tipici antidepressivi e ansiolitici; tali dati saranno necessari per informare la nostra comprensione della sicurezza e dell'accettabilità del microdosaggio. Alla luce di queste limitazioni, incoraggiamo ricerche future che impieghino un approccio di reclutamento più sistematico e disegni che valutino il dosaggio ottimale, le migliori pratiche e gli effetti avversi associati al microdosaggio di psichedelici.
Riferimenti
- Carod-Artal, F. J. Hallucinogenic drugs in pre-Columbian Mesoamerican cultures (English edition). (Neurolia, 2015).
- Nye, B. C. Microdosing: Le persone che assumono LSD a colazione. BBC News. BBC News (2017). Disponibile all'indirizzo: https://www.bbc.com/news/health-39516345.
- Williams, A. Come l'LSD ha salvato il matrimonio di una donna. New York Times (2017).
- Fadiman, J. & Korb, S. Il microdosaggio di psichedelici potrebbe essere sicuro e benefico? Un'esplorazione iniziale. J. Psychoactive Drugs https://doi.org/10.1080/02791072.2019.1593561 (2019).
Articolo PubMed Google Scholar - Ona, G. & Bouso, J. C. Potenziale sicurezza, benefici e influenza dell'effetto placebo nel microdosaggio di sostanze psichedeliche: Una revisione sistematica. Neurosci. Biobehav. Rev. https://doi. org/10.1016/j.neubiorev.2020.09.035 (2020).
Articolo PubMed Google Scholar - Kuypers, K. P. C. et al. Microdosing psychedelics: Più domande che risposte? Una panoramica e suggerimenti per la ricerca futura. J. Psychopharmacol. https://doi.org/10.1177/0269881119857204 (2019).
Articolo PubMed PubMed Central Google Scholar - Polito, V. & Stevenson, R. J. Uno studio sistematico sul microdosaggio di psichedelici. PLoS ONE https://doi.org/10.1371/journal.pone.0211023 (2019).
Articolo PubMed PubMed Central Google Scholar - Rootman, J., Kryskow, P., Harvey, K., Stamets, P., Santos-Brauls, E., Kupers, K. P. C., Polito, V., Bourzat, F., & Walsh, Z. Gli adulti che microdosano psichedelici riportano motivazioni legate alla salute e livelli più bassi di ansia e depressione rispetto ai non microdosatori. Nature: Sci. Rep. https://doi. org/10.1038/s41598-021-01811-4 (2021).
- Cameron, L. P., Nazarian, A. & Olson, D. E. Psychedelic microdosing: Prevalenza ed effetti soggettivi. J. Psychoactive Drugs https://doi.org/10.1080/02791072.2020.1718250 (2020).
Articolo PubMed PubMed Central Google Scholar - Lea, T., Amada, N. & Jungaberle, H. Psychedelic microdosing: Un'analisi dei subreddit. J. Psychoactive Drugs https://doi.org/10.1080/02791072.2019.1683260 (2020).
Articolo PubMed Google Scholar - Rosenbaum, D. et al. Microdosing psychedelics: Demografia, pratiche e comorbidità psichiatriche. J. Psychopharmacol. https://doi.org/10.1177/0269881120908004 (2020).
Articolo PubMed Google Scholar - Hutten, N. R. P. W., Mason, N. L., Dolder, P. C. & Kuypers, K. P. C. Motivi ed effetti collaterali del microdosaggio di psichedelici tra i consumatori. Int. J. Neuropsychopharmacol. https://doi.org/10.1093/ijnp/pyz029 (2019).
Articolo PubMed PubMed Central Google Scholar - Anderson, T. et al. Microdosing psychedelics: Differenze di personalità, salute mentale e creatività nei microdosatori. Psychopharmacology https://doi.org/10.1007/s00213-018-5106-2 (2019).
Articolo PubMed Google Scholar - Lea, T. et al. Esiti percepiti del microdosaggio di psichedelici come terapia autogestita per i disturbi mentali e da uso di sostanze. Psychopharmacology https://doi.org/10.1007/s00213-020-05477-0 (2020).
Articolo PubMed Google Scholar - Johnstad, P. G. Sostanze potenti in piccole quantità: Uno studio di intervista sul microdosaggio di psichedelici. NAD Nord. Stud. Alcohol Drugs https://doi.org/10.1177/1455072517753339 (2018).
Articolo Google Scholar - Webb, M., Copes, H. & Hendricks, P. S. Narrative identity, rationality, and microdosing classic psychedelics. Int. J. Drug Policy https://doi.org/10.1016/j.drugpo.2019.04.013 (2019).
Articolo PubMed Google Scholar - Szigeti, B. et al. La citizen science auto-cieca per esplorare il microdosaggio di psichedelici. Elife 10, e62878. https://doi.org/10.7554/eLife.62878 (2021).
ArticoloCAS PubMed PubMed Central Google Scholar - Kaertner, L. S. et al. Le aspettative positive predicono il miglioramento dei risultati della salute mentale legati al microdosaggio di psichedelici. Sci. Rep. https://doi. org/10.1038/s41598-021-81446-7 (2021).
Articolo PubMed PubMed Central Google Scholar - Van Elk, M. et al. Effetti del microdosaggio di psilocibina sulle esperienze di stupore ed estetica: Uno studio preregistrato sul campo e in laboratorio. Psychopharmacology https://doi.org/10.1007/s00213-021-05857-0 (2021).
Articolo PubMed PubMed Central Google Scholar - Marschall, J. et al. Il microdosaggio di psilocibina non influisce sui sintomi e sull'elaborazione delle emozioni: Uno studio preregistrato sul campo e in laboratorio. J. Psychopharmacol. 36(1), 97 (2022).
Articolo Google Scholar - Muthukumaraswamy, S. D., Forsyth, A. & Lumley, T. Blinding and expectancy confounds in psychedelic randomized controlled trials. Expert. Rev. Clin. Pharmacol. https://doi.org/10.1080/17512433.2021.1933434 (2021).
Articolo PubMed Google Scholar - Sleep, C. E., Lynam, D. R., Hyatt, C. S. & Miller, J. D. Perils of partialing redux: The case of the dark triad. J. Abnorm. Psychol. https://doi.org/10.1037/abn0000278 (2017).
Articolo pubblicato Google Scholar - Lynam, D. R., Hoyle, R. H. & Newman, J. P. The perils of partialing: cautionary tales from aggression and psychopathy. Assessment 13(3), 328-341. https://doi.org/10.1177/1073191106290562 (2006).
Articolo PubMed PubMed Central Google Scholar - Schenberg, E. E. Chi è cieco nella ricerca psichedelica? Lettera all'editore riguardo a: confondimento del cieco e dell'aspettativa negli studi controllati randomizzati sugli psichedelici. Expert. Rev. Clin. Pharmacol. https://doi.org/10.1080/17512433.2021.1951473 (2021).
Articolo PubMed Google Scholar - Nagano, M. et al. Riduzione della depressione e dell'ansia con l'assunzione per 4 settimane di Hericium erinaceus. Biomed. Res. https://doi.org/10.2220/biomedres.31.231 (2010).
Articolo PubMed Google Scholar - Mori, K., Inatomi, S., Ouchi, K., Azumi, Yo. & Tuchida, T. Improving Effects of the Mushroom Yamabushitake on Mild Cognitiv Impairment. Zhongguo Zhong Yao Za Zhi (2009).
- Tsai-Teng, T. et al. Il micelio Hericium erinaceus arricchito di erinacina A migliora le patologie legate alla malattia di Alzheimer nei topi transgenici APPswe/PS1dE9. J. Biomed. Sci. https://doi.org/10.1186/s12929-016-0266-z (2016).
Articolo PubMed PubMed Central Google Scholar - Yang, P. P., Lin, C. Y., Lin, T. Y. & Chiang, W. C. Hericium erinaceus mycelium exerts neuroprotective in Parkinson's disease-in vitro and in vivo models. J. Drug Res. Dev. https://doi.org/10.16966/2470-1009.150 (2020).
Articolo Google Scholar - Stamets, P. I funghi psilocibinici e la micologia della coscienza. (Intervento su invito a Psychedelic Science, 2017).
- de Vos, C. M. H., Mason, N. L. & Kuypers, K. P. C. Psichedelici e neuroplasticità: Una revisione sistematica che svela le basi biologiche degli psichedelici. Front. Psychiatry https://doi.org/10.3389/fpsyt.2021.724606 (2021).
Articolo PubMed PubMed Central Google Scholar - Vigna, L. et al. L 'Hericium erinaceus migliora i disturbi dell'umore e del sonno in pazienti affetti da sovrappeso o obesità: Il pro-BDNF e il BDNF circolanti potrebbero essere potenziali biomarcatori? Evidence-based Complement. Altern. Med. https://doi.org/10.1155/2019/7861297 (2019).
Articolo Google Scholar - Quantified Citizen. Quantified Citizen (Versioni 1.1.-1.2.1.) [App mobile]. Apple App store. (2019). https://apps.apple.com/us/app/quantified-citizen/id1485884140
- Watson, D., Clark, L. A. & Tellegen, A. Sviluppo e validazione di brevi misure di affetti positivi e negativi: Le scale PANAS. J. Pers. Soc. Psychol. https://doi.org/10.1037//0022-3514.54.6.1063 (1988).
Articolo PubMed Google Scholar - Lovibond, P. F. & Lovibond, S. H. La struttura degli stati emotivi negativi: Confronto tra la Depression Anxiety Stress Scales (DASS) e i Beck Depression and Anxiety Inventories. Behav. Res. Ther. https://doi.org/10.1016/0005-7967(94)00075-U (1995).
Articolo PubMed Google Scholar - Bot, B. M. et al. Lo studio mPower, dati mobili sulla malattia di Parkinson raccolti con ResearchKit. Sci. Data https://doi.org/10.1038/sdata.2016.11 (2016).
Articolo PubMed PubMed Central Google Scholar - Zens, M., Woias, P., Suedkamp, N. P. & Niemeyer, P. "Back on track": Uno studio osservazionale su un'applicazione mobile utilizzando il framework researchkit di Apple. JMIR mHealth uHealth https://doi.org/10.2196/mhealth.6259 (2017).
Articolo PubMed PubMed Central Google Scholar - Lee, C. Y. et al. Uno studio di convalida di un'applicazione di finger tapping basata su smartphone per la valutazione quantitativa della bradicinesia nella malattia di Parkinson. PLoS ONE https://doi.org/10.1371/journal.pone.0158852 (2016).
Articolo PubMed PubMed Central Google Scholar - Boukhvalova, A. K. et al. Identificazione e quantificazione della disabilità neurologica tramite smartphone. Front. Neurol. https://doi.org/10.3389/fneur.2018.00740 (2018).
Articolo PubMed PubMed Central Google Scholar - Corsi, P. M. La memoria umana e la regione temporale mediale del cervello. Dissertatopm Abstracts International (1973).
- Farrell Pagulayan, K., Busch, R., Medina, K., Bartok, J. & Krikorian, R. Developmental normative data for the Corsi Block-Tapping task. J. Clin. Exp. Neuropsychol. https://doi.org/10.1080/13803390500350977 (2006).
Articolo PubMed Google Scholar - Brunetti, R., Del Gatto, C. & Delogu, F. eCorsi: implementazione e test del compito di Corsi block-tapping per tablet digitali. Front. Psychol. https://doi.org/10.3389/fpsyg.2014.00939 (2014).
Articolo PubMed PubMed Central Google Scholar - Gronwall, D., & Sampson, H. The Psychological Effects of Concussion. Auckland University Press, 1974.
- Tombaugh, T. N. Una revisione completa del Paced Auditory Serial Addition Test (PASAT). Arch. Clin. Neuropsychol. https://doi.org/10.1016/j.acn.2005.07.006 (2006).
Articolo PubMed Google Scholar - Gelman, A., Hill, J. & Yajima, M. Perché (di solito) non dobbiamo preoccuparci dei confronti multipli. J. Res. Educ. Eff. https://doi. org/10.1080/19345747.2011.618213 (2012).
Articolo Google Scholar - Rosenbaum, P. R. & Rubin, D. B. Reducing bias in observational studies using subclassification on the propensity score. J. Am. Stat. Assoc. https://doi.org/10.1080/01621459.1984 (1984).
Articolo Google Scholar - Lovibond, S. H. & Lovibond, P. F. Manual for the Depression Anxiety Stress Scales 2nd edn. (Psychology Foundation of Australia, 1995).
Google Scholar
Ringraziamenti
Desideriamo ringraziare Jim Fadiman per le sue consulenze su questo progetto e per il suo lavoro pionieristico sul microdosaggio in generale. Vorremmo anche riconoscere il supporto tecnico che abbiamo ricevuto dall'intero team di Quantified Citizen, in particolare gli sforzi di Delano Mandelbaum. Inoltre, apprezziamo la consulenza al progetto di Renee Davis, Zolton Bair e Chase Beathard di Fungi Perfecti. Infine, vorremmo riconoscere il sostegno finanziario dell'autore principale Joseph Rootman, attraverso una sovvenzione a cui hanno contribuito Mitacs e Quantified Citizen.Informazioni sull'autore
Autori e affiliazioni
- Dipartimento di Psicologia, University of British Columbia, Kelowna, BC, Canada
Joseph M. Rootman e Zach Walsh - Quantified Citizen Technologies Inc., Vancouver, BC, Canada
Maggie Kiraga, Kalin Harvey & Eesmyal Santos-Brault - Dipartimento di Medicina di famiglia, University of British Columbia, Vancouver, BC, Canada
Pamela Kryskow - Fungi Perfecti, LLC, MycoMedica Life Sciences, Olympia, WA, USA
Paul Stamets - Dipartimento di Neuropsicologia e Psicofarmacologia, Facoltà di Psicologia e Neuroscienze, Università di Maastricht, Maastricht, Paesi Bassi
Maggie Kiraga & Kim P. C. Kuypers
Contributi
J.R. ha progettato lo studio, analizzato i dati, scritto parzialmente la prima versione del manoscritto, creato le referenze e modificato il manoscritto. M.K. ha collaborato all'analisi dei dati, ha scritto parzialmente la prima versione del manoscritto e lo ha modificato. P.K. ha progettato lo studio, ha scritto parzialmente la prima versione del manoscritto e ne ha curato l'editing. K.H. ha progettato lo studio, orchestrato la raccolta dei dati, scritto parzialmente la prima versione del manoscritto e modificato il manoscritto. P.S. ha progettato lo studio, ha scritto parzialmente la prima versione del manoscritto e ne ha curato l'editing. E.S.B. ha progettato lo studio, orchestrato la raccolta dei dati, scritto parzialmente la prima versione del manoscritto e modificato il manoscritto. K.P.C.K. ha scritto parzialmente la prima versione del manoscritto e ne ha curato l'editing. Z.W ha progettato lo studio, ha scritto parzialmente la prima versione del manoscritto e ne ha curato l'editing.Autore corrispondente
Corrispondere a Joseph M. Rootman.Dichiarazioni etiche
Interessi contrastanti
Joseph Rootman ha ricevuto finanziamenti per la ricerca da Quantified Citizen Technologies, un'azienda che produce software per la ricerca mobile decentralizzata che ha fornito la piattaforma di raccolta dati per questo studio. Maggie Kiraga è una dipendente di Quantified Citizen. Kalin Harvey è cofondatore e CTO di Quantified Citizen, cofondatore dello Psychedelic Data Project, cofondatore e direttore della Ketamine Assisted Therapy Association of Canada e investitore di MycoMedica Life Sciences. Pamela Kryskow è membro del comitato di consulenza clinica di Numinus Wellness, un'azienda che fornisce servizi di psicoterapia psichedelica. Per questo ruolo, Pamela Kryskow viene retribuita con azioni Numinus. È consulente volontaria di Nectara. È cofondatrice di MycoMedica Life Sciences e fa parte del comitato consultivo medico-scientifico. Paul Stamets è un investitore di Quantified Citizen, MycoMedica Life Sciences, PBC e possiede Fungi Perfecti, LLC che vende integratori Lion Mane. È richiedente di brevetti in corso che combinano funghi psilocibina, funghi Lion Mane e niacina. Eesmyal Santos-Brault è cofondatore e CEO di Quantified Citizen, cofondatore dello Psychedelic Data Project e investitore di MycoMedica Life Sciences. Kim PC Kuypers è ricercatore principale in progetti di ricerca, il presente studio non è incluso, sponsorizzati da Mindmed e Silopharma, aziende che stanno sviluppando farmaci psichedelici, ed è membro retribuito del comitato scientifico consultivo di Clerkenwell Health. Zach Walsh ha un rapporto di consulenza retribuita con Numinus Wellness e Entheotech BioMedical per quanto riguarda lo sviluppo medico degli psichedelici, ed è membro del comitato consultivo della Multidisciplinary Association for Psychedelic Studies (MAPS) Canada e di MycoMedica Life Sciences.
