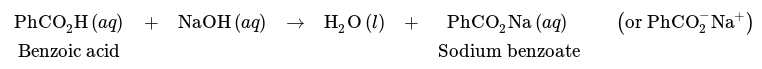G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,654
- Solutions
- 3
- Reaction score
- 2,732
- Points
- 113
- Deals
- 1
Extractie theorie.
"Extractie" verwijst naar de overdracht van verbinding(en) van een vaste stof of vloeistof naar een ander oplosmiddel of andere fase. Wanneer een theezakje aan heet water wordt toegevoegd, worden de bestanddelen die verantwoordelijk zijn voor de smaak en kleur van thee uit de theegrond in het water geëxtraheerd. Cafeïnevrije koffie wordt gemaakt door oplosmiddelen of superkritisch kooldioxide te gebruiken om de cafeïne uit koffiebonen te extraheren. In het scheikundelab wordt meestal vloeistof-vloeistof extractie gebruikt, een proces dat plaatsvindt in een scheitrechter. Een oplossing met opgeloste componenten wordt in de trechter geplaatst en een niet-mengbaar oplosmiddel wordt toegevoegd, wat resulteert in twee lagen die door elkaar worden geschud. Meestal is de ene laag waterig en de andere laag een organisch oplosmiddel. Componenten worden "geëxtraheerd" wanneer ze van de ene laag naar de andere bewegen. De vorm van de scheitrechter zorgt voor een efficiënte drainage en scheiding van de twee lagen.
Fig.1 Schematische weergave van extractie

Verbindingen bewegen van de ene vloeistof naar de andere afhankelijk van hun relatieve oplosbaarheid in elke vloeistof. Een snelle richtlijn voor de oplosbaarheid is het principe "zo lost het op", wat betekent dat apolaire verbindingen gemakkelijk geëxtraheerd worden in apolaire oplosmiddelen (en omgekeerd). De verbindingen die verantwoordelijk zijn voor de smaak en kleur van thee moeten polair zijn als ze gemakkelijk worden geëxtraheerd in heet water. Als je twee vloeistoffen in een scheitrechter laat equilibreren, komt het grootste deel van een verbinding vaak terecht in de laag waarin het beter oplosbaar is.
Fig.2

Stap-voor-stap procedures voor extracties.
Vloeistof-vloeistof extractie
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/threads/extraction.553/
Enkele extractie.
De afbeeldingen in dit gedeelte tonen een enkele extractie van methylrood (gekleurde verbinding, Fig. 3) uit een waterige oplossing (onderste laag) in 25 ml ethylacetaat (bovenste laag). De waterige oplossing heeft oorspronkelijk een roze kleur, omdat methylrood rood wordt in een zure oplossing (de waterige oplossing is gemaakt van 50 ml water, 5 druppels 0,1MHCl en 5 druppels 1% methylroodindicatoroplossing). Het methylrood heeft een grote verdelingscoëfficiënt en wordt in dit proces uit de waterige laag in het ethylacetaat geëxtraheerd.
Voortgang van de extractie van methylrood (de gekleurde verbinding) uit de zure waterige laag (onder) naar de organische laag (boven). Het omkeren gebeurde langzaam om de extractie stapsgewijs te zien. Zelfs bij voorzichtig mengen wordt het methylrood snel geëxtraheerd.


De opstelling voorbereiden (voor eenmalige extractie)
1. Pak een scheitrechter (fig. 4 a).- a) Als de scheitrechter een Teflon stopkraan heeft, zet de stopkraan dan weer in elkaar als hij gedemonteerd was om te drogen, en plaats de onderdelen in de juiste volgorde (Fig.4 b). Zorg ervoor dat de Teflon stopkraan matig strak zit zodat hij nog gemakkelijk kan draaien, maar niet zo los dat er vloeistof rond de verbinding kan sijpelen.
- b) Als je een glazen stopkraan gebruikt (Fig.4 c), hoeft deze waarschijnlijk niet verder voorbereid te worden. Er moet een heel dun laagje vet worden gebruikt om de kraan af te dichten en bevriezing te voorkomen. Als zowel glazen als teflon afsluitkranen beschikbaar zijn, is teflon een betere keuze, omdat er altijd een mogelijkheid is dat oplosmiddel het vet dat gebruikt wordt bij glazen afsluitkranen oplost en het monster verontreinigt.
- c) Zorg ook voor een stop (teflon of geslepen glas) die goed in de bovenste aansluiting van de trechter past (Fig.4 a).
2. Plaats de scheitrechter in een ringklem die bevestigd is aan een ringstatief of traliewerk. De trechters kunnen gemakkelijk breken, dus demp de trechter in de metalen klem met stukjes ingesneden rubber of plastic slang (Fig.4 d).
Voeg de oplossingen toe (voor eenmalige extractie)
3. Voordat je iets in een scheitrechter giet, moet je ervoor zorgen dat de stopkraan in de "gesloten" stand staat, waarbij de stopkraan horizontaal staat (Fig.5 a). Plaats als beveiliging altijd een erlenmeyer onder de scheitrechter voordat je gaat gieten (Fig.5 b). Deze kan vloeistof opvangen als de kraan per ongeluk open blijft staan, of als de kraan los zit en er onbedoeld vloeistof door lekt.
4. Giet de te extraheren vloeistof met behulp van een trechter in de scheitrechter (Fig.5 b). Een scheitrechter mag nooit gebruikt worden met een hete of warme vloeistof. Het geslepen glazen verbindingsstuk bovenop een scheitrechter zal eerder aan de stop blijven kleven als er op een bepaald moment vloeistof in het verbindingsstuk zat. Door vloeistof in de scheitrechter te gieten met een trechter met een korte steel wordt voorkomen dat de stop nat wordt, zodat deze minder snel bevriest tijdens het mengen.
3. Voordat je iets in een scheitrechter giet, moet je ervoor zorgen dat de stopkraan in de "gesloten" stand staat, waarbij de stopkraan horizontaal staat (Fig.5 a). Plaats als beveiliging altijd een erlenmeyer onder de scheitrechter voordat je gaat gieten (Fig.5 b). Deze kan vloeistof opvangen als de kraan per ongeluk open blijft staan, of als de kraan los zit en er onbedoeld vloeistof door lekt.
4. Giet de te extraheren vloeistof met behulp van een trechter in de scheitrechter (Fig.5 b). Een scheitrechter mag nooit gebruikt worden met een hete of warme vloeistof. Het geslepen glazen verbindingsstuk bovenop een scheitrechter zal eerder aan de stop blijven kleven als er op een bepaald moment vloeistof in het verbindingsstuk zat. Door vloeistof in de scheitrechter te gieten met een trechter met een korte steel wordt voorkomen dat de stop nat wordt, zodat deze minder snel bevriest tijdens het mengen.
Giet een hoeveelheid van het extractiemiddel in de scheitrechter, zoals aangegeven in de procedure (Fig.5 c). Het is niet nodig om precieze hoeveelheden oplosmiddel te gebruiken voor extracties, en de volumes kunnen worden afgemeten in een maatcilinder. Als een procedure vraagt om 20 ml oplosmiddel, is het acceptabel als er telkens 20-25 ml wordt gebruikt.
Meng de oplossingen (voor eenmalige extractie)
6. Plaats de stop op de trechter en houd de trechter zo vast dat de vingers van één hand de stop stevig omsluiten, terwijl de andere hand de bodem van de trechter vasthoudt (Fig.6 a).
7. 7. Keer de trechter voorzichtig om (fig. 6 b) en wervel het mengsel een beetje. Hoewel het niet ongewoon is dat er wat vloeistof in de geslepen glazen voeg kruipt wanneer deze wordt omgekeerd, zou dit minimaal moeten zijn. Als er vloeistof op je vingers of handschoenen druppelt wanneer je de trechter omkeert, is de stop waarschijnlijk de verkeerde maat.
Meng de oplossingen (voor eenmalige extractie)
6. Plaats de stop op de trechter en houd de trechter zo vast dat de vingers van één hand de stop stevig omsluiten, terwijl de andere hand de bodem van de trechter vasthoudt (Fig.6 a).
7. 7. Keer de trechter voorzichtig om (fig. 6 b) en wervel het mengsel een beetje. Hoewel het niet ongewoon is dat er wat vloeistof in de geslepen glazen voeg kruipt wanneer deze wordt omgekeerd, zou dit minimaal moeten zijn. Als er vloeistof op je vingers of handschoenen druppelt wanneer je de trechter omkeert, is de stop waarschijnlijk de verkeerde maat.
8. Onmiddellijk na het schudden en met de trechter nog steeds omgekeerd, "ontlucht" je de trechter door de afsluitkraan kort te openen om de druk te laten ontsnappen (fig. 6 c). De druk in de trechter neemt toe naarmate het oplosmiddel verdampt in de vrije ruimte en extra damp toevoegt aan de initiële luchtdruk van ∼1 atmosfeer in de trechter. Bij zeer vluchtige oplosmiddelen (zoals diethylether) is een duidelijke "swoosh" te horen bij het ontluchten, en kleine hoeveelheden vloeistof kunnen zelfs uit de afsluitkraan sputteren. Als er vloeistof uit de kraan spat, probeer deze dan terug te laten lopen in de trechter. Het geluid dat gepaard gaat met ontluchten houdt normaal gesproken op na de tweede of derde keer omkeren, omdat de vrije ruimte verzadigd raakt met oplosmiddeldampen en de druk binnen en buiten de trechter gelijk wordt.
Veiligheidsaanwijzing: Richt de kraan nooit op iemand terwijl je ontlucht, want het is mogelijk dat er vloeistof op hem of haar spat.
9. Sluit de kraan en meng de oplossingen een beetje krachtiger, waarbij je af en toe stopt om het systeem te ontluchten. Er zijn verschillende meningen over hoe krachtig oplossingen in scheitrechters gemengd moeten worden en hoe lang. In het algemeen zou 10-20 seconden zachtjes mengen voldoende moeten zijn. Bij sommige oplossingen (bijvoorbeeld dichloormethaan) moet ervoor worden gezorgd dat er niet te krachtig wordt geschud, omdat deze oplossingen vaak emulsies vormen (waarbij het grensvlak tussen de oplossingen niet helder wordt). Bij oplossingen die gevoelig zijn voor emulsies, moet een trechter gedurende een minuut zachtjes worden geschud.
10. Zet de scheitrechter rechtop in de ringklem om de lagen volledig te laten scheiden. Het grensvlak tussen de lagen moet vrij snel tot rust komen, vaak binnen ongeveer 10 seconden. Als het grensvlak troebel of niet goed gedefinieerd is (er heeft zich een emulsie gevormd), raadpleeg dan het gedeelte over het oplossen van problemen voor tips.
De lagen scheiden (voor eenmalige extractie)
11. Vloeistof loopt niet goed weg uit een scheitrechter als de stop erop blijft zitten, omdat er dan geen lucht in de trechter kan komen om de verplaatste vloeistof te vervangen. Als er wel vloeistof uit de trechter zou lopen zonder vervanging door een gelijke hoeveelheid lucht, zou er een negatieve druk in de trechter ontstaan. Verwijder dus de stop voordat je vloeistof uit een scheitrechter laat lopen (Fig.7 a).
12. Tap het grootste deel van de onderste laag af in een schone erlenmeyer en plaats de ringklem zo dat de punt van de scheitrechter in de erlenmeyer zit om spatten te voorkomen (fig.7 b). Stop het aftappen wanneer het scheidingsvlak zich binnen 1 cm van de bodem van de stopkraan bevindt.
13. Draai voorzichtig met de trechter om druppels die aan het glas vastzitten los te maken (fig. 7 c). Een glazen roerstaafje kan worden gebruikt om hardnekkig vastzittende druppels los te slaan.
14. Tap verder de onderste laag af en stop wanneer het grensvlak net in de stopkraankamer komt (fig. 7 d). Label de erlenmeyer (bijv. "onderste laag").
Veiligheidsaanwijzing: Richt de kraan nooit op iemand terwijl je ontlucht, want het is mogelijk dat er vloeistof op hem of haar spat.
9. Sluit de kraan en meng de oplossingen een beetje krachtiger, waarbij je af en toe stopt om het systeem te ontluchten. Er zijn verschillende meningen over hoe krachtig oplossingen in scheitrechters gemengd moeten worden en hoe lang. In het algemeen zou 10-20 seconden zachtjes mengen voldoende moeten zijn. Bij sommige oplossingen (bijvoorbeeld dichloormethaan) moet ervoor worden gezorgd dat er niet te krachtig wordt geschud, omdat deze oplossingen vaak emulsies vormen (waarbij het grensvlak tussen de oplossingen niet helder wordt). Bij oplossingen die gevoelig zijn voor emulsies, moet een trechter gedurende een minuut zachtjes worden geschud.
10. Zet de scheitrechter rechtop in de ringklem om de lagen volledig te laten scheiden. Het grensvlak tussen de lagen moet vrij snel tot rust komen, vaak binnen ongeveer 10 seconden. Als het grensvlak troebel of niet goed gedefinieerd is (er heeft zich een emulsie gevormd), raadpleeg dan het gedeelte over het oplossen van problemen voor tips.
De lagen scheiden (voor eenmalige extractie)
11. Vloeistof loopt niet goed weg uit een scheitrechter als de stop erop blijft zitten, omdat er dan geen lucht in de trechter kan komen om de verplaatste vloeistof te vervangen. Als er wel vloeistof uit de trechter zou lopen zonder vervanging door een gelijke hoeveelheid lucht, zou er een negatieve druk in de trechter ontstaan. Verwijder dus de stop voordat je vloeistof uit een scheitrechter laat lopen (Fig.7 a).
12. Tap het grootste deel van de onderste laag af in een schone erlenmeyer en plaats de ringklem zo dat de punt van de scheitrechter in de erlenmeyer zit om spatten te voorkomen (fig.7 b). Stop het aftappen wanneer het scheidingsvlak zich binnen 1 cm van de bodem van de stopkraan bevindt.
13. Draai voorzichtig met de trechter om druppels die aan het glas vastzitten los te maken (fig. 7 c). Een glazen roerstaafje kan worden gebruikt om hardnekkig vastzittende druppels los te slaan.
14. Tap verder de onderste laag af en stop wanneer het grensvlak net in de stopkraankamer komt (fig. 7 d). Label de erlenmeyer (bijv. "onderste laag").
15. Giet de bovenste laag uit de bovenkant van de scheitrechter in een andere schone erlenmeyer (fig.8 a) en zorg ervoor dat je deze erlenmeyer opnieuw labelt (fig.8 b). Het is de juiste techniek om de onderste laag af te tappen via de afsluitkraan en de bovenste laag uit te gieten via de bovenkant van de trechter. Deze methode minimaliseert het opnieuw mengen van de oplossingen, omdat alleen de onderste laag de steel van de trechter raakt.
16. Gooi nooit vloeistoffen van een extractie weg voordat je absoluut zeker weet dat je de gewenste verbinding hebt. Ongewenste lagen kunnen op de juiste manier worden weggegooid als je de gewenste verbinding in handen hebt (bijvoorbeeld nadat de rotatieverdamper het oplosmiddel heeft verwijderd).
Fouten gemaakt tijdens extracties (bijv. doorgaan met de verkeerde laag) kunnen worden opgelost zolang de oplossingen niet in de afvalcontainer zijn gedaan! De lagen moeten ook bewaard worden tot na de verdamping omdat de gewenste verbinding mogelijk niet goed oplosbaar is in het gebruikte oplosmiddel. Als de verbinding in het ene oplosmiddel niet wordt geëxtraheerd, kan later een ander oplosmiddel worden geprobeerd, maar alleen als de lagen nog niet zijn weggegooid.
Schoonmaken (voor eenmalige extractie)
Om een scheitrechter schoon te maken, spoel je hem eerst met aceton in een afvalcontainer. Was de trechter vervolgens met water en zeep op de werkbank. Demonteer de Teflon stopkraan (indien gebruikt). Laat de onderdelen na het spoelen met gedestilleerd water gescheiden drogen in je kastje (fig. 8 c).
Fouten gemaakt tijdens extracties (bijv. doorgaan met de verkeerde laag) kunnen worden opgelost zolang de oplossingen niet in de afvalcontainer zijn gedaan! De lagen moeten ook bewaard worden tot na de verdamping omdat de gewenste verbinding mogelijk niet goed oplosbaar is in het gebruikte oplosmiddel. Als de verbinding in het ene oplosmiddel niet wordt geëxtraheerd, kan later een ander oplosmiddel worden geprobeerd, maar alleen als de lagen nog niet zijn weggegooid.
Schoonmaken (voor eenmalige extractie)
Om een scheitrechter schoon te maken, spoel je hem eerst met aceton in een afvalcontainer. Was de trechter vervolgens met water en zeep op de werkbank. Demonteer de Teflon stopkraan (indien gebruikt). Laat de onderdelen na het spoelen met gedestilleerd water gescheiden drogen in je kastje (fig. 8 c).
Meerdere extracties.
In dit gedeelte staan stapsgewijze instructies over hoe je een waterige oplossing extraheert met een organisch oplosmiddel dat minder dicht is dan water (de organische laag komt bovenop). Als voorbeeld zijn de instructies geschreven om een waterige oplossing drie keer te extraheren met elke keer 25 ml diethylether (3×25 ml diethylether). Een procedurele samenvatting van de eerste twee extracties staat in Fig.9 Twee extracties als de organische laag bovenop ligt.
Extractie #1
1. Voer een enkele extractie uit met ongeveer 25 ml diethylether (een exacte hoeveelheid is niet nodig), zoals eerder beschreven, en zorg ervoor dat je elke laag op de juiste manier labelt (bijvoorbeeld "bovenste organische laag" en "onderste waterige laag").
Extractie #2
2. Breng de waterige laag terug naar de scheitrechter. Het is niet nodig om de trechter tussen de extracties door te wassen.
3. Voeg een nieuwe portie diethylether van 25 ml toe aan de scheitrechter. Sluit de trechter af, keer om en schud met ontluchten, en laat de lagen scheiden.
Bij deze stap moeten er twee lagen in de scheitrechter aanwezig zijn. Als er geen twee lagen zijn, is waarschijnlijk de verkeerde laag toegevoegd aan de trechter in stap 2 (een veelgemaakte fout). Een manier om te testen of dit de fout was, is door een beetje water uit een spuitflesje toe te voegen. Als de laag die in de scheitrechter is teruggebracht de organische laag is (onjuist), dan zal het water uit de spuitfles niet mengen met de oplossing en in plaats daarvan als druppels op de bodem vallen. Als de organische laag (onjuist) per ongeluk teruggestuurd is naar de scheitrechter, dan is er geen schade aangericht, omdat de organische laag gewoon verdund is. Giet de vloeistof terug in de kolf die bedoeld was voor de organische laag en voeg in plaats daarvan de waterige oplossing toe aan de trechter.
4. Giet de onderste waterige laag af in een erlenmeyer: het is acceptabel om dezelfde erlenmeyer te gebruiken die gebruikt is voor de waterige laag in de eerste extractie (die gelabeld kan zijn als "onderste waterige laag").
5. Aangezien het meestal gebruikelijk is om de organische lagen in meerdere extracties samen te voegen, kan de bovenste organische laag uit de scheitrechter in dezelfde kolf worden gegoten die gebruikt werd voor de organische laag in de eerste extractie (die gelabeld kan zijn als "bovenste organische laag"). In deze kolf moet ongeveer 50 ml diethylether van de twee extracties zitten.
Extractie #3
6. Herhaal de extractie een derde keer door de waterige laag van de tweede extractie toe te voegen aan de scheitrechter, gevolgd door nog een verse portie diethylether van 25 ml. Sluit de trechter af, keer om en schud met ontluchten, en laat de lagen scheiden.
7. Giet de waterige laag af in de daarvoor bestemde kolf en giet de bovenste laag opnieuw in de kolf met de organische laag, waar zich ongeveer 75 ml diethylether van de drie extracties zou moeten bevinden.
1. Voer een enkele extractie uit met ongeveer 25 ml diethylether (een exacte hoeveelheid is niet nodig), zoals eerder beschreven, en zorg ervoor dat je elke laag op de juiste manier labelt (bijvoorbeeld "bovenste organische laag" en "onderste waterige laag").
Extractie #2
2. Breng de waterige laag terug naar de scheitrechter. Het is niet nodig om de trechter tussen de extracties door te wassen.
3. Voeg een nieuwe portie diethylether van 25 ml toe aan de scheitrechter. Sluit de trechter af, keer om en schud met ontluchten, en laat de lagen scheiden.
Bij deze stap moeten er twee lagen in de scheitrechter aanwezig zijn. Als er geen twee lagen zijn, is waarschijnlijk de verkeerde laag toegevoegd aan de trechter in stap 2 (een veelgemaakte fout). Een manier om te testen of dit de fout was, is door een beetje water uit een spuitflesje toe te voegen. Als de laag die in de scheitrechter is teruggebracht de organische laag is (onjuist), dan zal het water uit de spuitfles niet mengen met de oplossing en in plaats daarvan als druppels op de bodem vallen. Als de organische laag (onjuist) per ongeluk teruggestuurd is naar de scheitrechter, dan is er geen schade aangericht, omdat de organische laag gewoon verdund is. Giet de vloeistof terug in de kolf die bedoeld was voor de organische laag en voeg in plaats daarvan de waterige oplossing toe aan de trechter.
4. Giet de onderste waterige laag af in een erlenmeyer: het is acceptabel om dezelfde erlenmeyer te gebruiken die gebruikt is voor de waterige laag in de eerste extractie (die gelabeld kan zijn als "onderste waterige laag").
5. Aangezien het meestal gebruikelijk is om de organische lagen in meerdere extracties samen te voegen, kan de bovenste organische laag uit de scheitrechter in dezelfde kolf worden gegoten die gebruikt werd voor de organische laag in de eerste extractie (die gelabeld kan zijn als "bovenste organische laag"). In deze kolf moet ongeveer 50 ml diethylether van de twee extracties zitten.
Extractie #3
6. Herhaal de extractie een derde keer door de waterige laag van de tweede extractie toe te voegen aan de scheitrechter, gevolgd door nog een verse portie diethylether van 25 ml. Sluit de trechter af, keer om en schud met ontluchten, en laat de lagen scheiden.
7. Giet de waterige laag af in de daarvoor bestemde kolf en giet de bovenste laag opnieuw in de kolf met de organische laag, waar zich ongeveer 75 ml diethylether van de drie extracties zou moeten bevinden.
Problemen oplossen.
In dit gedeelte worden veelvoorkomende problemen en oplossingen bij extracties beschreven.Er is maar één laag
De meest voorkomende reden voor het hebben van slechts één laag in een scheitrechter terwijl er twee zouden moeten zijn (zoals wanneer de procedure zegt dat je "de lagen moet scheiden"), is dat er een fout is gemaakt. Wat er waarschijnlijk gebeurd is, is dat de verkeerde laag is toegevoegd aan de scheitrechter - bijvoorbeeld de organische laag is onbewust toegevoegd in plaats van de waterige laag. Wanneer organisch oplosmiddel wordt toegevoegd aan een organische laag in de scheitrechter, is het resultaat slechts één laag. De fout kan hersteld worden zolang de lagen nog niet weggegooid zijn! Als de juiste laag aan de trechter wordt toegevoegd, werkt alles zoals gepland. Om deze fout in de toekomst te voorkomen, moet je de erlenmeyers labelen. Zorg er ook voor dat je nooit een laag weggooit voordat je absoluut zeker weet dat je alles goed hebt gedaan.
Een incidentele reden dat er slechts één laag wordt gevormd in een scheitrechter is als er grote hoeveelheden verbindingen aanwezig zijn die in beide oplosmiddelen oplossen, bijvoorbeeld als er grote hoeveelheden ethanol aanwezig zijn, die goed oplossen in zowel waterige als organische oplosmiddelen. In deze situatie is de beste aanpak om de lastige verbinding (d.w.z. de ethanol) vóór de extractie te verwijderen met een rotatieverdamper.
Er zijn drie lagen
De meest voorkomende reden voor drie lagen in een scheitrechter is onvoldoende menging (Fig.10 a). Als de trechter met meer kracht geschud wordt, zal het waarschijnlijk in twee lagen neerslaan (Fig.10 b). Het is ook mogelijk dat een middelste derde laag een emulsie is, waarbij de twee lagen niet volledig gescheiden zijn.
De meest voorkomende reden voor het hebben van slechts één laag in een scheitrechter terwijl er twee zouden moeten zijn (zoals wanneer de procedure zegt dat je "de lagen moet scheiden"), is dat er een fout is gemaakt. Wat er waarschijnlijk gebeurd is, is dat de verkeerde laag is toegevoegd aan de scheitrechter - bijvoorbeeld de organische laag is onbewust toegevoegd in plaats van de waterige laag. Wanneer organisch oplosmiddel wordt toegevoegd aan een organische laag in de scheitrechter, is het resultaat slechts één laag. De fout kan hersteld worden zolang de lagen nog niet weggegooid zijn! Als de juiste laag aan de trechter wordt toegevoegd, werkt alles zoals gepland. Om deze fout in de toekomst te voorkomen, moet je de erlenmeyers labelen. Zorg er ook voor dat je nooit een laag weggooit voordat je absoluut zeker weet dat je alles goed hebt gedaan.
Een incidentele reden dat er slechts één laag wordt gevormd in een scheitrechter is als er grote hoeveelheden verbindingen aanwezig zijn die in beide oplosmiddelen oplossen, bijvoorbeeld als er grote hoeveelheden ethanol aanwezig zijn, die goed oplossen in zowel waterige als organische oplosmiddelen. In deze situatie is de beste aanpak om de lastige verbinding (d.w.z. de ethanol) vóór de extractie te verwijderen met een rotatieverdamper.
Er zijn drie lagen
De meest voorkomende reden voor drie lagen in een scheitrechter is onvoldoende menging (Fig.10 a). Als de trechter met meer kracht geschud wordt, zal het waarschijnlijk in twee lagen neerslaan (Fig.10 b). Het is ook mogelijk dat een middelste derde laag een emulsie is, waarbij de twee lagen niet volledig gescheiden zijn.
Er is onoplosbaar materiaal op het grensvlak.
Een kleine hoeveelheid onoplosbare film tussen twee lagen is niet ongewoon tijdens een extractie. Polymere materialen hebben de neiging om tussen de lagen te rusten, omdat interacties tussen oplosmiddelen bij het grensvlak geminimaliseerd worden. Een kleine film is niet iets om je zorgen over te maken, want als een kleine hoeveelheid in de organische laag terechtkomt, zal een volgende droog- en filtratiestap deze vaak verwijderen.
Het grensvlak kan niet gezien worden.
Soms zijn de verbindingen in een scheitrechter zo donker dat ze het grensvlak tussen de twee lagen verbergen. Als dit gebeurt, zijn er verschillende methoden die je kunnen helpen om het grensvlak te zien. Een daarvan is om de scheitrechter tegen het licht te houden of met een zaklamp op het glas te schijnen (Fig.11 b). Met extra licht kun je soms het grensvlak zien. Een tweede methode is om de lagen zorgvuldig te observeren terwijl je de trechter heen en weer kantelt (Fig.11 c). Je oog kan soms subtiele verschillen opmerken in de manier waarop de vloeistoffen stromen. Een derde methode is om wat meer oplosmiddel aan de trechter toe te voegen om een van de lagen wat te verdunnen, of om een ander oplosmiddel toe te voegen om de brekingsindex te veranderen.
De lagen gaan niet goed uit elkaar (er vormt zich een emulsie)
Emulsies kunnen om verschillende redenen ontstaan.
1. De dichtheid van elke laag kan zo gelijk zijn dat er weinig motivatie is om de vloeistoffen te scheiden.2. Er kunnen zeepachtige verbindingen of andere emulgatoren aanwezig zijn die sommige componenten in elkaar oplossen.
Emulsies kunnen heel moeilijk te corrigeren zijn en het is het beste om ze in eerste instantie te vermijden door oplossingen die gevoelig zijn voor emulsies (bijv. dichloormethaan met sterk basische of dichte oplossingen) voorzichtig te schudden in de scheitrechter. Als er toch een emulsie ontstaat, zijn er enkele manieren om te proberen deze te verhelderen.
- a) Voor milde emulsies, zwenk de lagen voorzichtig rond en probeer zwevende druppels neer te slaan met een glazen roerstaaf.
- b) Laat de oplossing indien mogelijk enige tijd staan (zelfs tot de volgende labperiode). Met genoeg tijd bezinken sommige oplossingen vanzelf. Dit is natuurlijk niet altijd praktisch.
- c) Gebruik voor kleine volumes een centrifuge als die beschikbaar is. Een centrifuge versnelt het proces om een emulsie uit zichzelf te laten bezinken. Denk eraan dat een centrifuge in balans moet zijn, anders kan hij van het werkblad wiebelen. Verdeel de oplossingen gelijkmatig door buisjes van gelijk volume tegenover elkaar in de centrifuge te plaatsen.
- d) Als er een emulsie ontstaat omdat de twee lagen dezelfde dichtheid hebben, probeer dan de dichtheid van elke laag te veranderen om ze meer van elkaar te laten verschillen. Om een emulsie te verhelderen, probeer je de dichtheid van de bovenste laag te verlagen of de dichtheid van de onderste laag te verhogen. Als er bijvoorbeeld een emulsie ontstaat met ethylacetaat (bovenste laag) en een waterige oplossing (onderste laag), voeg dan wat NaCl toe. NaCl zal oplossen in de waterige laag en de dichtheid van de waterige oplossing verhogen. Je kunt ook wat ethylacetaat toevoegen, waardoor de organische laag verdund wordt en de dichtheid lager wordt. Als laatste redmiddel kan wat pentaan worden toegevoegd, dat zich mengt met de bovenste organische laag en de dichtheid ervan verlaagt (pentaan is een van de minst dichte organische oplosmiddelen). De toevoeging van pentaan wordt gebruikt als laatste poging, omdat het het vermogen van de organische laag om enigszins polaire verbindingen te extraheren negatief zal beïnvloeden.
Als er een emulsie ontstaat met een waterige oplossing (bovenste laag) en dichloormethaan (onderste laag), voeg dan wat water uit een spuitfles toe om de bovenste laag te verdunnen en de dichtheid ervan te verlagen. Deze methode werkte goed om de emulsie in Fig 13 c te verhelderen, zoals blijkt uit Fig 13 d. - c) Probeer de oplosbaarheid van het ene bestanddeel in het andere te verminderen. Een methode is om NaCl of NH4Cl toe te voegen aan de scheitrechter, dat oplost in de waterige laag en het vermogen van organische verbindingen om op te lossen in water vermindert ("uitzouten").
Zuur-base extractie
Zuur-base extractie
- G.Patton
- 2
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/threads/extraction.553/
Hoe ze werken.
Een aanpassing van de eerder in dit hoofdstuk besproken extracties is het uitvoeren van een chemische reactie in de scheitrechter om de polariteit en dus de verdeling van een verbinding in de waterige en organische lagen te veranderen. Een veelgebruikte methode is het uitvoeren van een zuur-basereactie, die sommige verbindingen kan omzetten van neutrale naar ionische vormen (of omgekeerd).
Stel je bijvoorbeeld voor dat een mengsel van benzoëzuur en cyclohexaan is opgelost in een organisch oplosmiddel zoals ethylacetaat in een scheitrechter. Om de componenten te scheiden, kan geprobeerd worden om benzoëzuur met water te verwijderen, maar benzoëzuur is niet bijzonder goed oplosbaar in water vanwege de apolaire aromatische ring, en er zouden slechts kleine hoeveelheden in de waterige laag worden geëxtraheerd (Fig.14 a).
Stel je bijvoorbeeld voor dat een mengsel van benzoëzuur en cyclohexaan is opgelost in een organisch oplosmiddel zoals ethylacetaat in een scheitrechter. Om de componenten te scheiden, kan geprobeerd worden om benzoëzuur met water te verwijderen, maar benzoëzuur is niet bijzonder goed oplosbaar in water vanwege de apolaire aromatische ring, en er zouden slechts kleine hoeveelheden in de waterige laag worden geëxtraheerd (Fig.14 a).
Scheiding van een mengsel van benzoëzuur en cyclohexaan is echter mogelijk met behulp van een spoeling met een base, zoals NaOH. Door zijn zure aard kan benzoëzuur als volgt reageren met NaOH, wat resulteert in het carboxylaatzout natriumbenzoaat.
De oplosbaarheidseigenschappen van carbonzuren verschillen aanzienlijk van hun overeenkomstige carboxylaatzouten. Natriumsalicylaat is ruwweg 350 keer beter oplosbaar in water dan salicylzuur vanwege het ionische karakter (Fig.15), en het is tamelijk onoplosbaar in organische oplosmiddelen zoals diethylether.
Daarom zou een spoeling met NaOH benzoëzuur omzetten in zijn ionische carboxylaatvorm, die dan beter oplosbaar zou zijn in de waterige laag, waardoor het natriumbenzoaat geëxtraheerd zou kunnen worden in de waterige laag. Cyclohexaan zou in de organische laag blijven omdat het geen affiniteit heeft voor de waterige fase en op geen enkele manier kan reageren met NaOH. Op deze manier kan een mengsel van benzoëzuur en cyclohexaan worden afgescheiden (Fig.14 b). De waterige laag kan later desgewenst worden aangezuurd met HCl(aq) om het benzoëzuur weer om te zetten in zijn neutrale vorm.
Wassen met natriumbicarbonaat
Een zuur-base extractie kan gebruikt worden om carbonzuren uit de organische laag in de waterige laag te extraheren. Zoals in het vorige gedeelte is besproken, kan NaOH worden gebruikt om een carbonzuur om te zetten in de meer wateroplosbare ionische carboxylaatvorm. Als het mengsel echter een gewenste verbinding bevat die met NaOH kan reageren, moet een mildere base zoals natriumbicarbonaat worden gebruikt. Er treedt een vergelijkbare reactie op.
Wassen met natriumbicarbonaat
Een zuur-base extractie kan gebruikt worden om carbonzuren uit de organische laag in de waterige laag te extraheren. Zoals in het vorige gedeelte is besproken, kan NaOH worden gebruikt om een carbonzuur om te zetten in de meer wateroplosbare ionische carboxylaatvorm. Als het mengsel echter een gewenste verbinding bevat die met NaOH kan reageren, moet een mildere base zoals natriumbicarbonaat worden gebruikt. Er treedt een vergelijkbare reactie op.
Een verschil bij het gebruik van de base NaHCO3 in plaats van NaOH is dat het bijproduct koolzuur (H2CO3) kan ontleden tot water en kooldioxidegas. Als je een zure oplossing met natriumbicarbonaat in een scheitrechter schudt, moet je voorzichtig zwenken en vaker ontluchten om de druk van het gas af te laten.
Een voorbeeld van een reactie waarbij vaak natriumbicarbonaat wordt gewassen is een Fischer veresteringsreactie. Ter demonstratie werd benzoëzuur samen met geconcentreerd zwavelzuur in ethanol refluxed om ethylbenzoaat te vormen (Fig.16 a en b). Een TLC-plaat van het reactiemengsel na 1 uur reflux toonde restanten van niet-gereageerd carbonzuur (Fig.16 c), wat niet ongewoon is vanwege de energie van de reactie.
Een voorbeeld van een reactie waarbij vaak natriumbicarbonaat wordt gewassen is een Fischer veresteringsreactie. Ter demonstratie werd benzoëzuur samen met geconcentreerd zwavelzuur in ethanol refluxed om ethylbenzoaat te vormen (Fig.16 a en b). Een TLC-plaat van het reactiemengsel na 1 uur reflux toonde restanten van niet-gereageerd carbonzuur (Fig.16 c), wat niet ongewoon is vanwege de energie van de reactie.
Het resterende carboxylzuur kan van het gewenste esterproduct worden verwijderd met behulp van een zuur-base-extractie in een scheitrechter. Een spoeling met natriumbicarbonaat zet benzoëzuur om in de meer wateroplosbare natriumbenzoaatvorm, waardoor het in de waterige laag wordt geëxtraheerd (fig. 17). Bovendien neutraliseert het natriumbicarbonaat het katalytische zuur in deze reactie.
Natriumbicarbonaat verdient de voorkeur boven NaOH in dit proces, omdat het een veel zwakkere base is; wassen met NaOH zou hydrolyse van het esterproduct kunnen veroorzaken.
Mengsels van zuren en basen
Zoals eerder besproken, kunnen de zuur-base eigenschappen van verbindingen gebruikt worden om selectief bepaalde verbindingen uit mengsels te extraheren. Deze strategie kan worden uitgebreid naar andere voorbeeldenMengsels van zuren en basen
Basen extraheren
Basische verbindingen zoals amines kunnen geëxtraheerd worden uit organische oplossingen door ze te schudden met zure oplossingen om ze om te zetten in beter in water oplosbare zouten. Op deze manier kunnen ze uit een organische laag in een waterige laag geëxtraheerd worden.Het extraheren van carbonzuren versus fenolen
Zoals eerder besproken, kunnen carbonzuren uit een organische laag geëxtraheerd worden in een waterige laag door ze te schudden met basische oplossingen, waardoor ze omgezet worden in hun beter in water oplosbare zouten.
Zoals eerder besproken, kunnen carbonzuren uit een organische laag geëxtraheerd worden in een waterige laag door ze te schudden met basische oplossingen, waardoor ze omgezet worden in hun beter in water oplosbare zouten.
Een vergelijkbare reactie vindt plaats met fenolen (PhOH), en ook deze kunnen worden geëxtraheerd in een waterige NaOH-laag (Fig.18 a).
Fenolen zijn echter aanzienlijk minder zuur dan carbonzuren en zijn niet zuur genoeg om volledig te reageren met NaHCO3, een zwakkere base. Daarom kan een oplossing van bicarbonaat worden gebruikt om mengsels van fenolen en carbonzuren te scheiden (Fig.18 b).
Fenolen zijn echter aanzienlijk minder zuur dan carbonzuren en zijn niet zuur genoeg om volledig te reageren met NaHCO3, een zwakkere base. Daarom kan een oplossing van bicarbonaat worden gebruikt om mengsels van fenolen en carbonzuren te scheiden (Fig.18 b).
Extractie van zure, basische en neutrale verbindingen
Met de zuur-base eigenschappen die eerder zijn besproken, kan een mengsel dat zure (bijv. RCO2H), basische (bijv. RNH2) en neutrale componenten bevat, worden gezuiverd door een reeks extracties, zoals samengevat in Fig.19 (waarbij een organisch oplosmiddel met een lagere dichtheid dan water wordt gebruikt).
Met de zuur-base eigenschappen die eerder zijn besproken, kan een mengsel dat zure (bijv. RCO2H), basische (bijv. RNH2) en neutrale componenten bevat, worden gezuiverd door een reeks extracties, zoals samengevat in Fig.19 (waarbij een organisch oplosmiddel met een lagere dichtheid dan water wordt gebruikt).
Er wordt aangenomen dat lezers die dit type experiment uitvoeren bekend zijn met het uitvoeren van enkelvoudige en meervoudige extracties. In dit gedeelte worden de verschillen beschreven tussen algemene extractieprocedures en het proces zoals samengevat in Fig. 19.
1. Het isoleren van de zure component:
a) Als de zure component zich in de waterige laag in een erlenmeyer bevindt, kan deze door toevoeging van 2M HCl(aq) weer worden omgezet in de neutrale component totdat de oplossing een pH van 3-4 geeft (zoals bepaald met pH-papier). Als er grote hoeveelheden zuur aanwezig zijn zodat aanzuren een te groot volume 2M HCl(aq) zou vereisen, dan kan geconcentreerd HCl(aq) druppelsgewijs toegevoegd worden. Lagere concentraties Hcl(aq) zijn minder gevaarlijk, maar als het volume van de waterige laag met een grote hoeveelheid wordt vergroot, heeft dit invloed op de efficiëntie van latere extracties en filterstappen.
b) Na aanzuren kunnen twee routes gevolgd worden, afhankelijk van of de zure component vast of vloeibaar is.
1. Het isoleren van de zure component:
a) Als de zure component zich in de waterige laag in een erlenmeyer bevindt, kan deze door toevoeging van 2M HCl(aq) weer worden omgezet in de neutrale component totdat de oplossing een pH van 3-4 geeft (zoals bepaald met pH-papier). Als er grote hoeveelheden zuur aanwezig zijn zodat aanzuren een te groot volume 2M HCl(aq) zou vereisen, dan kan geconcentreerd HCl(aq) druppelsgewijs toegevoegd worden. Lagere concentraties Hcl(aq) zijn minder gevaarlijk, maar als het volume van de waterige laag met een grote hoeveelheid wordt vergroot, heeft dit invloed op de efficiëntie van latere extracties en filterstappen.
b) Na aanzuren kunnen twee routes gevolgd worden, afhankelijk van of de zure component vast of vloeibaar is.
- Als zich na aanzuren van het ionische zout een vaste stof vormt, kan deze worden opgevangen door middel van zuigfiltratie. Deze methode moet alleen worden gebruikt als er grote hoeveelheden grote kristallen worden gezien. Als zich fijne kristallen vormen (wat vaak voorkomt), zullen deze het filterpapier verstoppen en een goede drainage verhinderen. Als er slechts een kleine hoeveelheid vaste stof wordt gezien in vergelijking met de theoretische hoeveelheid, dan is de verbinding waarschijnlijk goed oplosbaar in water en zou filtratie leiden tot een laag terugvindingspercentage.
- Als er geen vaste stof wordt gevormd bij aanzuren (of als er fijne kristallen of een kleine hoeveelheid vaste stof wordt gevormd), extraheer de zure component dan terug in een organisch oplosmiddel (×3). Gebruik als vuistregel een derde van de hoeveelheid oplosmiddel voor de extracties als de oorspronkelijke laag (bijv. bij gebruik van 100 ml waterige oplossing, extraheer met 33 ml organisch oplosmiddel per keer). Zorg ervoor dat je de waterige oplossing eerst afkoelt in een ijsbad voordat je gaat extraheren als de aanzuring merkbare hitte veroorzaakt. Was vervolgens met pekel (×1) als diethylether of ethylacetaat wordt gebruikt, droog met een droogmiddel en verwijder het oplosmiddel met een rotatieverdamper om de zuivere zure component over te houden.
2. De basische component isoleren:
Ga op dezelfde manier te werk als bij de isolatie van de zure component, maar baseer de oplossing met 2M NaOH(aq) totdat deze een pH van 9-10 geeft, zoals bepaald met pH-papier.
3. De neutrale component isoleren:
De neutrale component is de "overgebleven" verbinding in de organische laag. Om te isoleren, was je met pekel (×1) als je diethylether of ethylacetaat gebruikt, droog je met een droogmiddel en verwijder je het oplosmiddel met een rotatieverdamper om de pure neutrale component over te houden.
Ga op dezelfde manier te werk als bij de isolatie van de zure component, maar baseer de oplossing met 2M NaOH(aq) totdat deze een pH van 9-10 geeft, zoals bepaald met pH-papier.
3. De neutrale component isoleren:
De neutrale component is de "overgebleven" verbinding in de organische laag. Om te isoleren, was je met pekel (×1) als je diethylether of ethylacetaat gebruikt, droog je met een droogmiddel en verwijder je het oplosmiddel met een rotatieverdamper om de pure neutrale component over te houden.
Conclusie.
Extractiemethoden worden gebruikt om bepaalde stoffen uit een mengsel te extraheren. Deze stoffen kunnen basisch, zuur of neutraal (polair of apolair) zijn. Deze methode wordt bijvoorbeeld gebruikt tijdens de productie van amfetamine in de fase van decanteren: verzamel de bovenste laag met amfetamine base in alcohol. Het kan een beetje gedroogd worden met watervrij magnesiumsulfaat, en de slak kan extra geëxtraheerd worden met een apolair oplosmiddel (ether, benzeen, tolueen), het oplosmiddel wordt dan verdampt. De productie van mefedron omvat manipulatie met een scheitrechter en extractie. Zuur-base extractie wordt ook gebruikt om sommige psychoactieve stoffen te zuiveren van onzuiverheden.
Attachments
Last edited: