- Joined
- Apr 29, 2023
- Messages
- 78
- Reaction score
- 43
- Points
- 18
PPA HIPOFOSFOR I JOD = D AMFETAMINA LUB UŻYJ GO DO PRODUKCJI 4 METYLOAMINOREKSU
PodstawoweinformacjeBezpieczeństwoCenaUżyciePreparatyisurowceSpektrumPowiązane

ChemicalBook CAS DataBase List Phenylpropanolamine
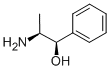
Fenylopropanolamina (PPA) jest aminą sympatykomimetyczną o mieszanym działaniu, podobną do efedryny. Jej podstawowym mechanizmem działania jest bezpośredni agonizm a-adrenergiczny, ale występuje również pośrednia stymulacja uwalniania noradrenaliny. W listopadzie 2000 r. Komitet Doradczy ds. Leków Bez Recepty Amerykańskiej Agencji ds. Żywności i Leków (FDA) ustalił, że istnieje znaczący związek między PPA a udarem krwotocznym i zalecił, aby PPA nie był uważany za bezpieczny do stosowania bez recepty. W tym czasie wystosowano pismo do producentów z prośbą o dobrowolne usunięcie PPA z ich produktów. Później, w 2005 roku, FDA opublikowała wstępną monografię końcową dla produktów zawierających PPA, proponując status kategorii II (nie jest ogólnie uznawany za bezpieczny i skuteczny). Do chwili obecnej nie wydano ostatecznej monografii, jednak wszyscy producenci usunęli PPA ze swoich produktów.
Producent
Propadrine, MSD, USA, 1941 r.
Zastosowanie
Norefedryna, zwana również fenylopropanolaminą (PPA), jest syntetyczną formą alkaloidu efedryny. Stosowana w leczeniu nietrzymania moczu u psów i kotów; środek udrożniający nos. Po doniesieniach o wystąpieniu krwotoku śródczaszkowego i innych działań niepożądanych, w tym kilku zgonów, PPA nie jest już sprzedawany w USA i Kanadzie.
Zastosowanie
Centralne podniecenie nerwowe
Zastosowanie
PPA był stosowany jako środek obkurczający nos i jako środek anorektyczny. Badania wykazały korzyści u ludzi w przypadku nietrzymania moczu, a PPA jest nadal stosowany w medycynie weterynaryjnej w tym celu.
Definicja
ChEBI: (-)-norefedryna jest amfetaminą, która jest propylobenzenem podstawionym grupą hydroksylową w pozycji 1 i grupą aminową w pozycji 2 (stereoizomer 1R,2S). Jest to alkaloid roślinny. Pełni rolę metabolitu roślinnego. Należy do amfetamin i alkaloidów fenetyloaminowych.
Proces produkcji
W jednym ze sposobów opisanych w patencie US 2,151,517, 10,7 kg technicznego benzaldehydu jest energicznie mieszane z roztworem 11,0 kg wodorosiarczynu sodu w 50,0 litrach wody, aż do zakończenia tworzenia się produktu addycji. Jednocześnie 8,25 kg nitroetanu rozpuszcza się w roztworze 4,5 kg sody kaustycznej w 20,0 litrach wody, a powstały ciepły roztwór dodaje się energicznie mieszając do magmy wodorosiarczynu sodu benzaldehydu. Mieszaninę miesza się przez 30 minut, a następnie pozostawia na noc.
Wodna część mieszaniny jest teraz odsysana z warstwy supernatantu oleistego fenylnitropropanolu i zastępowana świeżym roztworem 11,0 kg wodorosiarczynu sodu w 50,0 litrach wody. Mieszanina fenylnitropropanolu i roztworu wodorosiarczynu jest teraz energicznie mieszana przez 15 minut w celu usunięcia i odzyskania niewielkich ilości nieprzereagowanego benzaldehydu, a następnie ponownie pozostawia się do rozwarstwienia. Tym razem fenylnitropropanol jest odsysany i filtrowany w celu usunięcia niewielkiej ilości materiału żywicznego. Pozostały wodny roztwór wodorosiarczynu sodu poddaje się reakcji z benzaldehydem, jak opisano powyżej, dzięki czemu proces jest ciągły.
Otrzymany w ten sposób 1-fenylo-2-nitropropanol jest bezbarwnym olejem o ciężarze właściwym 1,14 w temperaturze 20°C, bezwonnym w stanie czystym, lotnym z parą wodną i wrzącym w temperaturze od 150°C do 165°C pod ciśnieniem 5 mm słupa rtęci. Jest rozpuszczalny w alkoholu, eterze, acetonie, chloroformie, czterochlorku węgla, benzenie i lodowatym kwasie octowym. Wydajność 1-fenylo-2-nitropropanolu otrzymanego w tej procedurze wynosi od 17,1 do 17,7 kg.
Jest on uwodorniany i przekształcany w chlorowodorek w kolejnych etapach. Chlorowodór ma temperaturę topnienia 192°-194°C.
W alternatywnej drodze opisanej w patencie US 3,028,429 propiofenon może być poddany reakcji z azotynem alkilu w celu otrzymania izonitrozopropiofenonu, który jest następnie uwodorniany i ostatecznie przekształcany w chlorowodorek.
nazwa handlowa
Np.multix;Acutrim;Adistop-f;Amertuss;Amplisiex;Am-tuss liq;Anorexin;Antiadipositum;Apoephedrin;e Aridose;Arm;Bifed-20;Biphetane;Biphetap;Blu-hist;Brocon cr;Bromanate;Bromepaph;Brometapp;Bronco-chintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat;Dalca;Decidex;Decomine;Demazine;Deprecstop;Dexatrim;D-sinus;Efed ii;Eficol;Endal;Endecon;Endex;E-son;Espornade spansule;E-tapp 3;Exyphen;Factus;Fornagest;Fugoa n;Gardax;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nektatussin;Neosoldana;Nexaam;Nobese;Norephedrine;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel tabletki;Rinutan;Rotabromofen;Rupton;Rynatapp;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Funkcja terapeutyczna
Lek zmniejszający przekrwienie błony śluzowej nosa, anoreksja
Światowa Organizacja Zdrowia (WHO)
Fenylopropanolamina, amina sympatykomimetyczna, jest szeroko dostępna w preparatach dostępnych bez recepty od 1941 roku. Jest jednym z najczęściej stosowanych leków udrożniających nos i jest powszechnym składnikiem preparatów do redukcji masy ciała, chociaż pojawiły się wątpliwości co do jej przydatności w tym wskazaniu. Jest również stosowany w wysiłkowym nietrzymaniu moczu. Jego stosowanie wiązało się z okazjonalnym nadmiernym wzrostem ciśnienia krwi, zwłaszcza u osób nadwrażliwych.
Opis ogólny
Fenylopropanolamina jest N-desmetylanalogiem efedryny, a zatem ma wiele podobnych właściwości. Brak grupy N-metylowej powoduje, że fenylopropanolamina jest nieco bardziej polarna, a zatem nie dostaje się do OUN tak dobrze jak efedryna. Ta modyfikacja daje środek, który ma nieco wyższe działanie wazopresyjne i niższe centralne działanie stymulujące niż efedryna. Jego działanie jako środka udrożniającego nos jest bardziej długotrwałe niż działanie efedryny. Fenylopropanolamina była powszechnym aktywnym składnikiem leków hamujących apetyt oraz leków na kaszel i przeziębienieOTC do 2001 r., kiedy to Agencja Żywności i Leków (FDA) zaleciła jej usunięcie z takich leków, ponieważ badania wykazały zwiększone ryzyko udaru krwotocznego u młodych kobiet, które przyjmowały lek.
Profil bezpieczeństwa
Umiarkowanie toksyczny podskórnie. Po podgrzaniu do rozkładu emituje bardzo toksyczne opary NOx.
Ocena toksyczności
Podstawowym działaniem PPA jest bezpośredni agonizm a-adrenergiczny, chociaż powoduje on również pośrednie uwalnianie noradrenaliny w pozazwojowych zakończeniach nerwów współczulnych. PPA ma również słabe właściwości agonistyczne β. Nadciśnienie tętnicze wynika ze zwężenia naczyń krwionośnych obwodowych, w którym pośredniczą receptory α-adrenergiczne. Często występuje odruchowa bradykardia. Działanie sympatykomimetyczne może wywoływać niepokój, bezsenność, pobudzenie, drżenie, tachykardię i rozszerzenie źrenic.
MSDS|CAS|Baza danych|Noweprodukty
Skontaktuj się znami|Wersjakomputerowa
Książka chemiczna
PodstawoweinformacjeBezpieczeństwoCenaUżyciePreparatyisurowceSpektrumPowiązane

ChemicalBook CAS DataBase List Phenylpropanolamine

Fenylopropanolamina
- Nazwa produktu Fenylopropanolamina
- CAS14838-15-4
- Numer CBNCB22131029
- MFC9H13NO
- MW151.21
- EINECS238-900-2
- MOL File14838-15-4.mol
Właściwości chemiczne
| Temperatura topnienia | 101-101.5° |
| Temperatura wrzenia | 273,23°C (przybliżona) |
| Gęstość | 1,0406 (przybliżona) |
| Współczynnik załamania światła | 1,5380 (wartość szacunkowa) |
| pka | pKa 9.19(H2O,t=25±0.5,I=0.01)(w przybliżeniu) |
| kolor | Płytki z H2O |
| FDA UNII | 33RU150WUN |
| NIST Chemistry Reference | Benzenemethanol, «alpha»-(1-aminoethyl)-, (r*,s*)-(.+/-.)-(14838-15-4) |
| Kod ATC | R01BA01,R01BA51 |
| System rejestracji substancji EPA | Phenylpropanolamine (14838-15-4) |
Bezpieczeństwo
| Dane dotyczące substancji niebezpiecznych | 14838-15-4(Dane dotyczące substancji niebezpiecznych) |
| Toksyczność | LD50 scu-rat: 850 mg/kg JPETAB 85,199,45 |
Cena fenylopropanolaminy
Fenylopropanolamina Właściwości chemiczne, zastosowanie, produkcja
OpisFenylopropanolamina (PPA) jest aminą sympatykomimetyczną o mieszanym działaniu, podobną do efedryny. Jej podstawowym mechanizmem działania jest bezpośredni agonizm a-adrenergiczny, ale występuje również pośrednia stymulacja uwalniania noradrenaliny. W listopadzie 2000 r. Komitet Doradczy ds. Leków Bez Recepty Amerykańskiej Agencji ds. Żywności i Leków (FDA) ustalił, że istnieje znaczący związek między PPA a udarem krwotocznym i zalecił, aby PPA nie był uważany za bezpieczny do stosowania bez recepty. W tym czasie wystosowano pismo do producentów z prośbą o dobrowolne usunięcie PPA z ich produktów. Później, w 2005 roku, FDA opublikowała wstępną monografię końcową dla produktów zawierających PPA, proponując status kategorii II (nie jest ogólnie uznawany za bezpieczny i skuteczny). Do chwili obecnej nie wydano ostatecznej monografii, jednak wszyscy producenci usunęli PPA ze swoich produktów.
Producent
Propadrine, MSD, USA, 1941 r.
Zastosowanie
Norefedryna, zwana również fenylopropanolaminą (PPA), jest syntetyczną formą alkaloidu efedryny. Stosowana w leczeniu nietrzymania moczu u psów i kotów; środek udrożniający nos. Po doniesieniach o wystąpieniu krwotoku śródczaszkowego i innych działań niepożądanych, w tym kilku zgonów, PPA nie jest już sprzedawany w USA i Kanadzie.
Zastosowanie
Centralne podniecenie nerwowe
Zastosowanie
PPA był stosowany jako środek obkurczający nos i jako środek anorektyczny. Badania wykazały korzyści u ludzi w przypadku nietrzymania moczu, a PPA jest nadal stosowany w medycynie weterynaryjnej w tym celu.
Definicja
ChEBI: (-)-norefedryna jest amfetaminą, która jest propylobenzenem podstawionym grupą hydroksylową w pozycji 1 i grupą aminową w pozycji 2 (stereoizomer 1R,2S). Jest to alkaloid roślinny. Pełni rolę metabolitu roślinnego. Należy do amfetamin i alkaloidów fenetyloaminowych.
Proces produkcji
W jednym ze sposobów opisanych w patencie US 2,151,517, 10,7 kg technicznego benzaldehydu jest energicznie mieszane z roztworem 11,0 kg wodorosiarczynu sodu w 50,0 litrach wody, aż do zakończenia tworzenia się produktu addycji. Jednocześnie 8,25 kg nitroetanu rozpuszcza się w roztworze 4,5 kg sody kaustycznej w 20,0 litrach wody, a powstały ciepły roztwór dodaje się energicznie mieszając do magmy wodorosiarczynu sodu benzaldehydu. Mieszaninę miesza się przez 30 minut, a następnie pozostawia na noc.
Wodna część mieszaniny jest teraz odsysana z warstwy supernatantu oleistego fenylnitropropanolu i zastępowana świeżym roztworem 11,0 kg wodorosiarczynu sodu w 50,0 litrach wody. Mieszanina fenylnitropropanolu i roztworu wodorosiarczynu jest teraz energicznie mieszana przez 15 minut w celu usunięcia i odzyskania niewielkich ilości nieprzereagowanego benzaldehydu, a następnie ponownie pozostawia się do rozwarstwienia. Tym razem fenylnitropropanol jest odsysany i filtrowany w celu usunięcia niewielkiej ilości materiału żywicznego. Pozostały wodny roztwór wodorosiarczynu sodu poddaje się reakcji z benzaldehydem, jak opisano powyżej, dzięki czemu proces jest ciągły.
Otrzymany w ten sposób 1-fenylo-2-nitropropanol jest bezbarwnym olejem o ciężarze właściwym 1,14 w temperaturze 20°C, bezwonnym w stanie czystym, lotnym z parą wodną i wrzącym w temperaturze od 150°C do 165°C pod ciśnieniem 5 mm słupa rtęci. Jest rozpuszczalny w alkoholu, eterze, acetonie, chloroformie, czterochlorku węgla, benzenie i lodowatym kwasie octowym. Wydajność 1-fenylo-2-nitropropanolu otrzymanego w tej procedurze wynosi od 17,1 do 17,7 kg.
Jest on uwodorniany i przekształcany w chlorowodorek w kolejnych etapach. Chlorowodór ma temperaturę topnienia 192°-194°C.
W alternatywnej drodze opisanej w patencie US 3,028,429 propiofenon może być poddany reakcji z azotynem alkilu w celu otrzymania izonitrozopropiofenonu, który jest następnie uwodorniany i ostatecznie przekształcany w chlorowodorek.
nazwa handlowa
Np.multix;Acutrim;Adistop-f;Amertuss;Amplisiex;Am-tuss liq;Anorexin;Antiadipositum;Apoephedrin;e Aridose;Arm;Bifed-20;Biphetane;Biphetap;Blu-hist;Brocon cr;Bromanate;Bromepaph;Brometapp;Bronco-chintoxil;Cenadex;Chlor-rest;Cinturex;Cletanol;Codimal;Cofpac;Cold cap;Coldecon;Col-decon;Conex-grippe;Contop;Coricidin f;Corsym;Coryztime;Cremacoat;Dalca;Decidex;Decomine;Demazine;Deprecstop;Dexatrim;D-sinus;Efed ii;Eficol;Endal;Endecon;Endex;E-son;Espornade spansule;E-tapp 3;Exyphen;Factus;Fornagest;Fugoa n;Gardax;Ginsopan;Headway;Histade;Histatapp;Hsp 540;Ipercron;Kol-tac;Kontexin;Koryza;Leder;Lipo-sinahist;Lunerin;Mardram;Minus-x;Monatuss;Mucolyt-expecto;Nd-hist;Nektatussin;Neosoldana;Nexaam;Nobese;Norephedrine;Nornatane;Ornacol;Ornatos;Ornex;Pabron nose;Panacorn;Panadyl;Parhist;Partapp;Pholcolix spansule;Pneumidex;Polcimut;Profenade;Propagest;Reduzin;Rhindecon;Rhinergal;Rhinervert;Rhinicept;Rhinidrin;Rhinocap;Rinexin;Rinomar;Rinotussal;Rinurel lictus;Rinurel tabletki;Rinutan;Rotabromofen;Rupton;Rynatapp;Rynex;Ryza-gesic;Sacietyl;Scotuss;Secron;Sinacin;Sinudan;Sinu-lets;Sinutab cough l;Spandecon;Srda;Sto-caps;Sulfa-probocon;Symptrol;Taviset;Tinaroc;Totolin;Tricon;Tri-congestic;Triogesic elixir;Triominic;Triotussic;Turbispan;Tussilene-dm;V cold;Veltane;Veltap;Vernate;Vistaminic;Voxin-pg;W 58;X 112 antiadipo;Zerinol;Partuss;Permatrim;Phenapap.
Funkcja terapeutyczna
Lek zmniejszający przekrwienie błony śluzowej nosa, anoreksja
Światowa Organizacja Zdrowia (WHO)
Fenylopropanolamina, amina sympatykomimetyczna, jest szeroko dostępna w preparatach dostępnych bez recepty od 1941 roku. Jest jednym z najczęściej stosowanych leków udrożniających nos i jest powszechnym składnikiem preparatów do redukcji masy ciała, chociaż pojawiły się wątpliwości co do jej przydatności w tym wskazaniu. Jest również stosowany w wysiłkowym nietrzymaniu moczu. Jego stosowanie wiązało się z okazjonalnym nadmiernym wzrostem ciśnienia krwi, zwłaszcza u osób nadwrażliwych.
Opis ogólny
Fenylopropanolamina jest N-desmetylanalogiem efedryny, a zatem ma wiele podobnych właściwości. Brak grupy N-metylowej powoduje, że fenylopropanolamina jest nieco bardziej polarna, a zatem nie dostaje się do OUN tak dobrze jak efedryna. Ta modyfikacja daje środek, który ma nieco wyższe działanie wazopresyjne i niższe centralne działanie stymulujące niż efedryna. Jego działanie jako środka udrożniającego nos jest bardziej długotrwałe niż działanie efedryny. Fenylopropanolamina była powszechnym aktywnym składnikiem leków hamujących apetyt oraz leków na kaszel i przeziębienieOTC do 2001 r., kiedy to Agencja Żywności i Leków (FDA) zaleciła jej usunięcie z takich leków, ponieważ badania wykazały zwiększone ryzyko udaru krwotocznego u młodych kobiet, które przyjmowały lek.
Profil bezpieczeństwa
Umiarkowanie toksyczny podskórnie. Po podgrzaniu do rozkładu emituje bardzo toksyczne opary NOx.
Ocena toksyczności
Podstawowym działaniem PPA jest bezpośredni agonizm a-adrenergiczny, chociaż powoduje on również pośrednie uwalnianie noradrenaliny w pozazwojowych zakończeniach nerwów współczulnych. PPA ma również słabe właściwości agonistyczne β. Nadciśnienie tętnicze wynika ze zwężenia naczyń krwionośnych obwodowych, w którym pośredniczą receptory α-adrenergiczne. Często występuje odruchowa bradykardia. Działanie sympatykomimetyczne może wywoływać niepokój, bezsenność, pobudzenie, drżenie, tachykardię i rozszerzenie źrenic.
Preparaty i surowce
SurowceSpektrum fenylopropanolaminy
14838-15-4, fenylopropanolaminaPowiązane wyszukiwanie
Wyślij zapytanieMSDS|CAS|Baza danych|Noweprodukty
Skontaktuj się znami|Wersjakomputerowa
Książka chemiczna
