2C-B
4-BROMO-2,5-DIMETOXIFENETILAMINA
SÍNTESE: Uma solução de 100 g de 2,5-dimetoxibenzaldeído em 220 g de nitrometano foi tratada com 10 g de acetato de amônio anidro e aquecida em um banho de vapor por 2,5 h com agitação ocasional. A mistura de reação vermelho-escura foi removida do excesso de nitrometano sob vácuo, e o resíduo cristalizou espontaneamente. Esse nitrostyrene bruto foi purificado por moagem sob IPA, filtragem e secagem ao ar, para produzir 85 g de 2,5-dimetoxi-beta-nitrostyrene como um produto amarelo-alaranjado de pureza adequada para a próxima etapa. A purificação adicional pode ser obtida por recristalização a partir de IPA em ebulição.
Em um balão de fundo redondo de 2 L equipado com um agitador magnético e colocado sob uma atmosfera inerte, foram adicionados 750 mL de THF anidro, contendo 30 g de LAH. Em seguida, foram adicionados, em solução de THF, 60 g de 2,5-dimetoxi-beta-nitrostyrene. A solução final tinha uma cor marrom-amarelada suja e foi mantida em temperatura de refluxo por 24 h. Após o resfriamento, o excesso de hidreto foi destruído pela adição gota a gota de IPA. Em seguida, 30 mL de NaOH a 15% foram adicionados para converter os sólidos inorgânicos em uma massa filtrável. A mistura de reação foi filtrada e o bolo do filtro foi lavado primeiro com THF e depois com MeOH. Os licores-mãe e as lavagens combinados foram liberados do solvente sob vácuo e o resíduo foi suspenso em 1,5 L de H2O. Essa solução foi acidificada com HCl, lavada com 3x100 mL de CH2Cl2, tornada fortemente básica com NaOH 25% e reextraída com 4x100 mL de CH2Cl2. Os extratos agrupados foram removidos do solvente sob vácuo, resultando em 26 g de resíduo oleoso, que foi destilado a 120-130 °C a 0,5 mm/Hg para dar 21 g de um óleo branco, 2,5-dimetoxifenetilamina
(2C-H), que capta dióxido de carbono do ar muito rapidamente.
A uma solução bem agitada de 24,8 g de 2,5-dimetoxifenetilamina em 40 mL de ácido acético glacial, foram adicionados 22 g de bromo elementar dissolvido em 40 mL de ácido acético. Após alguns minutos, houve a formação de sólidos e a evolução simultânea de calor considerável. Permitiu-se que a mistura de reação voltasse à temperatura ambiente, filtrou-se e os sólidos foram lavados com moderação com ácido acético frio. Esse era o sal de bromidrato. Há muitas formas complicadas de sal, tanto polimorfos quanto hidratos, que podem tornar o isolamento e a caracterização do 2C-B traiçoeiros. O caminho mais feliz é formar o sal de cloridrato insolúvel por meio da base livre. Toda a massa de sal úmido com ácido acético foi dissolvida em H2O quente, tornada básica a pelo menos pH 11 com NaOH 25% e extraída com 3x100 mL de CH2Cl2. A remoção do solvente resultou em 33,7 g de resíduo que foi destilado a 115-130 °C a 0,4 mm/Hg. O óleo branco, 27,6 g, foi dissolvido em 50 mL de H2O contendo 7,0 g de ácido acético. Essa solução clara foi agitada vigorosamente e tratada com 20 mL de HCl concentrado. Houve uma formação imediata do sal anidro do cloridrato de 2,5-dimetoxi-4-bromofenetilamina (2C-B). Essa massa de cristais foi removida por filtração (pode se soltar consideravelmente com a adição de mais 60 mL de H2O), lavada com um pouco de H2O e, em seguida, com várias porções de 50 mL de Et2O. Quando completamente seco ao ar, foram obtidos 31,05 g de agulhas brancas finas, com um mp de 237-239 °C com decomposição. Quando há muita H2O presente no momento da adição do HCl concentrado final, obtém-se uma forma hidratada de 2C-B. O sal de hidrobrometo derrete a 214,5-215 °C. O sal de acetato foi relatado como tendo uma temperatura de 208-209 °C.
DOSAGEM: 12 a 24 mg.
DURAÇÃO: 4 a 8 h.
DOM
STP; 2,5-DIMETOXI-4-METILANFETAMINA
SÍNTESE: A uma solução de 54,9 g de 2,5-dimetoxi-4-metilbenzaldeído (veja a receita de
2C-D para sua preparação) em 215 g de ácido acético glacial foram adicionados 19,5 g de acetato de amônio anidro e 30,6 g de nitroetano. Essa mistura foi aquecida por 3 h no banho de vapor, a mistura de reação foi resfriada em um banho de gelo úmido, permitindo a formação espontânea de cristais amarelos. Foi adicionada a maior quantidade possível de H2O (apenas para evitar um caráter oleoso turvo persistente) e, após algumas horas adicionais em repouso, o 1-(2,5-dimetoxi-4-metilfenil)-2-nitropropeno cristalino foi removido por filtração e recristalizado a partir de ácido acético em ebulição. O rendimento, após secagem até peso constante, foi de 28,3 g e a temperatura média foi de 87-88 °C. Anal. (C12H15NO4) C, H ,N.
Uma suspensão de 9,5 g de LAH em 750 mL de Et2O anidro bem agitado foi mantida em refluxo sob uma atmosfera inerte, com o retorno do solvente condensado passando por um dedal de Soxhlet contendo 9,5 g de 1-(2,5-dimetoxi-4-metilfenil)-2-nitropropeno. Depois que a adição do nitroestireno foi concluída, a suspensão agitada foi mantida em refluxo por mais 4 horas, depois resfriada à temperatura ambiente e deixada em agitação durante a noite. O excesso de hidreto foi destruído pela adição de 750 mL de H2SO4 a 8%, com cuidado, até que a evolução do hidrogênio cessasse e, em seguida, a uma velocidade que permitisse a dispersão dos sólidos formados. As fases foram separadas, a fase aquosa foi lavada uma vez com Et2O, tratada com 225 g de tartarato de sódio e potássio e, por fim, tornada básica (pH >9) com NaOH a 5%. Essa fase foi extraída com 3x150 mL de CH2Cl2, os extratos foram agrupados e o solvente foi removido sob vácuo. O resíduo foi 9,6 g de um óleo transparente que formou espontaneamente cristais com uma temperatura de 60,5-61 °C a partir do hexano. Esses sólidos foram dissolvidos em 150 mL de Et2O anidro e saturados com gás HCl anidro. Depois de permanecer em temperatura ambiente por 2 h, o cloridrato cristalino de 2,5-dimetoxi-4-metilanfetamina (DOM) foi removido por filtração, lavado com Et2O e seco ao ar até peso constante. Foram obtidos 8,25 g de cristais brancos brilhantes que tinham um ponto de fusão de 190,5-191,5 °C. O sulfato tinha uma temperatura de 131 °C. Anal. (C12H20ClNO2) C, H ,N.
O nitrostyrene acima também pode ser convertido no produto final de amina por meio do intermediário da fenilacetona correspondente. A uma suspensão bem agitada de 10,4 g de ferro em pó em 20 mL de ácido acético glacial mantido em temperatura de refluxo, foram adicionados 4,9 g de 1-(2,5-dimetoxi-4-metilfenil)-2-nitropropeno como um sólido. O refluxo continuou por 2 horas e, em seguida, tudo foi filtrado em Celite úmida. Após a lavagem com 300 mL de H2O seguida de 300 mL de Et2O, o filtrado combinado e as lavagens foram separados, e a fase aquosa foi extraída com 2x100 mL de Et2O. A fase orgânica e os extratos foram combinados e lavados com 2x100 mL de K2CO3 saturado e o solvente foi removido sob vácuo, produzindo um óleo avermelhado pesando 3,3 g. Este foi destilado a 111-115 °C a 0,5 mm/Hg para dar um sólido verde-claro. Após a recristalização a partir do benzeno, foram obtidos 2,8 g de 1-(2,5-dimetoxi-4-metilfenil)-2-propanona como cristais brancos com uma temperatura média de 57-59 °C. Essa cetona também foi descrita como um óleo amarelo-claro com um bp de 115-118 °C a 0,4 mm/Hg. Uma solução de 0,7 g de 1-(2,5-dimetoxifenil-4-metil)-2-propanona em 20 mL de MeOH foi tratada com 6,0 g de acetato de amônio, 0,3 g de cianoborohidreto de sódio e 3 g de peneiras moleculares Linde 3 A. A mistura foi agitada durante a noite, os sólidos foram removidos por filtração e o filtrado foi dissolvido em 100 mL de H2O. A solução foi acidificada com H2SO4 diluído e lavada com 2x25 mL de CH2Cl2. A fase aquosa foi tornada básica com NaOH aquoso, e o produto foi extraído com 2x25 mL de CH2Cl2. O solvente foi removido sob vácuo e o resíduo destilado (a 160 °C a 0,2 mm/Hg) para dar origem a um produto incolor que foi dissolvido em 3 mL de IPA, neutralizado com HCl concentrado e diluído com 50 mL de Et2O anidro. Obteve-se 0,18 g de cloridrato de 2,5-dimetoxi-4-metilanfetamina (DOM) como um sólido branco com uma temperatura média de 187-188 °C.
Os isômeros ópticos do DOM foram preparados de duas maneiras. A base racêmica foi resolvida como o sal de ácido orto-nitrotartranílico por recristalização de EtOH. O ácido (+) fornece preferencialmente o isômero (+) ou "S" do DOM. Além disso, a 1-(2,5-dimetoxi-4-metilfenil)-2-propanona mencionada acima pode ser aminada redutivamente com alfa-metil benzilamina opticamente ativa com níquel Raney. Essa amina é isolada e purificada por recristalização do sal de cloridrato. Quando opticamente puro, o grupo benzílico foi removido por hidrogenólise com paládio sobre carbono. A PM de qualquer um dos isômeros ópticos, como os sais de cloridrato, foi de 204-205 °C.
DOSAGEM: 3 - 10 mg.
DURAÇÃO: 14 - 20 h.
MDA
3,4-METILENODIOXIANFETAMINA
SÍNTESE: (a partir do piperonal) A uma solução de 15,0 g de piperonal em 80 mL de ácido acético glacial foram adicionados 15 mL de nitroetano, seguidos de 10 g de ciclohexilamina. A mistura foi mantida em temperatura de banho de vapor por 6 h, diluída com 10 mL de H2O, semeada com um cristal do produto e resfriada durante a noite a 10 °C. Os cristais amarelos brilhantes foram removidos por filtração e secos ao ar para produzir 10,7 g de 1-(3,4-metilenodioxifenil)-2-nitropropeno com uma temperatura média de 93-94 °C. Esse valor foi aumentado para 97-98 °C por recristalização a partir de ácido acético. Os esforços mais convencionais de síntese de nitrostyrene usando um excesso de nitroetano como solvente e acetato de amônio anidro como base, dão produto impuro em rendimentos muito baixos. O nitrostyrene foi produzido com sucesso a partir dos componentes em MeOH frio, com NaOH aquoso como base.
Uma suspensão de 20 g de LAH em 250 mL de THF anidro foi colocada sob uma atmosfera inerte e agitada magneticamente. Foram adicionados, gota a gota, 18 g de 1-(3,4-metilenodioxifenil)-2-nitropropeno em solução em THF e a mistura de reação foi mantida em refluxo por 36 h. Depois de voltar à temperatura ambiente, o excesso de hidreto foi destruído com 15 mL de IPA, seguido por 15 mL de NaOH a 15%. Foram adicionados mais 50 mL de H2O para completar a conversão dos sais de alumínio em um sólido solto, branco e facilmente filtrável. Esse sólido foi removido por filtração e o bolo do filtro foi lavado com THF adicional. O filtrado combinado e as lavagens foram removidos do solvente sob vácuo, e o resíduo foi dissolvido em H2SO4 diluído. A lavagem com 3 x 75 mL de CH2Cl2 removeu grande parte da cor, e a fase aquosa foi tornada básica e reextraída com 3 x 100 mL de CH2Cl2. A remoção do solvente produziu 13,0 g de um óleo de cor amarela que foi destilado. A fração que ferveu a 80-90 °C a 0,2 mm pesou 10,2 g e era branca como água. Ela foi dissolvida em 60 mL de IPA, neutralizada com HCl concentrado e diluída com 120 mL de Et2O anidro, o que produziu uma turbidez duradoura. Formaram-se cristais espontaneamente, que foram removidos por filtração, lavados com Et2O e secos ao ar para fornecer 10,4 g de cloridrato de 3,4-metilenodioxianfetamina (MDA) com um pH de 187-188 °C.
(a partir de 3,4-metilenodioxifenilacetona) A uma solução de 32,5 g de acetato de amônio anidro em 120 mL de MeOH, foram adicionados 7,12 g de 3,4-metilenodioxifenilacetona (consulte MDMA para obter informações sobre sua preparação), seguidos de 2,0 g de cianoborohidreto de sódio. A solução amarela resultante foi vigorosamente agitada e HCl concentrado foi adicionado periodicamente para manter o pH da mistura de reação entre 6 e 7, conforme determinado por papel de pH universal úmido externo. Após vários dias, os sólidos não dissolvidos permaneceram na mistura da reação e não foi necessário adicionar mais ácido. A mistura de reação foi adicionada a 600 mL de HCl diluído, que foi lavado com 3x100 mL de CH2Cl2. As lavagens combinadas foram extraídas novamente com uma pequena quantidade de HCl diluído, as fases aquosas foram combinadas e tornadas básicas com NaOH 25%. Em seguida, o produto foi extraído com 3x100 mL de CH2Cl2, esses extratos foram combinados e o solvente foi removido sob vácuo para fornecer 3,8 g de um resíduo de cor vermelha. Esse resíduo foi destilado a 80-90 °C a 0,2 mm/Hg para fornecer 2,2 g de um óleo branco absolutamente aquoso. Não houve formação óbvia de um sal de carbonato quando exposto ao ar. Ele foi dissolvido em 15 mL de IPA, neutralizado com 25 gotas de HCl concentrado e diluído com 30 mL de Et2O anidro. Lentamente, houve a deposição de cristais brancos de cloridrato de 3,4-metilenodioxianfetamina (MDA), que pesava 2,2 g e tinha uma temperatura de 187-188 °C. A preparação da formamida (um precursor do MDMA) e da acetamida (um precursor do MDE) está descrita nessas entradas.
DOSAGEM: 80 - 160 mg.
DURAÇÃO: 4 - 6
(revisado em setembro de 2001).
MESCALINA;
3,4,5-TRIMETOXIFENETILAMINA
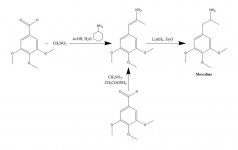
SÍNTESE: Uma solução de 20 g de 3,4,5-trimetoxibenzaldeído, 40 mL de nitrometano e 20 mL de ciclohexilamina em 200 mL de ácido acético foi aquecida no banho de vapor por 1 h. A mistura de reação foi então diluída lentamente e com boa agitação, com 400 mL de H2O, o que permitiu a formação de uma massa cristalina amarela pesada. Essa massa foi removida por filtração, lavada com H2O e sugada o mais seco possível. A recristalização a partir de MeOH fervente (15 mL/g) produziu, após filtração e secagem ao ar, beta-nitro-3,4,5-trimetoxiestireno como cristais amarelos brilhantes pesando 18,5 g. Uma síntese alternativa foi eficaz, usando um excesso de nitrometano como solvente e reagente, se a quantidade de catálise de acetato de amônio fosse mantida pequena. Uma solução de 20 g de 3,4,5-trimetoxibenzaldeído em 40 mL de nitrometano contendo 1 g de acetato de amônio anidro foi aquecida no banho de vapor por 4 h. O solvente foi removido sob vácuo e o óleo amarelo residual foi dissolvido em dois volumes de MeOH quente, decantado de alguns insolúveis e deixado esfriar. Os cristais formados foram removidos por filtração, lavados com MeOH e secos ao ar, produzindo 14,2 g de cristais amarelos brilhantes de beta-nitro-3,4,5-trimetoxiestireno. O uso dessas proporções, mas com 3,5 g de acetato de amônio, deu origem a produtos de reação lateral extensos, mesmo quando trabalhados após apenas 1,5 h de aquecimento. O rendimento do nitroestireno foi, nesse último caso, insatisfatório.
A uma suspensão de refluxo suave de 2 g de LAH em 200 mL de Et2O, foram adicionados 2,4 g de beta-nitro-3,4,5-trimetoxiestireno como uma solução saturada de Et2O usando um condensador de extração Soxhlet modificado para permitir o retorno contínuo do solvente condensado através do dedal. Depois que a adição foi concluída, as condições de refluxo foram mantidas por mais 48 h. Após o resfriamento da mistura de reação, um total de 150 mL de H2SO4 1,5 N foi adicionado com cautela, destruindo o excesso de hidreto e, por fim, fornecendo duas fases claras. Elas foram separadas, e a fase aquosa foi lavada uma vez com 50 mL de Et2O. Em seguida, foram adicionados 50 g de tartarato de sódio e potássio, seguidos de NaOH suficiente para elevar o pH a >9. Em seguida, extraiu-se com 3x75 mL de CH2Cl2, e o solvente dos extratos agrupados foi removido sob vácuo. O resíduo foi destilado a 120-130 °C a 0,3 mm/Hg, resultando em um óleo branco que foi dissolvido em 10 mL de IPA e neutralizado com HCl concentrado. Os cristais brancos que se formaram foram diluídos com 25 mL de Et2O, removidos por filtração e secos ao ar para fornecer 2,1 g de cloridrato de 3,4,5-trimetoxifenetilamina (M) como cristais brancos brilhantes. O sal de sulfato formou cristais espetaculares a partir da água, mas tinha um mp amplo e não característico. Uma síntese alternativa pode empregar 3,4,5-trimetoxifenilacetonitrila, conforme descrito em beta-D.
DOSAGEM: 200-400 mg (como sal de sulfato), 178-356 mg (como sal de cloridrato)
[Nota da Erowid: O texto original dizia "178-256", mas isso foi um erro. O erro foi encontrado por Bo e verificado com Shulgin. Consulte a página Erowid Mescaline Dosage (Dosagem de mescalina ) para obter uma discussão mais completa sobre as formas de mescalina].
DURAÇÃO: 10-12 h
TMA
3,4,5-TRIMETOXIANFETAMINA
SÍNTESE: A uma solução de 39,2 g de 3,4,5-trimetoxibenzaldeído em 30 mL de EtOH quente, foram adicionados 15,7 g de nitroetano, seguidos de 1,5 mL de n-butilamina. A mistura de reação foi deixada em repouso a 40 °C por 7 dias. Com o resfriamento e a raspagem, foram obtidas agulhas finas amarelas que, depois de removidas por filtração e secagem ao ar, pesaram 48 g. A recristalização a partir de EtOH deu 2-nitro-1-(3,4,5-trimetoxifenil)propeno como cristais amarelos com uma temperatura média de 94-95 °C. Anal. (C12H15NO5) C,H,N. Como alternativa, uma solução de 20 g do aldeído em 75 mL de nitroetano foi tratada com 4 g de acetato de amônio anidro e aquecida no banho de vapor até gerar uma cor vermelha intensa. A remoção do excesso de solvente/reagente sob vácuo resultou em um óleo vermelho que foi dissolvido em um volume igual de MeOH em ebulição. No resfriamento, os cristais amarelos do nitropropeno se separaram. A recristalização a partir de MeOH resultou, após secagem ao ar até peso constante, em 13,0 g com o mesmo pH.
Sob uma atmosfera inerte, 38 g de LAH foram umedecidos com 100 mL de Et2O anidro e, em seguida, suspensos em 1 L de THF seco. Isso foi levado a um refluxo suave e foi adicionada, lentamente, uma solução de 43,7 g de 2-nitro-1-(3,4,5-trimetoxifenil)propeno em 160 mL de THF. O refluxo foi mantido por 36 horas e, em seguida, a mistura de reação foi resfriada com um banho de gelo externo. O excesso de hidreto foi destruído pela adição cautelosa de 38 mL de H2O, seguida por 38 mL de NaOH a 15% e, finalmente, mais 114 mL de H2O. Os sais inorgânicos, que deveriam ter se transformado em uma massa solta, granular e facilmente filtrável, pareciam mais uma pasta de biblioteca, mas foram filtrados mesmo assim. Foi feita uma tentativa de lavagem com THF, mas não foi eficiente. O filtrado combinado e as lavagens foram removidos do solvente sob vácuo, resultando em 31,5 g da base bruta como um óleo âmbar. Esse óleo foi dissolvido em 140 mL de IPA, neutralizado com HCl concentrado (foram necessários 15 mL) e diluído com 650 mL de Et2O anidro. Houve uma fase oleosa inicial que, com agitação contínua, transformou-se em sólidos rosa pálido. Esses foram finamente moídos em CH3CN para dar 15,2 g de cloridrato de 3,4,5-trimetoxianfetamina (TMA) como cristais brancos que derreteram a 195-211 °C. Todos os sais de alumínio de todos os lugares foram dissolvidos em HCl diluído e 1 kg de tartarato de sódio e potássio foi adicionado. Adicionou-se NaOH a 25%, o que permitiu elevar o pH a >9 sem a precipitação de alumina básica. A extração dessa fase com CH2Cl2 foi seguida pela remoção do solvente e a formação de sal, conforme descrito acima, permitiu o isolamento de mais 6,4 g de TMA. O produto preparado dessa maneira contém cerca de 10-15% de 3,5-dimetoxi-4-hidroxianfetamina como impureza. Uma solução de 20 g de TMA feita dessa maneira em 200 mL de NaOH a 5% foi extraída com 2x200 mL de CH2Cl2. Os extratos agrupados foram lavados com 4x100 mL de NaOH a 5%, e as lavagens aquosas foram agrupadas com a fase de base original. A fase orgânica foi removida de seu CH2Cl2 sob vácuo para dar origem a um óleo que foi dissolvido em 40 mL de IPA, neutralizado com HCl concentrado e diluído com 400 mL de Et2O anidro. Houve a formação imediata de cristais brancos espetaculares de cloridrato de 3,4,5-trimetoxianfetamina puro, pesando 15,4 g e com uma temperatura de 220-221 °C. A fase aquosa foi levada à neutralidade, tratada com 10 g de di-hidrogenofosfato de potássio, levada ao pH 9,0 com a adição cuidadosa de NaOH e extraída com 5x100 mL de CH2Cl2. A evaporação do solvente sob vácuo resultou em um óleo que se cristalizou espontaneamente. Esse produto, 3,5-dimetoxi-4-hidroxianfetamina, pode ser purificado por
sublimação a 130 °C a 0,2 mm/Hg. Era um sólido cristalino branco que descoloriu lentamente no ar. A literatura descreve um sal de picrato com uma temperatura de 225 °C a partir de EtOH.
DOSAGEM: 100 - 250 mg.
DURAÇÃO: 6 a 8 h.