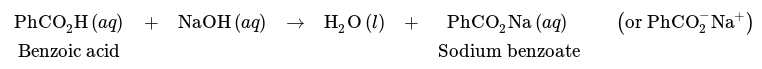G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,654
- Solutions
- 3
- Reaction score
- 2,732
- Points
- 113
- Deals
- 1
Teoria da extração.
A "extração" refere-se à transferência de composto(s) de um sólido ou líquido para um solvente ou fase diferente. Quando uma saqueta de chá é adicionada à água quente, os compostos responsáveis pelo sabor e cor do chá são extraídos da borra para a água. O café descafeinado é produzido utilizando solventes ou dióxido de carbono supercrítico para extrair a cafeína dos grãos de café. No laboratório de química, é mais comum utilizar a extração líquido-líquido, um processo que ocorre num funil de separação. Uma solução contendo componentes dissolvidos é colocada no funil e um solvente imiscível é adicionado, resultando em duas camadas que são agitadas juntas. É mais comum que uma camada seja aquosa e a outra seja um solvente orgânico. Os componentes são "extraídos" quando passam de uma camada para a outra. A forma da ampola de decantação permite uma drenagem eficiente e a separação das duas camadas.
Fig.1 Esquema da extração

Os compostos movem-se de um líquido para outro dependendo da sua solubilidade relativa em cada líquido. Um guia rápido para a solubilidade é o princípio "semelhante dissolve semelhante", o que significa que os compostos não polares devem ser facilmente extraídos para solventes não polares (e vice-versa). Os compostos responsáveis pelo sabor e cor do chá devem ser polares se forem facilmente extraídos para a água quente. Quando se permite o equilíbrio entre dois líquidos num funil de separação, a maioria de um composto acaba frequentemente na camada em que é mais solúvel.
Fig.2

Procedimentos passo a passo para extracções.
Extração Líquido-Líquido
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/threads/extraction.553/
Extração simples.
As imagens desta secção mostram uma extração simples de vermelho de metilo (composto colorido, Fig. 3) de uma solução aquosa (camada inferior) para 25 ml de acetato de etilo (camada superior). A solução aquosa tem originalmente uma cor rosa, uma vez que o vermelho de metilo aparece vermelho em solução ácida (a solução aquosa foi feita a partir de 50 ml de água, 5 gotas de 0,1MHCl e 5 gotas de solução indicadora de vermelho de metilo a 1%). O vermelho de metilo tem um grande coeficiente de partição e é extraído da camada aquosa para o acetato de etilo neste processo.
Progresso da extração do vermelho de metilo (o composto colorido) da camada aquosa ácida (em baixo) para a camada orgânica (em cima). As inversões foram feitas lentamente de modo a ver a extração passo a passo. Mesmo com uma mistura suave, o vermelho de metilo é rapidamente extraído.


Preparar a configuração (para extração única)
1. Obter uma ampola de decantação (Fig.4 a).- a) Se a ampola de decantação tiver uma torneira de Teflon, voltar a montar a torneira, caso tenha sido desmontada para secar, colocando as peças pela ordem adequada (Fig. 4 b). Certificar-se de que a torneira de Teflon está moderadamente apertada, de modo a poder rodar facilmente, mas não tão solta que o líquido possa infiltrar-se na junta.
- b) Se utilizar uma torneira de vidro (Fig.4 c), provavelmente não necessita de mais preparação. Deve ser utilizada uma camada muito fina de massa lubrificante para vedar a torneira e evitar o congelamento. Se estiverem disponíveis torneiras de vidro e de Teflon, é preferível utilizar Teflon, uma vez que existe sempre a possibilidade de o solvente dissolver a massa lubrificante utilizada nas torneiras de vidro e contaminar a amostra.
- c) Obter também uma rolha (Teflon ou vidro esmerilado) que encaixe bem na junta superior do funil (Fig.4 a).
2. Colocar a ampola de decantação numa pinça de anel fixada a um suporte de anel ou a uma treliça. Os funis partem-se facilmente, pelo que se deve amortecer o funil na pinça metálica com pedaços de borracha cortada ou de tubos de plástico (Fig. 4 d).
Adicionar as soluções (para extração simples)
3. Antes de verter qualquer coisa para um funil de separação, certifique-se de que a torneira está na posição "fechada", em que a torneira está na horizontal (Fig.5 a). Como medida de segurança, coloque sempre um frasco de Erlenmeyer por baixo da ampola de decantação antes de verter (Fig. 5 b). Este pode apanhar o líquido no caso de a torneira ser acidentalmente deixada aberta, ou se a torneira estiver solta e o líquido vazar involuntariamente.
4. Com um funil, deitar o líquido a extrair na ampola de decantação (Fig. 5 b). A ampola de decantação nunca deve ser utilizada com um líquido quente ou morno. A junta de vidro esmerilado no topo de uma ampola de decantação é mais suscetível de aderir à rolha se, em algum momento, tiver havido líquido na junta. Verter o líquido para a ampola de decantação com um funil de haste curta evita que a junta fique molhada, pelo que é menos provável que congele durante a mistura.
3. Antes de verter qualquer coisa para um funil de separação, certifique-se de que a torneira está na posição "fechada", em que a torneira está na horizontal (Fig.5 a). Como medida de segurança, coloque sempre um frasco de Erlenmeyer por baixo da ampola de decantação antes de verter (Fig. 5 b). Este pode apanhar o líquido no caso de a torneira ser acidentalmente deixada aberta, ou se a torneira estiver solta e o líquido vazar involuntariamente.
4. Com um funil, deitar o líquido a extrair na ampola de decantação (Fig. 5 b). A ampola de decantação nunca deve ser utilizada com um líquido quente ou morno. A junta de vidro esmerilado no topo de uma ampola de decantação é mais suscetível de aderir à rolha se, em algum momento, tiver havido líquido na junta. Verter o líquido para a ampola de decantação com um funil de haste curta evita que a junta fique molhada, pelo que é menos provável que congele durante a mistura.
Deitar uma quantidade de solvente de extração na ampola de decantação, como indicado no procedimento (Fig.5 c). Não é necessário utilizar quantidades exactas de solvente para as extracções e os volumes podem ser medidos numa proveta graduada. Se um procedimento exigir 20 ml de solvente, é aceitável que sejam utilizados entre 20 e 25 ml de cada vez.
Misturar as soluções (para uma única extração)
6. Colocar a rolha no funil e segurar o funil de modo a que os dedos de uma mão cubram firmemente a rolha, enquanto a outra mão agarra o fundo do funil (Fig. 6 a).
7. Inverta suavemente o funil (Fig.6 b) e agite um pouco a mistura. Embora não seja invulgar que algum líquido se infiltre na junta de vidro esmerilado quando invertida, isso deve ser mínimo. Se o líquido pingar para os teus dedos ou luvas quando invertes o funil, a rolha é provavelmente do tamanho errado.
Misturar as soluções (para uma única extração)
6. Colocar a rolha no funil e segurar o funil de modo a que os dedos de uma mão cubram firmemente a rolha, enquanto a outra mão agarra o fundo do funil (Fig. 6 a).
7. Inverta suavemente o funil (Fig.6 b) e agite um pouco a mistura. Embora não seja invulgar que algum líquido se infiltre na junta de vidro esmerilado quando invertida, isso deve ser mínimo. Se o líquido pingar para os teus dedos ou luvas quando invertes o funil, a rolha é provavelmente do tamanho errado.
8. A pressão pode acumular-se no interior da ampola de decantação quando as soluções são misturadas, pelo que, imediatamente após a agitação, e com a ampola ainda invertida, "ventilar" a ampola abrindo brevemente a torneira para permitir a libertação da pressão (Fig. 6 c). A pressão aumenta no funil à medida que o solvente evapora para o espaço livre e contribui com vapor adicional para a pressão inicial de ∼1 atmosfera de ar no funil. Com solventes altamente voláteis (como o éter dietílico), pode ouvir-se um "swoosh" definitivo quando se ventila, e pequenas quantidades de líquido podem mesmo salpicar a torneira. Se o líquido sair pela torneira, tente deixá-lo escorrer de volta para o funil. O ruído associado à ventilação cessa normalmente após a segunda ou terceira inversão, uma vez que o espaço livre fica saturado com vapores de solvente e as pressões dentro e fora do funil são igualadas.
Nota de segurança: Nunca aponte a torneira na direção de alguém enquanto ventila, pois é possível que algum líquido salpique para essa pessoa.
9. Feche a torneira e misture as soluções com um pouco mais de vigor, parando periodicamente para ventilar o sistema. Existem diferenças de opinião sobre a intensidade com que as soluções devem ser misturadas nas ampolas de decantação e durante quanto tempo. Como orientação geral, uma mistura ligeira durante 10-20 segundos deve ser suficiente. No caso de algumas soluções (por exemplo, diclorometano), deve ter-se o cuidado de não agitar demasiado vigorosamente, uma vez que estas soluções formam frequentemente emulsões (em que a interface entre as soluções não é clara). Com soluções propensas a emulsões, um funil deve ser agitado suavemente durante um minuto.
10. Colocar a ampola de decantação na vertical na pinça de anel para permitir que as camadas se separem completamente. A interface entre as camadas deve assentar rapidamente, frequentemente em cerca de 10 segundos. Se a interface estiver turva ou não estiver bem definida (formou-se uma emulsão), consultar a secção de resolução de problemas para obter sugestões.
Separar as camadas (para extração única)
11. O líquido não escorrerá bem de uma ampola de decantação se a rolha permanecer colocada, uma vez que o ar não pode entrar na ampola para substituir o líquido deslocado. Se o líquido escorrer do funil sem ser substituído por um volume igual de ar, formar-se-á uma pressão negativa no funil. Assim, antes de escoar o líquido de uma ampola de decantação, retirar a rolha (Fig.7 a).
12. Esvaziar a maior parte da camada inferior para um Erlenmeyer limpo, posicionando a pinça de anel de modo a que a ponta da ampola de decantação fique encaixada no Erlenmeyer para evitar salpicos (Fig. 7 b). Parar a drenagem quando a interface estiver a 1 cm do fundo da torneira.
13. Agitar suavemente o funil para desalojar as gotículas que se agarram ao vidro (Fig. 7 c). Pode utilizar-se uma vareta de agitação de vidro para derrubar as gotículas mais difíceis de agarrar.
14. Em seguida, drenar a camada inferior, parando quando a interface entrar na câmara da torneira (Fig. 7 d). Rotular o Erlenmeyer (por exemplo, "camada inferior").
Nota de segurança: Nunca aponte a torneira na direção de alguém enquanto ventila, pois é possível que algum líquido salpique para essa pessoa.
9. Feche a torneira e misture as soluções com um pouco mais de vigor, parando periodicamente para ventilar o sistema. Existem diferenças de opinião sobre a intensidade com que as soluções devem ser misturadas nas ampolas de decantação e durante quanto tempo. Como orientação geral, uma mistura ligeira durante 10-20 segundos deve ser suficiente. No caso de algumas soluções (por exemplo, diclorometano), deve ter-se o cuidado de não agitar demasiado vigorosamente, uma vez que estas soluções formam frequentemente emulsões (em que a interface entre as soluções não é clara). Com soluções propensas a emulsões, um funil deve ser agitado suavemente durante um minuto.
10. Colocar a ampola de decantação na vertical na pinça de anel para permitir que as camadas se separem completamente. A interface entre as camadas deve assentar rapidamente, frequentemente em cerca de 10 segundos. Se a interface estiver turva ou não estiver bem definida (formou-se uma emulsão), consultar a secção de resolução de problemas para obter sugestões.
Separar as camadas (para extração única)
11. O líquido não escorrerá bem de uma ampola de decantação se a rolha permanecer colocada, uma vez que o ar não pode entrar na ampola para substituir o líquido deslocado. Se o líquido escorrer do funil sem ser substituído por um volume igual de ar, formar-se-á uma pressão negativa no funil. Assim, antes de escoar o líquido de uma ampola de decantação, retirar a rolha (Fig.7 a).
12. Esvaziar a maior parte da camada inferior para um Erlenmeyer limpo, posicionando a pinça de anel de modo a que a ponta da ampola de decantação fique encaixada no Erlenmeyer para evitar salpicos (Fig. 7 b). Parar a drenagem quando a interface estiver a 1 cm do fundo da torneira.
13. Agitar suavemente o funil para desalojar as gotículas que se agarram ao vidro (Fig. 7 c). Pode utilizar-se uma vareta de agitação de vidro para derrubar as gotículas mais difíceis de agarrar.
14. Em seguida, drenar a camada inferior, parando quando a interface entrar na câmara da torneira (Fig. 7 d). Rotular o Erlenmeyer (por exemplo, "camada inferior").
15. Verter a camada superior do topo da ampola de decantação para outro Erlenmeyer limpo (Fig. 8 a), certificando-se de rotular novamente este frasco (Fig. 8 b). É uma técnica correcta drenar a camada inferior através da torneira e verter a camada superior a partir do topo do funil. Este método minimiza a re-mistura das soluções, uma vez que apenas a camada inferior toca na haste do funil.
16. Nunca deite fora os líquidos de uma extração até ter a certeza absoluta de que tem o composto desejado. As camadas não desejadas podem ser corretamente eliminadas quando o composto desejado estiver nas suas mãos (por exemplo, depois de o evaporador rotativo ter removido o solvente).
Os erros cometidos durante as extracções (por exemplo, continuar com a camada errada) podem ser resolvidos desde que as soluções não tenham sido colocadas no contentor de resíduos! As camadas também devem ser guardadas até depois da evaporação, porque o composto desejado pode não ser muito solúvel no solvente utilizado. Se o composto não for extraído com um solvente, pode tentar-se mais tarde com um solvente diferente, mas apenas se as camadas ainda não tiverem sido deitadas fora.
Limpeza (para extração simples)
Para limpar uma ampola de decantação, lavar primeiro com acetona para um recipiente de resíduos. Em seguida, lave o funil com água e sabão na bancada. Desmontar a torneira de Teflon (se utilizada). Depois de enxaguar com água destilada, deixar secar as partes separadas no seu cacifo (Fig.8 c).
Os erros cometidos durante as extracções (por exemplo, continuar com a camada errada) podem ser resolvidos desde que as soluções não tenham sido colocadas no contentor de resíduos! As camadas também devem ser guardadas até depois da evaporação, porque o composto desejado pode não ser muito solúvel no solvente utilizado. Se o composto não for extraído com um solvente, pode tentar-se mais tarde com um solvente diferente, mas apenas se as camadas ainda não tiverem sido deitadas fora.
Limpeza (para extração simples)
Para limpar uma ampola de decantação, lavar primeiro com acetona para um recipiente de resíduos. Em seguida, lave o funil com água e sabão na bancada. Desmontar a torneira de Teflon (se utilizada). Depois de enxaguar com água destilada, deixar secar as partes separadas no seu cacifo (Fig.8 c).
Extracções múltiplas.
Nesta secção são dadas instruções passo a passo sobre como extrair uma solução aquosa com um solvente orgânico menos denso que a água (a camada orgânica ficará no topo). Como exemplo, as instruções são escritas para extrair uma solução aquosa três vezes usando 25 ml de éter dietílico de cada vez (3×25 ml de éter dietílico). Um resumo do procedimento das duas primeiras extracções encontra-se na Fig.9 Duas extracções quando a camada orgânica está no topo.
Extração #1
1. Efetuar uma única extração utilizando aproximadamente 25 ml de éter dietílico (não é necessária uma quantidade exacta), como descrito anteriormente, certificando-se de que cada camada é devidamente identificada (por exemplo, "camada orgânica superior" e "camada aquosa inferior").
Extração #2
2. Devolver a camada aquosa à ampola de decantação. Não é necessário lavar o funil entre extracções.
3. Adicionar uma nova porção de 25 ml de éter etílico à ampola de decantação. Tapar a ampola, inverter e agitar com ventilação, deixando depois separar as camadas.
Nesta fase, devem existir duas camadas na ampola de decantação. Se não existirem duas camadas, é provável que a camada errada tenha sido adicionada ao funil na etapa 2 (um erro comum). Uma forma de testar se este foi o erro é adicionar um pouco de água de uma garrafa de esguicho. Se a camada devolvida ao funil de separação for a camada orgânica (incorrecta), a água da garrafa de esguicho não se misturará com a solução e cairá como gotículas no fundo. Se a camada orgânica (incorrecta) foi acidentalmente devolvida à ampola de decantação, não há qualquer dano, uma vez que a camada orgânica foi simplesmente diluída. Verter o líquido de volta para o frasco destinado à camada orgânica e, em vez disso, adicionar a solução aquosa ao funil.
4. Escoar a camada aquosa inferior para um Erlenmeyer: é aceitável utilizar o mesmo frasco que foi utilizado para a camada aquosa na primeira extração (que pode ter sido rotulado como "camada aquosa inferior").
5. Uma vez que é mais comum combinar as camadas orgânicas em extracções múltiplas, a camada orgânica superior pode ser vertida da ampola de decantação para o mesmo balão que foi utilizado para a camada orgânica na primeira extração (que pode ter sido rotulado como "camada orgânica superior"). Neste balão, deve haver cerca de 50 ml de éter etílico proveniente das duas extracções.
Extração #3
6. Repita a extração uma terceira vez, adicionando a camada aquosa da segunda extração à ampola de decantação, seguida de outra porção fresca de 25 ml de éter etílico. Tapar a ampola de decantação, inverter e agitar com ventilação, e deixar separar as camadas.
7. Escoar a camada aquosa para o balão apropriado e verter novamente a camada superior para o balão da camada orgânica, onde deverá haver cerca de 75 ml de éter etílico proveniente das três extracções.
1. Efetuar uma única extração utilizando aproximadamente 25 ml de éter dietílico (não é necessária uma quantidade exacta), como descrito anteriormente, certificando-se de que cada camada é devidamente identificada (por exemplo, "camada orgânica superior" e "camada aquosa inferior").
Extração #2
2. Devolver a camada aquosa à ampola de decantação. Não é necessário lavar o funil entre extracções.
3. Adicionar uma nova porção de 25 ml de éter etílico à ampola de decantação. Tapar a ampola, inverter e agitar com ventilação, deixando depois separar as camadas.
Nesta fase, devem existir duas camadas na ampola de decantação. Se não existirem duas camadas, é provável que a camada errada tenha sido adicionada ao funil na etapa 2 (um erro comum). Uma forma de testar se este foi o erro é adicionar um pouco de água de uma garrafa de esguicho. Se a camada devolvida ao funil de separação for a camada orgânica (incorrecta), a água da garrafa de esguicho não se misturará com a solução e cairá como gotículas no fundo. Se a camada orgânica (incorrecta) foi acidentalmente devolvida à ampola de decantação, não há qualquer dano, uma vez que a camada orgânica foi simplesmente diluída. Verter o líquido de volta para o frasco destinado à camada orgânica e, em vez disso, adicionar a solução aquosa ao funil.
4. Escoar a camada aquosa inferior para um Erlenmeyer: é aceitável utilizar o mesmo frasco que foi utilizado para a camada aquosa na primeira extração (que pode ter sido rotulado como "camada aquosa inferior").
5. Uma vez que é mais comum combinar as camadas orgânicas em extracções múltiplas, a camada orgânica superior pode ser vertida da ampola de decantação para o mesmo balão que foi utilizado para a camada orgânica na primeira extração (que pode ter sido rotulado como "camada orgânica superior"). Neste balão, deve haver cerca de 50 ml de éter etílico proveniente das duas extracções.
Extração #3
6. Repita a extração uma terceira vez, adicionando a camada aquosa da segunda extração à ampola de decantação, seguida de outra porção fresca de 25 ml de éter etílico. Tapar a ampola de decantação, inverter e agitar com ventilação, e deixar separar as camadas.
7. Escoar a camada aquosa para o balão apropriado e verter novamente a camada superior para o balão da camada orgânica, onde deverá haver cerca de 75 ml de éter etílico proveniente das três extracções.
Resolução de problemas.
Esta secção descreve problemas e soluções comuns nas extracções.Existe apenas uma camada
A razão mais comum para ter apenas uma camada numa ampola de decantação quando deveria haver duas (como quando o procedimento diz para "separar as camadas"), é ter cometido um erro. O que provavelmente aconteceu é que a camada errada foi adicionada à ampola de decantação - por exemplo, a camada orgânica foi adicionada inconscientemente em vez da camada aquosa. Quando o solvente orgânico é adicionado a uma camada orgânica na ampola de decantação, o resultado é apenas uma camada. O erro pode ser corrigido, desde que as camadas ainda não tenham sido deitadas fora! Se a camada correcta for adicionada ao funil, tudo correrá como planeado. Para evitar este erro no futuro, não se esqueça de etiquetar os frascos Erlenmeyer. Além disso, nunca deite fora uma camada até ter a certeza absoluta de que fez tudo corretamente.
Uma razão ocasional para a formação de apenas uma camada num funil de separação é a presença de grandes quantidades de compostos que se dissolvem em ambos os solventes, por exemplo, se estiverem presentes grandes quantidades de etanol, que se dissolve bem tanto em solventes aquosos como orgânicos. Nesta situação, a melhor abordagem é remover o composto problemático (ou seja, o etanol) num evaporador rotativo antes da extração.
Existem três camadas
A razão mais comum para a existência de três camadas numa ampola de decantação é a mistura inadequada (Fig.10 a). Se a ampola de decantação for agitada com mais vigor, é provável que se formem duas camadas (Fig. 10 b). Também é possível que uma terceira camada intermédia seja uma emulsão, onde as duas camadas não estão completamente separadas.
A razão mais comum para ter apenas uma camada numa ampola de decantação quando deveria haver duas (como quando o procedimento diz para "separar as camadas"), é ter cometido um erro. O que provavelmente aconteceu é que a camada errada foi adicionada à ampola de decantação - por exemplo, a camada orgânica foi adicionada inconscientemente em vez da camada aquosa. Quando o solvente orgânico é adicionado a uma camada orgânica na ampola de decantação, o resultado é apenas uma camada. O erro pode ser corrigido, desde que as camadas ainda não tenham sido deitadas fora! Se a camada correcta for adicionada ao funil, tudo correrá como planeado. Para evitar este erro no futuro, não se esqueça de etiquetar os frascos Erlenmeyer. Além disso, nunca deite fora uma camada até ter a certeza absoluta de que fez tudo corretamente.
Uma razão ocasional para a formação de apenas uma camada num funil de separação é a presença de grandes quantidades de compostos que se dissolvem em ambos os solventes, por exemplo, se estiverem presentes grandes quantidades de etanol, que se dissolve bem tanto em solventes aquosos como orgânicos. Nesta situação, a melhor abordagem é remover o composto problemático (ou seja, o etanol) num evaporador rotativo antes da extração.
Existem três camadas
A razão mais comum para a existência de três camadas numa ampola de decantação é a mistura inadequada (Fig.10 a). Se a ampola de decantação for agitada com mais vigor, é provável que se formem duas camadas (Fig. 10 b). Também é possível que uma terceira camada intermédia seja uma emulsão, onde as duas camadas não estão completamente separadas.
Existe material insolúvel na interface.
Uma pequena quantidade de película insolúvel entre duas camadas não é invulgar durante uma extração. Os materiais poliméricos tendem a repousar entre as camadas, uma vez que as interacções com o solvente são minimizadas na interface. Uma pequena película não é algo com que se preocupar, porque se uma pequena quantidade chegar à camada orgânica, uma etapa subsequente de secagem e filtração irá frequentemente removê-la.
A interface não pode ser vista.
Ocasionalmente, os compostos num funil de separação são tão escuros que obscurecem a interface entre as duas camadas. Se isto acontecer, existem vários métodos que podem ajudar a ver a interface. Um deles é segurar a ampola de decantação contra a luz ou apontar uma lanterna para o vidro (Fig.11 b). Por vezes, a luz adicional permite-lhe ver a interface. Um segundo método consiste em observar cuidadosamente as camadas enquanto se inclina o funil para trás e para o lado (Fig. 11 c). O olho pode por vezes detetar diferenças subtis na forma como os líquidos fluem. Um terceiro método é adicionar um pouco mais de solvente ao funil para diluir um pouco uma das camadas, ou adicionar um solvente diferente para alterar o índice de refração.
As camadas não se separam bem (forma-se uma emulsão)
As emulsões podem ocorrer por várias razões.
1. A densidade de cada camada pode ser tão semelhante que há pouca motivação para que os líquidos se separem.2. Podem estar presentes compostos semelhantes ao sabão ou outros agentes emulsionantes que dissolvem alguns componentes uns nos outros.
As emulsões podem ser muito difíceis de retificar e é preferível evitá-las agitando suavemente no funil de separação soluções propensas a emulsões (por exemplo, diclorometano com soluções altamente básicas ou densas). No entanto, se se formar uma emulsão, existem algumas formas de a tentar clarificar.
- a) Para emulsões ligeiras, agitar suavemente as camadas e tentar derrubar as gotículas em suspensão com uma vareta de agitação de vidro.
- b) Se possível, deixe a solução repousar durante algum tempo (mesmo até ao período seguinte do laboratório). Com tempo suficiente, algumas soluções assentam por si próprias. É claro que isto pode não ser prático.
- c) Para volumes pequenos, utilize uma centrifugadora, se tiver uma disponível. Uma centrífuga acelera o processo de sedimentação autónoma de uma emulsão. Lembre-se de que uma centrífuga precisa de estar equilibrada, caso contrário pode balançar para fora da bancada. Divida as soluções em partes iguais, colocando tubos de igual volume opostos dentro da centrífuga.
- d) Se uma emulsão se formar porque as duas camadas têm densidades semelhantes, tente alterar a densidade de cada camada para as tornar mais diferentes. Para ajudar a clarificar uma emulsão, tente diminuir a densidade da camada superior ou aumentar a densidade da camada inferior. Por exemplo, se ocorrer uma emulsão com acetato de etilo (camada superior) e uma solução aquosa (camada inferior), adicione um pouco de NaCl. O NaCl dissolver-se-á na camada aquosa e aumentará a densidade da solução aquosa. Em alternativa, adicionar mais acetato de etilo, que diluirá a camada orgânica e diminuirá a sua densidade. Como último recurso, adicionar um pouco de pentano, que se misturará com a camada orgânica superior e diminuirá a sua densidade (o pentano é um dos solventes orgânicos menos densos). A adição de pentano é utilizada como um esforço final, uma vez que irá afetar negativamente a capacidade da camada orgânica para extrair compostos algo polares.
Se ocorrer uma emulsão com uma solução aquosa (camada superior) e diclorometano (camada inferior), adicionar um pouco de água de uma garrafa de esguicho para diluir a camada superior e diminuir a sua densidade. Este método funcionou bem para clarificar a emulsão da Fig. 13 c, como mostra a Fig. 13 d. - c) Tentar diminuir a solubilidade de um componente no outro. Um método consiste em adicionar NaCl ou NH4Cl ao funil de separação, que se dissolve na camada aquosa e diminui a capacidade dos compostos orgânicos se dissolverem em água ("salting out").
Extração ácido-base
ExtraçãoÁcido-Base
- G.Patton
- 2
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/threads/extraction.553/
Como funcionam.
Uma modificação das extracções discutidas anteriormente neste capítulo consiste em realizar uma reação química na ampola de decantação para alterar a polaridade e, consequentemente, a partição de um composto nas camadas aquosa e orgânica. Um método comum é a realização de uma reação ácido-base, que pode converter alguns compostos de formas neutras para formas iónicas (ou vice-versa).
Por exemplo, imagine-se que uma mistura de ácido benzoico e ciclo-hexano é dissolvida num solvente orgânico, como o acetato de etilo, numa ampola de decantação. Para separar os componentes, pode tentar-se uma lavagem com água para remover o ácido benzoico, mas este não é particularmente solúvel em água devido ao seu anel aromático não polar, e apenas pequenas quantidades seriam extraídas para a camada aquosa (Fig.14 a).
Por exemplo, imagine-se que uma mistura de ácido benzoico e ciclo-hexano é dissolvida num solvente orgânico, como o acetato de etilo, numa ampola de decantação. Para separar os componentes, pode tentar-se uma lavagem com água para remover o ácido benzoico, mas este não é particularmente solúvel em água devido ao seu anel aromático não polar, e apenas pequenas quantidades seriam extraídas para a camada aquosa (Fig.14 a).
A separação de uma mistura de ácido benzoico e ciclo-hexano é, no entanto, possível através de uma lavagem com uma base, como o NaOH. Devido à sua natureza ácida, o ácido benzoico pode sofrer uma reação com NaOH da seguinte forma, resultando no sal carboxilato de benzoato de sódio.
As propriedades de solubilidade dos ácidos carboxílicos são substancialmente diferentes dos seus correspondentes sais de carboxilato. O salicilato de sódio é cerca de 350 vezes mais solúvel em água do que o ácido salicílico, devido ao seu carácter iónico (Fig.15), e é bastante insolúvel em solventes orgânicos como o éter dietílico.
Por conseguinte, uma lavagem com NaOH converteria o ácido benzoico na sua forma iónica de carboxilato, que seria então mais solúvel na camada aquosa, permitindo que o benzoato de sódio fosse extraído para a camada aquosa. O ciclo-hexano permaneceria na camada orgânica, uma vez que não tem afinidade com a fase aquosa, nem pode reagir com o NaOH de forma alguma. Desta forma, é possível separar uma mistura de ácido benzoico e ciclo-hexano (Fig.14 b). A camada aquosa pode ser posteriormente acidificada com HCl(aq), se desejado, para converter o ácido benzoico de volta à sua forma neutra.
Lavagens com bicarbonato de sódio
Pode ser utilizada uma extração ácido-base para extrair ácidos carboxílicos da camada orgânica para a camada aquosa. Como foi discutido na secção anterior, o NaOH pode ser utilizado para converter um ácido carboxílico na sua forma iónica de carboxilato, mais solúvel em água. No entanto, se a mistura contiver um composto desejado que possa reagir com o NaOH, deve ser utilizada uma base mais suave, como o bicarbonato de sódio. Ocorre uma reação semelhante.
Lavagens com bicarbonato de sódio
Pode ser utilizada uma extração ácido-base para extrair ácidos carboxílicos da camada orgânica para a camada aquosa. Como foi discutido na secção anterior, o NaOH pode ser utilizado para converter um ácido carboxílico na sua forma iónica de carboxilato, mais solúvel em água. No entanto, se a mistura contiver um composto desejado que possa reagir com o NaOH, deve ser utilizada uma base mais suave, como o bicarbonato de sódio. Ocorre uma reação semelhante.
Uma diferença na utilização da base NaHCO3 em vez de NaOH é que o subproduto ácido carbónico (H2CO3) pode decompor-se em água e gás dióxido de carbono. Ao agitar uma solução ácida com bicarbonato de sódio numa ampola de decantação, deve ter-se o cuidado de agitar suavemente e ventilar com mais frequência para libertar a pressão do gás.
Um exemplo de uma reação que utiliza frequentemente a lavagem com bicarbonato de sódio no trabalho é uma reação de esterificação de Fischer. Para demonstrar, o ácido benzoico foi refluxado em etanol juntamente com ácido sulfúrico concentrado para formar benzoato de etilo (Fig.16 a e b). Uma placa de TLC da mistura de reação a 1 hora de refluxo mostrou ácido carboxílico residual não reagido (Fig.16 c), o que não é invulgar devido à energia da reação.
Um exemplo de uma reação que utiliza frequentemente a lavagem com bicarbonato de sódio no trabalho é uma reação de esterificação de Fischer. Para demonstrar, o ácido benzoico foi refluxado em etanol juntamente com ácido sulfúrico concentrado para formar benzoato de etilo (Fig.16 a e b). Uma placa de TLC da mistura de reação a 1 hora de refluxo mostrou ácido carboxílico residual não reagido (Fig.16 c), o que não é invulgar devido à energia da reação.
O ácido carboxílico residual pode ser removido do produto éster desejado utilizando uma extração ácido-base numa ampola de decantação. Uma lavagem com bicarbonato de sódio converte o ácido benzoico na sua forma mais solúvel em água, o benzoato de sódio, extraindo-o para a camada aquosa (Fig. 17). Adicionalmente, o bicarbonato de sódio neutraliza o ácido catalítico nesta reação.
O bicarbonato de sódio é preferível ao NaOH neste processo, uma vez que é uma base muito mais fraca; a lavagem com NaOH pode causar a hidrólise do produto éster.
Misturas de Ácidos e Bases
Como foi discutido anteriormente, as propriedades ácido-base dos compostos podem ser utilizadas para extrair seletivamente determinados compostos de misturas. Esta estratégia pode ser alargada a outros exemplosMisturas de Ácidos e Bases
Extração de Bases
Os compostos básicos, como as aminas, podem ser extraídos de soluções orgânicas agitando-os com soluções ácidas para os converter em sais mais solúveis em água. Desta forma, podem ser extraídos de uma camada orgânica para uma camada aquosa.Extração de ácidos carboxílicos vs. fenóis
Como discutido anteriormente, os ácidos carboxílicos podem ser extraídos de uma camada orgânica para uma camada aquosa, agitando-os com soluções básicas, o que os converte nos seus sais mais solúveis em água.
Como discutido anteriormente, os ácidos carboxílicos podem ser extraídos de uma camada orgânica para uma camada aquosa, agitando-os com soluções básicas, o que os converte nos seus sais mais solúveis em água.
Uma reação semelhante ocorre com os fenóis (PhOH), que também podem ser extraídos para uma camada aquosa de NaOH (Fig.18 a).
No entanto, os fenóis são consideravelmente menos ácidos do que os ácidos carboxílicos e não são suficientemente ácidos para reagir completamente com NaHCO3, uma base mais fraca. Por isso, uma solução de bicarbonato pode ser usada para separar misturas de fenóis e ácidos carboxílicos (Fig.18 b).
No entanto, os fenóis são consideravelmente menos ácidos do que os ácidos carboxílicos e não são suficientemente ácidos para reagir completamente com NaHCO3, uma base mais fraca. Por isso, uma solução de bicarbonato pode ser usada para separar misturas de fenóis e ácidos carboxílicos (Fig.18 b).
Extração de compostos ácidos, básicos e neutros
As propriedades ácido-base discutidas anteriormente permitem que uma mistura contendo componentes ácidos (por exemplo, RCO2H), básicos (por exemplo, RNH2) e neutros seja purificada através de uma série de extracções, como resumido na Fig.19 (que utiliza um solvente orgânico menos denso que a água).
As propriedades ácido-base discutidas anteriormente permitem que uma mistura contendo componentes ácidos (por exemplo, RCO2H), básicos (por exemplo, RNH2) e neutros seja purificada através de uma série de extracções, como resumido na Fig.19 (que utiliza um solvente orgânico menos denso que a água).
ros


Assume-se que os leitores que realizam este tipo de experiências estão familiarizados com a realização de extracções simples e múltiplas. Nesta secção são descritas as diferenças entre os procedimentos gerais de extração e o processo resumido na Fig. 19.
1. Isolamento do componente ácido:
a) Quando o componente ácido se encontra na camada aquosa de um Erlenmeyer, pode ser convertido de novo no componente neutro através da adição de HCl 2M (aq) até a solução atingir um pH de 3-4 (determinado com papel de pH). Se estiverem presentes grandes quantidades de ácido, de modo a que a acidificação exija um volume demasiado grande de HCl 2M (aq), pode adicionar-se HCl concentrado (aq) gota a gota. As concentrações mais baixas de Hcl(aq) são menos perigosas, mas o aumento do volume da camada aquosa em grande quantidade afectaria a eficiência das extracções subsequentes e das etapas de filtração.
b) Após a acidificação, podem tomar-se duas direcções, dependendo do facto de o componente ácido ser sólido ou líquido.
1. Isolamento do componente ácido:
a) Quando o componente ácido se encontra na camada aquosa de um Erlenmeyer, pode ser convertido de novo no componente neutro através da adição de HCl 2M (aq) até a solução atingir um pH de 3-4 (determinado com papel de pH). Se estiverem presentes grandes quantidades de ácido, de modo a que a acidificação exija um volume demasiado grande de HCl 2M (aq), pode adicionar-se HCl concentrado (aq) gota a gota. As concentrações mais baixas de Hcl(aq) são menos perigosas, mas o aumento do volume da camada aquosa em grande quantidade afectaria a eficiência das extracções subsequentes e das etapas de filtração.
b) Após a acidificação, podem tomar-se duas direcções, dependendo do facto de o componente ácido ser sólido ou líquido.
- Se se formar um sólido após a acidificação do sal iónico, este pode ser recolhido por filtração por sucção. Este método só deve ser utilizado se forem observadas grandes quantidades de cristais de grandes dimensões. Se se formarem cristais finos (o que é bastante comum), estes irão obstruir o papel de filtro e interferir com a drenagem adequada. Se for observada apenas uma pequena quantidade de sólido em comparação com a quantidade teórica, é provável que o composto seja bastante solúvel em água e a filtração levaria a uma baixa recuperação.
- Se não se formar qualquer sólido após a acidificação (ou se se formarem cristais finos ou uma quantidade reduzida de sólido), extrair o componente ácido de volta para um solvente orgânico (×3). Como regra geral, utilizar nas extracções um terço da quantidade de solvente da camada original (por exemplo, se se utilizar 100 ml de solução aquosa, extrair com 33 ml de solvente orgânico de cada vez). Certifique-se de que arrefece primeiro a solução aquosa num banho de gelo antes da extração se a acidificação criar um calor percetível. Proceder a uma lavagem com salmoura (×1) se se utilizar éter etílico ou acetato de etilo, secar com um agente secante e remover o solvente por meio de um evaporador rotativo para deixar o componente ácido puro.
2. Isolamento do componente básico:
Utilizar um processo semelhante ao do isolamento do componente ácido, mas basificar a solução com NaOH 2M (aq) até obter um pH de 9-10, determinado com papel de pH.
3. Isolamento do componente neutro:
O componente neutro será o composto "restante" na camada orgânica. Para o isolar, lavar com salmoura (×1) se se utilizar éter dietílico ou acetato de etilo, secar com um agente secante e remover o solvente por meio de um evaporador rotativo para deixar o componente neutro puro.
Utilizar um processo semelhante ao do isolamento do componente ácido, mas basificar a solução com NaOH 2M (aq) até obter um pH de 9-10, determinado com papel de pH.
3. Isolamento do componente neutro:
O componente neutro será o composto "restante" na camada orgânica. Para o isolar, lavar com salmoura (×1) se se utilizar éter dietílico ou acetato de etilo, secar com um agente secante e remover o solvente por meio de um evaporador rotativo para deixar o componente neutro puro.
Conclusão.
Os métodos de extração são utilizados para extrair algumas substâncias de uma mistura. Estas substâncias podem ser bases, ácidos ou neutros (polares ou não polares). Por exemplo, este método é utilizado durante a produção de anfetaminas na fase de decantação: recolher a camada superior que contém a base de anfetamina em álcool. Pode secar-se um pouco com sulfato de magnésio anidro e a escória pode ser extraída adicionalmente com um solvente não polar (éter, benzeno, tolueno), sendo o solvente depois evaporado. A produção de mefedrona inclui a manipulação com funil de separação e extração. Além disso, a extração ácido-base é utilizada na purificação de algumas substâncias psicoactivas a partir de impurezas.
Attachments
Last edited: