Brain
Expert Pharmacologist
- Joined
- Jul 6, 2021
- Messages
- 264
- Reaction score
- 292
- Points
- 63
Psilocybín (3-[2-(dimetylamino)etyl]-1H-indol-4-yl dihydrogenfosfát) je alkaloid z rodiny tryptamínov, fosforylovaný derivát psilocínu, ktorý má psychedelické vlastnosti. Zo všetkých biologických zdrojov psilocybínu obsahujú najväčšie množstvo druhy húb rodov Psilocybe, Panaeolus, Stropharia, Gymnopilus, Inocybe; psilocybín však obsahuje aj približne 200 ďalších druhov húb. Čeľaď húb s obsahom psilocybínu, ktorá je známa pod názvom "magické huby", sa pre svoje halucinogénne účinky používala v histórii. Koncom 50. rokov 20. storočia Albert Hoffman zo spoločnosti Sandoz Laboratories izoloval a syntetizoval psychoaktívne zlúčeniny psilocybín a psilocín z húb obsahujúcich psilocybín. Spoločnosť Sandoz psilocybín predávala ako indocybín na základné psychofarmakologické a terapeutické klinické skúšky. V súčasnosti sú druhy Psilocybe známe v Ázii, Austrálii, Spojených štátoch, Kanade, Mexiku, Strednej a Južnej Amerike, Afrike a Európe. Existuje veľká miera dôkazov, že druhy obsahujúce psilocybín sa začali vyskytovať v Afrike a Európe, ako aj náznaky, že Psilocybe sa vyskytovali v Starom svete pred vznikom moderných ľudí. Huby obsahujúce psilocybín možno nájsť vo voľnej prírode alebo vypestovať v kontrolovanom prostredí z výtlačkov spór. Popularita psilocybínu rýchlo rástla v 60. rokoch 20. storočia. V roku 1970 bol zaradený do zoznamu I, čo viedlo k výraznému obmedzeniu výskumu psilocybínu. Nedávne predbežné štúdie psilocybínu však ukázali perspektívy jeho použitia pri liečbe obsedantno-kompulzívnej poruchy, závislosti od alkoholu, veľkej depresívnej poruchy a depresie u pacientov v terminálnom štádiu rakoviny. Psilocybín je v Spojených štátoch podľa zákona o kontrolovaných látkach z roku 1971 zaradený do zoznamu I, a preto sa ročne môže vyrobiť len obmedzené množstvo. Napriek svojmu štatútu látky zaradenej do zoznamu I bol psilocybín od 60. rokov 20. storočia populárnou rekreačnou drogou, a hoci jeho užívanie po zaradení medzi kontrolované látky oslablo, rekreačné užívanie pokračuje. Väčšina ostatných vyspelých krajín klasifikovala psilocybín a huby obsahujúce psilocybín tiež ako nelegálne. Hlavnou výnimkou z tejto všeobecnosti je Holandsko, ktoré má právnu medzeru umožňujúcu pestovanie, predaj a požívanie psychoaktívnych "hľuzoviek" obsahujúcich psilocybín. Na mnohých miestach boli zistené skoré dôkazy o užívaní šamanmi v Strednej a Južnej Amerike. Moderné štúdium sa začalo koncom 50. rokov 20. storočia etnomykológom R. Gordonom Wassonom a pokračovalo slávnymi výskumníkmi psychedelických látok Timothym Learym, Ralphom Metznerom a Ramom Dassom na Harvardovej univerzite, Albertom Hofmannom v laboratóriách Sandoz, Terrencom McKennom a Jonathanom Ottom v 60. a začiatkom 70. rokov 20. storočia. Záujem psychiatrov a psychológov v 50. rokoch 20. storočia nasledoval vďaka jeho vnímanému potenciálu ako nástroja na skrátenie psychoterapie. Výskum, ktorý sa zaujímal o psychedelickú liečbu závislostí, sa začal už v 50. rokoch 20. storočia. Často sa pozorovali prenikavé účinky, ktoré pomáhali pri vytriezvení, čo podnietilo Humphryho Osmonda, aby zaviedol termín "psychedelikum" ako spôsob, ako opísať schopnosti tejto triedy drog "prejaviť myseľ"." Väčšina klinických výskumov sa uskutočnila v 60. rokoch 20. storočia, pričom sa často používala syntetická verzia indocybinu.
Syntéza pcilocybínu
Syntéza pcilocínu
Psilocybín bol nájdený vo viac ako 100 druhoch húb, z ktorých mnohé patria do rodu Psilocybe. Alkaloid psilocybín v rode Inocybeacede sa objavuje medzi 10 a 20 mya a je pravdepodobné, že približne v tom čase sa objavil aj psilocybín v rode Psilocybe. V súčasnosti sú známe druhy rodu Psilocybe v Ázii, Austrálii, Spojených štátoch, Kanade, Mexiku, Strednej a Južnej Amerike, Afrike a Európe. Existuje veľká miera dôkazov o tom, že druhy obsahujúce psilocybín začali vznikať v Afrike a Európe, ako aj náznaky, že Psilocybe sa v Starom svete vyskytovali ešte pred vznikom moderných ľudí. Huby obsahujúce psilocybín možno nájsť vo voľnej prírode alebo vypestovať v kontrolovanom prostredí z odtlačkov spór, ktoré sa vytvárajú tak, že sa klobúk známej huby položí na list voskovaného papiera a spóry sa nechajú spadnúť na papier, čím sa vytvorí jedinečný odtlačok huby. Hoci je druhý spôsob podstatne bežnejší a oveľa bezpečnejší, niektorí používatelia stále vyhľadávajú "magické huby" vo voľnej prírode. Nebezpečenstvo nesprávnej identifikácie je stále prítomné a je to chyba, na ktorú sú náchylní aj tí najskúsenejší mykológovia. Nesprávna identifikácia môže viesť k omylu, na ktorý sú náchylní aj tí najskúsenejší mykológovia. Nesprávna identifikácia môže viesť k rôznym situáciám, od miernych ťažkostí až po smrť. Náhla smrť sa najčastejšie vyskytuje u amatérskych mykológov, ktorí hľadajú huby obsahujúce psilocybín a ďalší typ psychoaktívnej huby všeobecne známej ako "Muchotrávka" (Amanita muscaria), čo je ikonický červeno-biely bodkovaný klobúk huby často vídaný v rozprávkach (namiesto psilocybínu obsahuje A. muscaria psychoaktívne látky muscimol a kyselinu ibotenio.) Bohužiaľ, viaceré druhy Amanita sú smrteľné, vrátane výstižne pomenovaných "čiapočka smrti" (Amanita phalloides) a "ničivý anjel" (Amanita virosa), ktoré môžu vyzerať veľmi podobne ako Amanita muscaria a príbuzné druhy. Odkaz a používanie "magických húb" je viditeľné v celej ranej histórii a pokračuje až do modernej doby. Rané dôkazy o používaní šamanmi v Strednej a Južnej Amerike boli identifikované na mnohých miestach. Moderné štúdium sa začalo koncom 50. rokov 20. storočia etnomykológom R. Gordonom Wassonom a pokračovalo slávnymi psychedelickými výskumníkmi Timothym Learym, Ralphom Metznerom a Ramom Dassom na Harvardovej univerzite, Albertom Hofmannom v laboratóriách Sandoz, Terrencom McKennom a Jonathanom Ottom v 60. a začiatkom 70. rokov 20. storočia. Záujem psychiatrov a psychológov v 50. rokoch 20. storočia nasledoval vďaka jeho vnímanému potenciálu ako nástroja na skrátenie psychoterapie. Výskum, ktorý sa zaujímal o psychedelickú liečbu závislostí, sa začal už v 50. rokoch 20. storočia. Často sa pozorovali prenikavé účinky, ktoré pomáhali pri vytriezvení, čo podnietilo Humphryho Osmonda, aby zaviedol termín "psychedelikum" ako spôsob, ako opísať schopnosti tejto triedy drog "meniť myseľ".
Štruktúra psilocybínu a ďalších indolalkylamínových halucinogénov je podobná endogénnemu neurotransmiteru serotonínu, hormónu melatonínu a predpokladanému endogénnemu psychedelickému N, N-dimetyltryptamínu. Všetky pochádzajú z tej istej zlúčeniny - tryptamínu. Psilocybín (O-fosforyl-4-hydroxy-N, N-dimetyltryptamín) a jeho aktívny defosforylovaný metabolit psilocín (N, N-dimetyltryptamín) štrukturálne patria do skupiny tryptamínových/indolamínových halucinogénov a sú štrukturálne príbuzné serotonínu. Ekvimolárna dávka k 1 mol psilocínu je 1,4 mol psilocybínu. Substitúcia indolového jadra v polohe 4 pravdepodobne zohráva podstatnú úlohu pri jeho halucinogénnych účinkoch. Psilocybín a psilocín v čistej forme sú biele kryštalické prášky. Zatiaľ čo psilocybín je rozpustný vo vode, psilocín je na druhej strane rozpustnejší v tukoch. Psilocín sa však môže riediť aj v okyslenom vodnom roztoku a v dimetylsulfoxide (DMSO; do 100 mM). Okrem toho sú obe látky rozpustné v metanole a etanole, ale takmer nerozpustné v petroléteri a chloroforme. Obe drogy sú nestabilné na svetle (najmä vo forme roztokov), ich stabilita pri nízkych teplotách v tme v inertnej atmosfére je veľmi dobrá. Psilocybín je termolabilná zlúčenina, rozpustná vo vode, metanole, etanole, ale je nerozpustná v organických rozpúšťadlách. Sama o sebe má mimoriadne nízku aktivitu; pôsobí najmä ako prodrug psilocínu. Hodnoty pKa sa pohybujú od 1,3 do 6,5. Pri vystavení ultrafialovému žiareniu sa narúša jeho stabilita v roztoku, čo spôsobuje oxidáciu. Rozpustný v 120 častiach vriaceho metanolu; ťažko rozpustný v etanole; prakticky nerozpustný v chloroforme, benzéne, tlak pár - 1,9X10-12 mm Hg pri 25 °C. Molekulová hmotnosť je 285,25; má amoniakálnu chuť, bod topenia 224 °C, pH 5,2 v 50 % vody etanolu, TDLo 75 mkg/kg pri intramuskulárnom podaní u človeka, TDLo 60 mkg/kg pri perorálnom podaní u človeka, LD50 280 mg/kg pri intravenóznom podaní u potkanov. Psilocybín sa považuje za látku, ktorá v porovnaní s psilocínom slabo preniká cez hematoencefalickú bariéru. Je to spôsobené rozdielom vo vodíkových väzbách, ktoré spôsobujú, že tento je viac lyofilný, čo uľahčuje prechod cez hematoencefalickú bariéru. Pri vizuálnom skúmaní sa purifikovaný psilocybín a psilocín dajú rozlíšiť. Jeden má vzhľad bieleho alebo takmer bieleho ihličkového kryštálu, druhý tvorí olejovitý tmavohnedý až čierny.
Právny status.
Vláda v roku 1968 uzákonila zákaz držby psilocybínu a psilocínu. V roku 1970 boli psilocybín a psilocín zaradené do zoznamu drog I. V USA Denver, Oakland, Chicago, Ann Arbor a Santa Cruz dekriminalizovali držbu magických húb, ale predaj húb je stále zakázaný. V roku 2020 Oregon legalizoval psilocybín a District of Columbia dekriminalizoval užívanie magických húb. Predaj a preprava psilocybínu z Rakúska je nezákonná. Držba bola dekriminalizovaná a pestovanie je legálne, pokiaľ huby nie sú určené na konzumáciu. Osoby prichytené pri prechovávaní húb určených na osobnú potrebu môžu byť požiadané, aby sa podrobili bezplatnej liečbe. V Portugalsku sú psilocybínové huby nezákonné, ale dekriminalizované. Od osôb prichytených s množstvom určeným na osobné použitie sa môže vyžadovať, aby absolvovali rehabilitáciu alebo terapiu. V Holandsku sú psilocybínové huby vo forme hľuzoviek legálne. V súlade s politikou OSN je psilocybín v Taliansku nezákonný; psilocybínové huby sú však dekriminalizované. Predaj a získavanie pestovateľských súprav a spór je legálne, ale dôsledkom prichytenia s hubami môžu byť administratívne tresty, napríklad strata vodičského preukazu. Španielsko dekriminalizovalo osobnú držbu a konzumáciu psilocybínových húb, zatiaľ čo samotný psilocybín zostáva nezákonný. Pestovanie a predaj sú nezákonné a legálnosť spór a súprav na pestovanie je nejasná. Britské Panenské ostrovy povoľujú držbu a pestovanie psilocybínových húb. Hoci ich predaj alebo preprava sú nezákonné (ale nevymáhateľné). Držanie, predaj, preprava a pestovanie psilocybínových húb sú na Jamajke legálne. Na Jamajke sa psilocybínové huby otvorene predávajú. V Brazílii je držanie, predaj, preprava a pestovanie magických húb legálne. Psilocybín a psilocín sú uvedené na zozname nelegálnych látok, samotné huby sa však za nelegálne nepovažujú. Držanie magických húb je v Mexiku nezákonné, hoci sa tam neuplatňuje, ak sú magické huby v domorodých kultúrach. Pestovanie húb je nezákonné, pokiaľ sa huby nepestujú vo voľnej prírode. Predaj a preprava sú nezákonné. Magické huby sú legálne na Samoe. Od roku 2018 sú nelegálne vo Vietname.
V súčasnosti sú klasifikované ako látka zaradená do zoznamu I. Vedci z Univerzity Johna Hopkinsa tvrdia, že psilocybínové huby by mali byť preradené zo zoznamu I do zoznamu IV. V roku 2019 mesto Oakland v Kalifornii odhlasovalo dekriminalizáciu magických húb len mesiac po tom, ako sa tak rozhodol Denver v štáte CO. V Kalifornii prebieha snaha o dekriminalizáciu psilocybínových húb na celoštátnej úrovni, pričom túto zmenu podporujú mnohé psychedelické osvetové a advokačné skupiny. Okrem toho zákonodarný zbor štátu Oregon zvažuje prijatie zákona o dekriminalizácii psilocybínových húb a ponúkaní licencií na ich pestovanie. Veľká časť tohto sľubného výskumu sa uskutočňuje vďaka Multidisciplinárnej asociácii psychedelických štúdií (MAPS). MAPS v súčasnosti vykonáva lekársky výskum s MDMA, psilocybínom, LSD, marihuanou, ibogainom a ayahuascou. Ďalšia organizácia, Heffter Research Institute, sa špecializuje na výskum psilocybínu. Medzi členmi správnej rady Heffter Research Institute je spoluzakladateľ Dr. David Nichols, všeobecne uznávaný výskumník, profesor a odborník na chémiu halucinogénov. Medzi ďalších výskumníkov patrí Dr. Dennis McKenna, uznávaný spisovateľ, etnofarmakológ, psychonaut a brat zosnulého Terrenca McKennu, a Dr. Roland Griffiths, ktorý na univerzite Johnsa Hopkinsa robí fenomenálny výskum psilocybínu a závislosti. V súčasnosti prebieha aj niekoľko medzinárodných štúdií o psilocybíne. Beckleyho nadácia so sídlom vo Veľkej Británii sponzoruje niektoré z najprogresívnejších výskumov psilocybínu v súčasnosti. Nadáciu Beckley Foundation založila v roku 1996 Amanda Fieldingová - sama uznávaná psychonautka a vedkyňa - a v súčasnosti spolu s MAPS a Heffterom sponzoruje výskum neurobiológie psilocybínu. Tento výskum prebieha na Imperial College London s Dr. Davidom Nuttom a Dr. Robin Carhart-Harrisovou, ktorí v minulosti publikovali výskum psilocybínu, konkrétne "Entropický model mozgu". Heffter tiež sponzoruje štúdiu vo Švajčiarsku s názvom "Účinky psilocybínu na pozornosť, vnímanie a poznávanie". Podobne MAPS sponzoruje štúdiu s názvom "Experimentálne štúdie účinkov psilocybínu na binokulárnu inverziu hĺbky, binokulárnu rivalitu" v Nemecku.
Farmakokinetika a farmakodynamika.
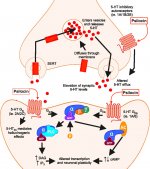
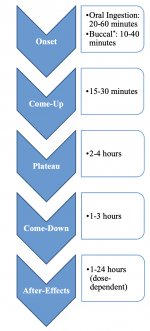
Po požití psilocybín podlieha biotransformácii v pečeni, kde sa neznámym enzýmom defosforyluje na psilocín. Po vstupe psilocínu do systémového krvného obehu sa dostáva do mozgu, kde má psychoaktívny účinok. Podľa iných údajov sa psilocybín po perorálnom podaní rýchlo defosforyluje v kyslom prostredí žalúdka alebo pôsobením alkalickej fosfatázy (a iných nešpecifických esteráz) v čreve, obličkách a pravdepodobne v krvi za vzniku fenolovej zlúčeniny psilocínu, ktorá môže ľahko prechádzať cez hematoencefalickú bariéru. Je pozoruhodné, že relatívna účinnosť psilocínu a psilocybínu je takmer totožná s pomerom molekulovej hmotnosti týchto zlúčenín. Blokovanie alkalickej fosfotázy kompetitívnymi substrátmi β-glycerofosfátu vyrovnáva príznaky intoxikácie. Psilocín prechádza oboma fázami metabolizmu. Prvá fáza metabolizmu zahŕňa oxidačnú deamináciu psilocínu na 4-hydroxyindol-3-acetaldehyd katalyzovanú pečeňovou monoaminooxidázou alebo aldehyddehydrogenázou s následnou oxidáciou na kyselinu 4-hydroxyindol-3-octovú, 4-hydroxyindol-3-acetaldehyd a 4-hydroxytryptofol. Enzýmy, ktoré sa zúčastňujú na týchto procesoch, neboli identifikované. Preto môžu inhibítory MAO zosilniť halucinogénne účinky psilocybínu, podobne ako etanol môže zosilniť trip, pretože jeho primárny metabolit acetaldehyd reaguje in vivo s endogénnymi amínmi, v dôsledku čoho vznikajú inhibítory MAO tetrahydroizochinolíny a β-karbolíny. Keďže psilocybín vyvoláva kompetitívnu inhibíciu MAO (ktorá metabolizuje serotonín), zvyšuje sa hladina serotonínu v mozgu a súčasne sa znižuje koncentrácia 5-HIAA. Takisto existuje z hľadiska klinických účinkov nevýznamná metabolická cesta, ktorá zahŕňa oxidáciu, ktorej výsledkom je tvorba tmavomodrého produktu, ktorý má štruktúru o-chinónu alebo iminochinónu. Túto cestu katalyzujú hydroxyindoloxidázy (ceruloplazmín, oxidáza obsahujúca meď z plazmy cicavcov, a cytochrómoxidáza). Uvedené metabolity vykazujú nevýznamnú fyziologickú aktivitu. Pri parenterálnom podávaní psilocybínu majú rovnakú úlohu tkanivové fosfatázy a tie v obličkách patria medzi najaktívnejšie. Vzhľadom na to, že kompetitívna blokáda defosforylácie blokuje psychotropný účinok psilocybínu, je zrejmé, že psilocín je hlavným aktívnym metabolitom psilocybínu. Do 5 hodín od perorálneho podania psilocybínu je až 80 % psilocínu prítomného v krvi ako konjugát O-glukuronidu a vylučuje sa močom v nezmenenej forme. Glukuronidácia hydroxylovej skupiny na psilocínO-glukuronid je dôležitým stupňom detoxikácie, preto enzymatická hydrolýza predlžuje čas detekcie vo vzorkách moču. Zatiaľ čo psilocín podlieha rozsiahlej glukoronidácii prostredníctvom UDP-glukuronozyltransferáz (UGT)1A10 v tenkom čreve, UGT1A9 sa na glukoronidácii podieľa najmä po jeho absorpcii do krvi. N-glukuronidácia sa v tomto prípade nevyskytuje v celom metabolizme. Okrem uvedenej cesty podlieha samotný psilocín aj oxidačnému metabolizmu. Demetylácia a desaminácia 4-hydroxyindol-3-yl-acetaldehydu (4-HIA) s následnou oxidáciou (pravdepodobne pečeňovou aldehyddehydrogenázou a monoaminooxidázou) vedie k vzniku kyseliny 4-hydroxyindol-3-octovej (4-HIAA) a 4-hydroxytryptofolu (4-HT). Tieto nevýznamné metabolity (približne 4 % sa rozpadajú vyššie opísaným spôsobom) možno zistiť v ľudskej krvnej plazme. Tretí spôsob metabolizmu psilocínu zahŕňa oxidáciu hydroxyindoloxidázami, ako bolo uvedené vyššie. Psilocín sa distribuuje do všetkých tkanív vrátane mozgu a vylučuje sa do 24 hodín. Väčšia časť sa vylúči počas prvých 8 hodín (približne 65 % močom a 15 - 20 % žlčou a stolicou). V moči ho možno zistiť v priebehu 2 týždňov. Najvyššie koncentrácie psilocínu sú v neokortexe, hipokampe, extrapyramídovom motorickom systéme a retikulárnej formácii. U ľudí možno psilocybín a psilocín zistiť v krvnej plazme po 20 - 40 minútach od perorálneho podania. Maximálne koncentrácie sa dosiahnu za 80 - 100 minút a možno ich zistiť do šiestich hodín. Doba polčasu psilocínu v krvnej plazme je približne 2/5 hodiny po perorálnom podaní a 1,23 hodiny - po parenterálnom podaní. Ako už bolo uvedené, približne 80 % psilocínu v plazme je v konjugovanej forme. Psilocín (90 - 97 %) a psilocybín (3 - 10 %) možno zistiť v moči v nezmenenej forme alebo konjugované s kyselinou glukoronovou. Eliminačný polčas je približne 50 minút, eliminačná konštanta je 0,307/h. Väčšina látky sa vylúči počas prvých troch hodín po perorálnom podaní a úplne sa vylúči močom do 24 hodín. Kompletná metabolická cesta psilocybínu bola preskúmaná len veľmi málo a stále je potrebné zhromaždiť veľa informácií, aby sa určili presné mechanizmy, ktoré sa podieľajú na jeho metabolizme.
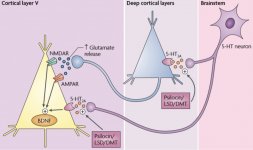
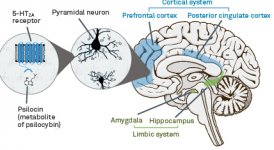
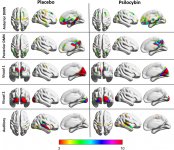
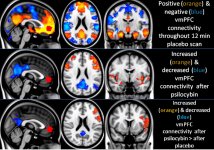
Farmakológia psilocybínu je veľmi zložitá a nie je dostatočne preskúmaná. Psilocybín môže mať pravdepodobne vlastnú nevýznamnú aktivitu; väčšinou však pôsobí ako prodrug psilocínu. Ten ľahko prechádza cez hematoencefalickú bariéru a má tam svoj psychoaktívny účinok. Hlavné väzobné miesta sú zhrnuté v tabuľke vyššie. Psilocín má najsilnejšiu väzbu na serotonínové receptory: (5-HT1D,2B,2C,5,6,7), má tiež stredný väzbový potenciál na miesta serotonínových receptorov (5-HT1A, 1B, 2A). Okrem serotonínových receptorov má psilocín určitú afinitu k histamínovým receptorom prvého typu (H1), alfa-2A a -2B receptorom a k dopamínovým receptorom tretieho typu (D3). V neurónoch exprimujúcich receptor 5HT2A, ale nie v neurónoch s knockoutom 5HT2A, psilocybín zvyšuje expresiu skorých génov (erg-1, erg-2, c-fos, jun-B, period-1, gpcr-26, fra-1, N- 10, I-κBα) a znižuje expresiu sty-kinázy. Netreba dodávať, že presná signálna dráha vedúca od receptora k aktivácii skorých génov zatiaľ nie je známa. Vzhľadom na to, že aj nehalucinogénny lisurid aktivuje c-fos, je pravdepodobné, že expresia c-fos odráža len zvýšenú aktivitu neurónov, zatiaľ čo expresia egr-1/ egr-2 je špecifická pre halucinogénny účinok. Gonzales-Meaeso vysvetlil túto selektivitu "teóriou agonistického obchodovania s receptorovou signalizáciou", kde halucinogény aktivujú heterokomplex 5HT2A/mGlu2 receptorov a odlišné G proteíny v porovnaní s nehalucinogénnymi agonistami 5-HT2A. Túto hypotézu podporuje štúdia, v ktorej myši s knockoutovaným génom pre receptor mGlu2 nevykazujú žiadne správanie pri zášklboch hlavy. Bolo dokázané, že psilocilín inhibuje sodík-dependentný serotonínový transportér (SERT), čo vedie k zvýšeniu koncentrácie serotonínu. Serotonín po uvoľnení zostáva v synaptickej štrbine, čo v konečnom dôsledku vedie k opakovanej aktivácii serotonergných postgangliových neurónov. Pokiaľ ide o hodnotenie väzbovej afinity k receptorom, sú zoradené nasledovne: 5HT2B > 5HT1D > D1 > 5HT1E > 5HT1A > 5HT5A > 5HT7 > 5HT6 > D3 > 5HT2C > 5HT1B > 5HT2A. Dokázala sa aj väzba na imidazolínové receptory prvého typu. Je zaujímavé, že afinita psilocybínu k ľudským 5-НТ2А receptorom je 15-krát vyššia ako u potkanov. Agonizmus 5НТ2А receptorov a aktivácia nadmerného počtu týchto receptorov a podtypov receptorov sú zodpovedné za jedinečné a intenzívne psychedelické účinky spôsobené psilocybínom. Predtým sa veľa diskutovalo o tom, či sú za izolované halucinácie po požití húb obsahujúcich psilocybín zodpovedné 5-НТ2А alebo 5-НТ2С receptory. Štúdie ukázali, že 5-НТ2А-antagonisti halucinácie potláčajú, zatiaľ čo antagonisti 5-НТ2С nemajú ani zosilnenie halucinácií, ani ich vyrovnávajúci účinok. Agonizmus na receptory 5-НТ2А sa teda spája s celkovou excitáciou neurónov, zlepšením pamäti a učenia, kontrakciami hladkého svalového tkaniva ciev, gastrointestinálneho traktu a bronchov, určitou protizápalovou aktivitou, zvýšenou produkciou prolaktínu a oxytocínu, adrenokortikotropného hormónu a renínu pri aktivácii systému renín-angiotenzín-aldosterón. Pokiaľ ide o aktiváciu 5-НТ2С psilocínom, dochádza k aktivácii proopiomelanokortínu (prekurzora α-, β- a γ-melanocyty stimulujúceho hormónu a adrenokortikotropného hormónu) a uvoľňovaniu kortizolu. Tieto hormóny zabezpečujú zvýšenú chuť do jedla, citlivosť na inzulín, metabolizmus glukózy, stabilizáciu na anxiogénne a stresové podnety. Psilocín pôsobí ako čiastočný agonista receptorov 5-НТ1А, ktoré sú exprimované najmä v rafe jadre (DRN) a mediálnom rafe jadre (MRN), ktoré sa nachádzajú v blízkosti strednej línie mozgového kmeňa pozdĺž celého jeho rostrálneho rozšírenia, ako somatodendritické autoreceptory. MRN podporuje aktiváciu procesov konsolidácie pamäti a je projektované do hipokampu, zatiaľ čo VRN je jedno z najväčších serotonínergických jadier v ľudskom mozgu, ktoré zabezpečuje významné množstvo serotonínergickej inervácie predného mozgu; okrem toho má MRN projekčné vlákna v amygdale a hypotalame, čo súvisí s reguláciou cirkadiánneho rytmu a viacerých typov buniek, ktoré produkujú katecholamín a substanciu-P. DRN a MRN sú bohaté na presynaptické receptory 5-НТ1А a psilocín má niekoľkonásobne (5 - 6-krát) silnejší účinok najmä na svojich presynaptických miestach v porovnaní s postsynaptickými. Táto preferencia sa vysvetľuje vysokou hustotou receptorov 5-НТ1А, ktoré sa nachádzajú v týchto oblastiach. Tento určitý typ receptorov, ktorý sa nachádza na telách serotonínergických buniek rafeovej zóny, sa nenachádza napríklad na postsynaptických membránach. V štúdiách pomocou fMRI sa zistilo, že psilocybín výrazne znižuje prietok krvi a žilové okysličenie mozgu. Táto skutočnosť koreluje s jeho subjektívnym účinkom a výrazne znižuje pozitívne spojenie medzi dvoma kľúčovými štrukturálnymi uzlami (mPFC и PCC). Je dokázané, že psilocybín zvyšuje metabolizmus glukózy v mozgu. Takisto sa niektorými experimentmi dokázalo, že DMN je kľúčová aj na udržanie kognitívnej integrácie a obmedzení za normálnych podmienok. Po naviazaní psilocínu na presynaptické receptory 5-НТ1А oblasti DRN potláča účinky tejto oblasti, pričom základné bunky zostávajú neporušené a zvyšujú sympatikovú aktivitu spojenú s locus coeruleus. Iné lokalizácie receptorov 5-НТ2А preukazujú rýchly pokles aktivity tohto receptora a zníženie ich hustoty pri aktivácii psilocínom. Psilocybín teda nemá toleranciu na inhibíciu účinku DRN. Je dôležité poznamenať, že selektívne agonisty receptorov 5-НТ1а nie sú vo svojej podstate halucinogénne, majú však úlohu pri ovplyvňovaní inhibičných účinkov, ktoré sa identifikujú v DRN.
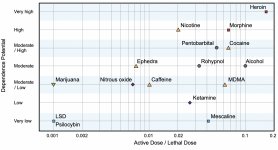
Hoci dopamínový receptor druhého typu zohráva významnú úlohu pri vzniku halucinácií pri rôznych duševných ochoreniach, predpokladá sa, že nemá žiadny aktívny a nepriamy vzťah k pôsobeniu psilocínu. Túto hypotézu ako prví dokázali Vollenweider a kol. keď zistili, že podávanie galoperidolu (agonistu D2R) neoslabuje psychoaktívne účinky psilocínu. Aj keď sa dopaminergné účinky psilocínu považujú za minimálne, v porovnaní s inými podtypmi dopamínových receptorov má relatívne vysokú väzbovú schopnosť na D3-receptor. Napriek tomu, že účinky sprostredkované cez D3R boli málo preskúmané, pravdepodobne prispievajú k charakteristickým psychoaktívnym vlastnostiam psilocybínu a jeho schopnosti spôsobovať závislosť. Chemický prekurzor psilocínu, 4-acetoxy-N,N-dimetyltryptamín, má fosforyloxyskupinu nahradenú acetoxyskupinou. Metabolizuje sa rovnakým spôsobom ako fosforyloxy skupina a táto modifikácia umožňuje obísť niektoré metabolické procesy prvej fázy. Napriek tomu, že psilacetín je identickou farmakologickou substitúciou ako psilocybín, veľa užívateľov uvádza, že medzi nimi je istý nevýznamný, ale rozoznateľný rozdiel. Psilacetín sa často opisuje ako látka s rýchlejším nástupom účinku, ktorý nezahŕňa úzkosť a nevoľnosť (ktoré sa spájajú s užívaním psilocybínu v dôsledku nedostatku chitínu, zvyčajne obsiahnutého v hubách) a má kratšie trvanie. Je známe, že medián letálnej dávky u potkanov je približne 293 mg/kg, čo naznačuje obrovské terapeutické okno psilocínu. Tachyfylaxia, rýchla desenzibilizácia na látku, ktorá vedie k zníženiu fyziologického účinku, je jav, ktorý sa spája s užívaním mnohých halucinogénov. Tolerancia na psilocybín sa začína vyvíjať hneď po prvom jednorazovom použití. Mechanizmus zahŕňa fyziologickú odpoveď na nadmernú stimuláciu 5-НТ2А receptorov rýchlym znížením počtu receptorových miest a znížením hustoty receptorov na bunke. Vo všeobecnosti sa predpokladá, že tieto receptorové miesta sa vrátia na päťdesiat percent pôvodnej úrovne za 3-7 dní od prvého použitia. Na pôvodné množstvo sa vrátia za 4 týždne v závislosti od dávky a dĺžky opakovaného používania. Okrem toho existuje skrížená tolerancia medzi indolalkylamínovými a fenylalkylamínovými triedami halucinogénov.
Attachments
-
 aDjgnEic18.jpg572.2 KB · Views: 1,591
aDjgnEic18.jpg572.2 KB · Views: 1,591 -
 sRHGpjI9LU.jpg788.9 KB · Views: 1,561
sRHGpjI9LU.jpg788.9 KB · Views: 1,561 -
 TQv018fRJh.jpg128.6 KB · Views: 922
TQv018fRJh.jpg128.6 KB · Views: 922 -
lF1rOfpW8k.jpg2.6 MB · Views: 948
-
 TSkYz5Gq6P.jpg363.8 KB · Views: 1,718
TSkYz5Gq6P.jpg363.8 KB · Views: 1,718 -
 sPlo2QDBMe.jpg551.6 KB · Views: 1,688
sPlo2QDBMe.jpg551.6 KB · Views: 1,688 -
 AxRV2Hfutv.jpg697.8 KB · Views: 1,710
AxRV2Hfutv.jpg697.8 KB · Views: 1,710 -
 b2Ma0wsVTD.jpg607.2 KB · Views: 1,775
b2Ma0wsVTD.jpg607.2 KB · Views: 1,775 -
 QtXjIHo7PJ.jpg438.5 KB · Views: 1,580
QtXjIHo7PJ.jpg438.5 KB · Views: 1,580 -
 rI0YMKgE6z.jpg1.1 MB · Views: 1,719
rI0YMKgE6z.jpg1.1 MB · Views: 1,719 -
 Q1ueUSGlFN.jpg614.4 KB · Views: 1,723
Q1ueUSGlFN.jpg614.4 KB · Views: 1,723
Last edited by a moderator:
