Mefedron (4-metilmetkatinon), metamfetamin ile yakın yapısal ve mekanik benzerliklere sahip bir β-ketoamfetamin uyarıcı kötüye kullanım ilacıdır. Mephedrone ile ilişkili en güçlü eylemlerden biri, dopamin (DA) salınımını uyarma ve dopamin taşıyıcısı (DAT) ile etkileşimi yoluyla geri alımını engelleme yeteneğidir. Mefedron DA sinir uçlarında toksisiteye neden olmasa da, bir DAT engelleyici olarak hizmet etme yeteneği, diğer DAT inhibitörleri gibi metamfetamin kaynaklı nörotoksisiteye karşı koruma sağlayabilir. Bu olasılığı test etmek için, fareler nörotoksik bir metamfetamin rejiminin (2 saat aralıklarla 2,5 veya 5,0 mg/kg'lık 4 enjeksiyon) her enjeksiyonundan önce mefedron (10, 20 veya 40 mg/kg) ile muamele edilmiştir. Striatumdaki DA sinir uçlarının bütünlüğü DA, DAT ve tirozin hidroksilaz seviyeleri ölçülerek değerlendirilmiştir. Farklı metamfetamin dozlarıyla ilişkili orta ila şiddetli DA toksisitesi, herhangi bir mephedron dozu tarafından önlenmemiş, aslında önemli ölçüde artmıştır. Mefedron ve metamfetamin ile kombine tedavinin neden olduğu hipertermi, tek başına her iki ilaçtan sonra görülenle aynıydı. Mefedron ayrıca amfetamin ve MDMA'nın DA sinir uçları üzerindeki nörotoksik etkilerini de artırmıştır. Buna karşılık, nomifensin metamfetamin kaynaklı nörotoksisiteye karşı koruma sağlamıştır. Mefedron metamfetamin nörotoksisitesini artırdığından, mevcut sonuçlar DAT ile diğer tipik DAT inhibitörlerinden farklı bir şekilde etkileşime girdiğini düşündürmektedir. Mefedronun tek başına DA sinir uçları üzerindeki nispeten zararsız etkileri, sıklıkla birlikte kullanılan ilaçlarla potansiyel olarak tehlikeli bir etkileşimi maskeleyerek nörotoksisitenin artmasına neden olur.
Mephedrone (4-methylmethcathinone) bir katinon türevi ve metamfetamin ve 3,4-metilendioksi-metamfetaminin (MDMA) yapısal analoğudur. Mefedron, metilon, butilon ve 3,4-metilendioksipirovaleron (MDPV) gibi diğer bileşiklerle birlikte "banyo tuzlarının" psikoaktif bileşenlerinden biridir. β-ketoamfetaminler, gizli laboratuvarlarda metamfetamin ve MDMA sentezi için gerekli öncüllerin oldukça kısıtlı bir şekilde bulunabilmesi ve buna bağlı olarak saflıklarının azalması nedeniyle artan oranlarda kötüye kullanılmaktadır (Winstock ve ark. 2011b, Brunt ve ark. 2011). β-ketoamfetaminlerin kötüye kullanımı artmaya devam ettikçe, yan etkilerinin listesi kardiyovasküler komplikasyonlar, ajitasyon, uykusuzluk, psikoz ve depresyonu içerecek şekilde büyümüştür (Schifano ve ark. 2011, Prosser ve Nelson 2012).
Metamfetamin ve MDMA'nın kimyasal türevleri olarak, β-ketoamfetaminlerin merkezi sinir sistemi üzerinde bu eski ilaçlarla aynı etkilere sahip olması şaşırtıcı değildir. Örneğin, bu ilaçlar dopamin (DA) ve serotonin (5-HT) taşıyıcılarını (sırasıyla DAT ve SERT) bloke eder (Cozzi vd. 1999, Rothman vd. 2003, Fleckenstein vd. 2000, Lopez-Arnau vd. 2012) ve in vitro (Kalix ve Glennon 1986, Gygi vd. 1997, Rothman vd. 2003) ve in vivo (Gygi vd. 1997, Kehr vd. 2011) monoamin salınımını uyarırlar. Metkatinon, triptofan hidroksilaz ve tirozin hidroksilaz (TH) aktivitesinde kalıcı azalmalara ve DA ve 5-HT'nin tükenmesine neden olur (Gygi ve ark. 1997, Gygi ve ark. 1996, Sparago ve ark. 1996). Yoksun metkatinon kullanıcılarında yapılan PET görüntüleme çalışmaları, DA terminallerinin kaybına işaret eden striatal DAT yoğunluğunun azaldığını ortaya koymuştur (McCann ve ark. 1998). DA salınımının eş zamanlı uyarılması ve alımının engellenmesi, metamfetamin ile ilişkili nörotoksisitenin altında yatan kritik unsurları yansıtmaktadır (Kuhn ve ark. 2008, Yamamoto ve Bankson 2005, Cadet ve ark. 2007, Fleckenstein ve ark. 2007).
Biz (Angoa-Perez ve ark. 2012) ve diğerleri (Baumann ve ark. 2012, Hadlock ve ark. 2011) yakın zamanda mefedronun metamfetamin ve MDMA gibi nörotoksisiteye neden olabileceği ihtimalini araştırdık. Şaşırtıcı bir şekilde, mefedron striatumun DA sinir uçları için toksik değildi (Hadlock ve ark. 2011, Baumann ve ark. 2012, Angoa-Perez ve ark. 2012). Mefedronun 5-HT sinir uçlarına zarar verip vermediği konusu, bir çalışmanın olumlu etkileri belgelemesi (Hadlock ve ark. 2011), diğerinin ise olumsuz olması (Baumann ve ark. 2012) nedeniyle belirsizliğini korumaktadır. Mefedronun DA sinir uçları üzerindeki nispeten iyi huylu etkisi ışığında ve bir DAT engelleyici olarak özellikleri göz önüne alındığında, DA nöronal sistemini metamfetaminin nörotoksik etkilerinden, amfonelik asit (Pu ve ark. 1994, Schmidt ve Gibb 1985, Marek ve ark. 1990) ve nomifensin (Poth ve ark. 2012) gibi diğer DAT engelleyicilerde olduğu gibi koruyabileceğini varsaydık. Şu anda mefedronun metamfetaminin nörotoksisitesini önemli ölçüde artırdığını bildiriyoruz. Bu etki, genellikle mefedron ile birlikte kullanılan ilaçlar olan amfetamin ve MDMA'ya kadar uzanmaktadır (Feyissa ve Kelly 2008, Schifano ve ark. 2011). Bu şaşırtıcı sonuçlar mefedronun kötüye kullanımına yeni bir ışık tutmakta ve bu β-ketoamfetaminin bu ince ve tehlikeli özelliğinin tanınmasına aciliyet kazandırmaktadır.
Materyaller ve yöntemler
İlaçlar ve Reaktifler
Mefedron hidroklorür ve 3,4-metilendioksimetamfetamin (MDMA) NIDA Araştırma Kaynakları İlaç Tedarik Programından temin edilmiştir. (+) Metamfetamin hidroklorür, nomifensin maleat, d-amfetamin sülfat, pentobarbital, DA ve tüm tamponlar ve HPLC reaktifleri Sigma-Aldrich'ten (St. Louis, MO, ABD) satın alınmıştır. Bisinçoninik asit protein tahlil kitleri Pierce'den (Rockford, IL, ABD) temin edilmiştir. Sıçan TH'ye karşı poliklonal antikorlar daha önce tarif edildiği şekilde üretilmiştir (Kuhn ve Billingsley 1987). Sıçan DAT'a karşı monoklonal antikorlar Dr. Roxanne A. Vaughan (Kuzey Dakota Üniversitesi, Grand Forks, ND, ABD) tarafından cömertçe sağlanmıştır. HRP-konjuge anti-IgG ikincil antikorlar Jackson ImmunoResearch Laboratories, Inc. (West Grove, PA, ABD) tarafından sağlanmıştır.
Hayvanlar
Deney sırasında 20-25 g ağırlığında olan dişi C57BL/6 fareler (Harlan, Indianapolis, IN, ABD), ışık (12 saat aydınlık/karanlık) ve sıcaklık kontrollü bir odada büyük ayakkabı kutusu kafeslerinde kafes başına 5 adet olacak şekilde barındırılmıştır. Nörotoksik amfetaminlerin nöronal hasarına karşı çok hassas oldukları bilindiğinden ve metamfetamin nörotoksisitesiyle ilgili önceki çalışmalarımızla tutarlılığı korumak için dişi fareler kullanılmıştır (Thomas ve ark. 2010, Thomas ve ark. 2008, Thomas ve ark. 2009). Farelerin yiyecek ve suya serbest erişimi vardı. Wayne Eyalet Üniversitesi Kurumsal Bakım ve Kullanım Komitesi hayvan bakımı ve deneysel prosedürleri onaylamıştır. Tüm prosedürler ayrıca NIH Laboratuvar Hayvanlarının Bakımı ve Kullanımı Kılavuzu ile de uyumluydu.
Farmakolojik, fizyolojik ve davranışsal prosedürler
Fareler, her enjeksiyon arasında 2 saat ara ile 10, 20 veya 40 mg/kg'lık 4 enjeksiyondan oluşan tıkınırcasına bir rejim kullanılarak mefedron ile tedavi edilmiştir. Bu tıkınırcasına tedavi rejimi, ikame edilmiş amfetaminleri ve katinon türevlerini enjekte etmek için kullanıldığında, kapsamlı DA sinir ucu hasarına yol açmaktadır. Şu anda kullanılan mefedron dozlarının DA sinir uçları için toksik olmadığı daha önce gösterilmiştir (Angoa-Perez ve ark. 2012). Fareler metamfetamin (4X 2,5 veya 5 mg/kg), amfetamin (4X 5 mg/kg) veya MDMA (4X 20 mg/kg) ile tek başına veya mefedron ile birlikte muamele edilmiştir. İki ilaçla muamele edildiğinde, farelere 4 metamfetamin, amfetamin veya MDMA enjeksiyonunun her birinden 30 dakika önce bir mefedron enjeksiyonu yapılmıştır. Kontroller, tek başına veya diğer amfetaminlerle kombinasyon halinde mefedron için kullanılan aynı programda fizyolojik salin enjeksiyonları aldı. Bir DAT inhibitörünün metamfetamin toksisitesi üzerindeki etkilerinin kontrolü için farelere her bir metamfetamin enjeksiyonundan (4X 5 mg/kg) 30 dakika önce nomifensin (4X 5 mg/kg) uygulanmıştır. Tüm enjeksiyonlar i.p. yolla yapılmıştır. Fareler son ilaç tedavisinden 2 gün sonra amfetaminle ilişkili nörotoksisite maksimuma ulaştığında feda edilmiştir. Vücut sıcaklığı, Bio Medic Data Systems, Inc. (Seaford, DE, ABD) tarafından sağlanan IPTT-300 implante edilebilir sıcaklık transponderleri kullanılarak telemetri yoluyla izlenmiştir. Sıcaklıklar, ilk METH enjeksiyonundan 20 dakika önce başlayarak her 60 dakikada bir non-invaziv olarak kaydedilmiş ve Bio Medic'in DAS-5001 konsol sistemi kullanılarak 9 saat boyunca devam etmiştir.
Striatal DA içeriğinin belirlenmesi
Striatal doku tedaviden sonra beyinden iki taraflı olarak diseke edildi ve -80°C'de saklandı. Dondurulmuş dokular tartılmış ve 4°C'de 10 hacim 0,16 N perklorik asit içinde sonike edilmiştir. Çözünmeyen protein santrifüjleme yoluyla uzaklaştırılmış ve DA, daha önce metamfetamin için tarif edildiği gibi elektrokimyasal saptamalı HPLC ile belirlenmiştir (Thomas ve ark. 2010, Thomas ve ark., 2009).
İmmünoblotlama ile TH ve DAT protein seviyelerinin belirlenmesi
İlaç tedavilerinin striatal TH ve DAT seviyeleri üzerindeki etkileri, striatal DA sinir uçlarına toksisitenin bir indeksi olarak immünoblotlama ile belirlendi. Fareler tedaviden sonra dekapitasyon ile feda edildi ve striatum iki taraflı olarak diseke edildi. Doku -80°C'de saklanmıştır. Dondurulmuş doku 95°C'de %1 SDS içinde sonikasyon ile parçalandı ve çözünmeyen materyal santrifüj ile çöktürüldü. Protein biksinoninik asit yöntemiyle belirlendi ve eşit miktarda protein (70 μg/lane) SDS-poliakrilamid jel elektroforeziyle çözüldü ve ardından nitroselüloza elektroblotlandı. Blotlar Tween 20 (%0,1 v/v) ve %5 yağsız kuru süt içeren Tris tamponlu salin içinde oda sıcaklığında 1 saat süreyle bloke edilmiştir. TH (1:1000) veya DAT'a (1:1000) karşı primer antikorlar blotlara eklenmiş ve 4°C'de 16 saat inkübasyona bırakılmıştır. Reaksiyona girmemiş antikorları uzaklaştırmak için blotlar Tris tamponlu salin içinde 3X yıkandı ve ardından HRP-konjuge anti-IgG sekonder antikor (1:4000) ile oda sıcaklığında 1 saat inkübe edildi. İmmünoreaktif bantlar gelişmiş kemilüminesans ile görselleştirildi ve TH- ve DAT-reaktif bantların göreceli yoğunlukları Kodak Image Station (Carestream Molecular Systems, Rochester, NY, ABD) ile görüntülenerek belirlendi ve ImageJ yazılımı (NIH) kullanılarak nicelleştirildi.
Veri analizi
Metamfetamin ve mefedronun DA, DAT ve TH üzerindeki doz etkilerini analiz etmek için iki yönlü ANOVA'lar gerçekleştirilmiştir. İlaç tedavilerinin striatal DA, TH ve DAT içeriği üzerindeki etkileri, tek yönlü ANOVA ve ardından Tukey'in çoklu karşılaştırma testi ile anlamlılık açısından test edilmiştir. İlaç tedavilerinin zaman içinde çekirdek vücut sıcaklığı üzerindeki sonuçları, tedaviden sonra ayrı zamanlarda sıcaklıktaki farklılıkların önemini belirlemek için iki yönlü ANOVA ve ardından Bonferroni testi kullanılarak analiz edildi. Farklılıklar p < 0.05 ise anlamlı kabul edilmiştir. Tüm istatistiksel analizler Windows için GraphPad Prism sürüm 5.02 kullanılarak gerçekleştirilmiştir (GraphPad Software, San Diego, CA, ABD, www.graphpad.com).
Şuraya git
Sonuçlar
Mefedronun metamfetamin kaynaklı nörotoksisite üzerindeki etkileri
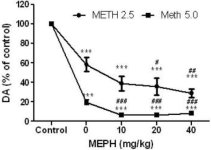
DA sinir ucu toksisitesine neden olmadığı bilinen dozlarda (10, 20 veya 40 mg/kg) mefedron (Angoa-Perez ve ark. 2012) her metamfetamin enjeksiyonundan 30 dakika önce uygulanmıştır. Metamfetamin, striatumun DA sinir uçlarında orta (4X 2,5 mg/kg) veya ciddi (4X 5 mg/kg) hasara neden olan dozlarda uygulanmıştır (Thomas ve ark. 2004, Thomas ve ark. 2010). Şekil 1'de sunulan sonuçlar, metamfetamin dozunun (F1,40 = 66.60, p < 0.0001) ve mefedron dozunun (F4,40 = 131.3, p < 0.0001) striatumdaki DA seviyeleri üzerindeki ana etkilerinin iki yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. Mefedronun 2.5 mg/kg (F4,22 = 35.96, p < 0.001) veya 5.0 mg/kg metamfetamin (F4,17 = 953.9, p < 0.0001) ile birlikte verilmesinin ana etkisi de tek yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm tedaviler, ilgili kontrole kıyasla DA'da önemli ölçüde daha fazla azalmaya neden olmuştur (tümü için p < 0.0001). Şekil 1 ayrıca 20 (p < 0.01) ve 40 mg/kg (p < 0.001) mefedron dozlarının 2.5 mg/kg metamfetaminin DA üzerindeki tükenme etkilerini önemli ölçüde artırdığını, tüm mefedron dozlarının ise 5.0 mg/kg metamfetaminin DA seviyeleri üzerindeki etkilerini önemli ölçüde artırdığını göstermektedir (tümü için p < 0.0001).
Şekil 1
Mefedronun striatal DA'da metamfetamin kaynaklı azalmalar üzerindeki etkileri. Fareler, her 2,5 (-) veya 5,0 mg/kg (■) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiş ve 2 gün sonra HPLC ile striatal DA seviyelerinin belirlenmesi için feda edilmiştir. Veriler grup başına 5-7 fare için ortalama ± SEM'dir. Bazı hata çubukları sembollerin boyutunu geçemeyecek kadar küçüktür ve görünür değildir. ***p < 0.001 vs kontroller ve #p < 0.01, ##p < 0.001 veya ###p < 0.0001 vs ilgili metamfetamin dozu (Tukey'in çoklu karşılaştırma testi).
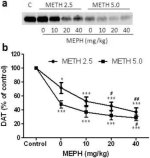
Şekil 2a, mefedronun immünoblotlama ile belirlendiği üzere DAT seviyelerinde metamfetamin kaynaklı azalmaları önemli ölçüde artırdığını göstermektedir. İmmünoblotlar sayısallaştırılmış ve DA sonuçlarıyla uyumlu olarak, metamfetamin dozunun (F1,92 = 9.48, p < 0.001) ve mefedron dozunun (F4,92 = 37.56, p < 0.0001) striatumdaki DAT seviyeleri üzerindeki ana etkileri iki yönlü ANOVA ile oldukça anlamlı bulunmuştur (Şekil 2b). Mefedronun 2.5 mg/kg (F4,56 = 15.55, p < 0.0001) veya 5.0 mg/kg metamfetamin (F4,39 = 24.84, p < 0.0001) ile birlikte verilmesinin ana etkisi de tek yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm tedaviler, ilgili kontrole kıyasla DAT'ta önemli ölçüde daha fazla azalmaya neden olmuştur (yalnızca 2,5 mg/kg metamfetamin için p < 0,01; diğer tüm tedaviler için p < 0,0001). Şekil 2b ayrıca 20 mg/kg (p < 0.01) ve 40 mg/kg (p < 0.001) mefedron dozlarının 2.5 mg/kg metamfetaminin neden olduğu DAT düşüşlerini önemli ölçüde artırdığını, sadece 40 mg/kg mefedron dozunun 5.0 mg/kg metamfetaminin DAT düşüşleri üzerindeki etkilerini önemli ölçüde artırdığını (p < 0.01) göstermektedir.
Şekil 2
Mefedronun striatal DAT'ta metamfetamin kaynaklı azalmalar üzerindeki etkileri. Fareler, her 2,5 (●) veya 5,0 mg/kg (■) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiş ve 2 gün sonra immünoblotlama yoluyla striatal DAT seviyelerinin belirlenmesi için feda edilmiştir (a). Blotlar ImageJ kullanılarak nicelleştirilmiştir ve veriler grup başına 10-12 fare için ortalama ± SEM'dir (b). *p < 0.01 veya ***p < 0.0001 vs kontrol (C) ve #p < 0.01 veya ##p < 0.001 vs ilgili metamfetamin dozu (Tukey'in çoklu karşılaştırma testi).
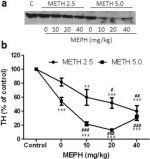
Şekil 3a, mefedronun immünoblotlama ile belirlendiği üzere TH seviyelerinde metamfetamin kaynaklı azalmaları önemli ölçüde artırdığını göstermektedir. İmmünoblotlar nicelleştirilmiştir ve DA ve DAT için yukarıdaki sonuçlarla uyumlu olarak, metamfetamin dozunun (F1,81 = 47.89, p < 0.0001) ve mefedron dozunun (F4,81 = 63.57, p < 0.0001) ana etkileri iki yönlü ANOVA ile oldukça anlamlıdır (Şekil 3b). Mefedronun 2,5 mg/kg (F4,34 = 12,98, p < 0,0001) veya 5,0 mg/kg metamfetamin (F4,49 = 99,16, p < 0,0001) ile birlikte verilmesinin ana etkisi de tek yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm muameleler, ilgili kontrole kıyasla TH'de önemli ölçüde daha fazla azalmaya neden olmuştur (2,5 mg/kg metamfetamin + 10 mg/kg mephedrone için p < 0,001; diğer tüm kombinasyonlar için p < 0,0001); TH seviyelerini önemli ölçüde değiştirmeyen tek başına 2,5 mg/kg metamfetamin hariç (yani, toksisite yok). Şekil 3b ayrıca 20 mg/kg (p < 0.01) ve 40 mg/kg (p < 0.001) mefedron dozlarının 2.5 mg/kg metamfetaminin neden olduğu TH düşüşlerini önemli ölçüde artırdığını ve her üç mefedron dozunun da 5.0 mg/kg metamfetaminin TH düşüşleri üzerindeki etkilerini önemli ölçüde (p < 0.0001) artırdığını göstermektedir.
Şekil 3
Mefedronun striatal TH'de metamfetamin kaynaklı azalmalar üzerindeki etkileri. Fareler her 2,5 (●) veya 5,0 mg/kg (■) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiş ve 2 gün sonra immünoblotlama (a) ile TH'nin striatal seviyelerinin belirlenmesi için feda edilmiştir. Lekeler ImageJ kullanılarak nicelleştirilmiştir ve veriler grup başına 10-12 fare için ortalama ± SEM'dir (b). Bazı hata çubukları sembollerin boyutunu geçemeyecek kadar küçüktür ve görünür değildir. **p < 0.001 veya ***p < 0.0001 vs kontrol (C) ve #p < 0.01, ##p < 0.001 veya ##p < 0.0001) vs ilgili metamfetamin dozu (Tukey'in çoklu karşılaştırma testi).
Mefedronun metamfetamin kaynaklı hipertermi üzerindeki etkileri
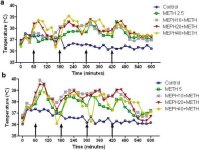
Metamfetamin gibi mefedron da önemli ölçüde hipertermiye neden olmaktadır (Hadlock ve ark. 2011, Baumann ve ark. 2012, Angoa-Perez ve ark. 2012). Her metamfetamin enjeksiyonundan 30 dakika önce mefedron verildiğinde, metamfetamin ve mefedron dozlarının (F1,300 = 11.99, p < 0.0001) zaman üzerindeki ana etkilerinin (F4,300 = 51.73, p < 0.0001) iki yönlü ANOVA ile oldukça anlamlı olduğu Şekil 4'te görülebilir. Zaman içinde 2.5 mg/kg metamfetamin (F4,120 = 41.44, p < 0.0001, panel a) (F30,120 = 3.84, p < 0.0001) veya 5.0 mg/kg metamfetamin (F4,120 = 78.09, p < 0.0001, panel b) (F30,120 = 9.98, p < 0.0001) ile birlikte verilen mefedronun ana etkileri de iki yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm tedaviler ilgili kontrollerden önemli ölçüde farklıydı (tüm tedaviler için p < 0.0001).
Şekil 4
Mefedronun metamfetamin kaynaklı hipertermi üzerindeki etkileri. Fareler, her 2,5 (a) veya 5,0 mg/kg (b) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiştir. Çekirdek sıcaklıkları, ilk metamfetamin enjeksiyonundan 60 dakika önce başlayan telemetri ile 20 dakika aralıklarla ölçülmüştür. 4 metamfetamin enjeksiyonu x ekseninde duran oklarla gösterilmiştir. Veriler grup başına 6-8 farenin ortalama vücut sıcaklığı olarak ifade edilmiştir. SEM'ler her zaman ortalamanın <%10'u kadardır ve anlaşılır olması için atlanmıştır.
Mefedronun amfetamin ve MDMA kaynaklı nörotoksisite üzerindeki etkileri
Mefedronun metamfetamin üzerindeki artırıcı etkilerinin diğer nörotoksik amfetaminlere genişletilip genişletilemeyeceğini test etmek için fareler bu β-ketoamfetamin (20 mg/kg) artı amfetamin (4X 5 mg/kg) veya MDMA (4X 20 mg/kg) ile muamele edilmiş ve sonuçlar Şekil 5'te sunulmuştur. Mefedronun kendisinin striatal DA, DAT veya TH'yi azaltmadığını hatırlayın (Angoa-Perez ve ark. 2012). İlacın ana etkisi (F5,27 = 27.18, p < 0.0001) DA azalmaları için tek yönlü ANOVA ile oldukça anlamlıydı (Şekil 5a). Şekil 5a'da ayrıca amfetamin (p < 0,001) veya MDMA (p < 0,001) ile tek başına veya mefedron ile kombinasyon halinde (her iki ilaç için p < 0,0001) yapılan tüm tedavilerin DA seviyelerini kontrolden önemli ölçüde düşürdüğü görülebilir. Mefedron, amfetamin (p < 0.01) veya MDMA'nın (p < 0.01) neden olduğu DA düşüşlerini önemli ölçüde artırmıştır. Şekil 5b, kombinasyon ilaç tedavilerinin striatumdaki DAT seviyeleri üzerindeki benzer etkilerini göstermektedir. İlacın ana etkisi (F4,49 = 42.63, p < 0.0001) DAT için tek yönlü ANOVA ile oldukça anlamlıydı. Şekil 5b'de amfetamin veya MDMA ile yapılan tüm uygulamaların kontrole kıyasla önemli ölçüde (hepsi için p < 0.0001) daha düşük olduğu da görülebilir. Mefedron ayrıca amfetamin veya MDMA'nın neden olduğu DAT azalmalarını önemli ölçüde artırmıştır (her iki durumda da p < 0.0001). Son olarak, Şek. 5c ilacın ana etkisinin (F4,50 = 75.06, p < 0.0001) TH'deki azalmalar için tek yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. Ayrıca Şekil 5c'de amfetamin veya MDMA ile yapılan tüm uygulamaların kontrole kıyasla önemli ölçüde (hepsi için p < 0.0001) daha düşük olduğu görülebilir. Mefedron ayrıca amfetamin veya MDMA'nın neden olduğu TH düşüşlerini önemli ölçüde artırmıştır (her iki durumda da p < 0.0001)
Şekil 5
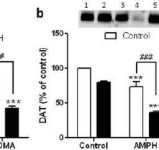
Mefedronun amfetamin veya MDMA kaynaklı DA sinir ucu nörotoksisitesi üzerindeki etkileri. Fareler, her 5.0 mg/kg amfetamin (AMPH) veya 20 mg/kg MDMA enjeksiyonundan 30 dakika önce 20 mg/kg mefedron (MEPH) ile muamele edilmiş ve (a) DA'nın striatal seviyelerinin HPLC ile belirlenmesi için tedaviden 2d sonra feda edilmiştir. (b) DAT ve (c) TH immünoblotlama ile belirlenmiş ve ImageJ kullanılarak blotlar nicelleştirilmiştir. DAT ve TH için temsili immünoblotlar sırasıyla (b) ve (c) panellerine ek olarak dahil edilmiştir ve her iki panel için tedaviler 1,5: kontrol; 2,6: MEPH; 3: AMPH; 4: AMPH + MEPH; 7: MDMA; ve 8: MDMA + MEPH ile gösterilmiştir. Veriler her gruptaki 5-12 fare için ortalama ± SEM'dir. **p < 0.001 veya ***p < 0.0001 vs kontrol ve #p < 0.01 veya ###p < 0.0001 vs AMPH veya MDMA (Tukey'in çoklu karşılaştırma testi).
Nomifensinin metamfetamin kaynaklı nörotoksisite üzerindeki etkileri
Bilinen kötüye kullanım veya nörotoksik potansiyeli olmayan güçlü bir DAT engelleyici olan nomifensin, metamfetamin kaynaklı nörotoksisiteye karşı koruma kabiliyeti ve metamfetamin, amfetamin ve MDMA'nın neden olduğu DA sinir uçlarına toksisite üzerindeki mefedron eylemlerinin aksine test edilmiştir. Şekil 6a'daki sonuçlar, ilacın DA seviyeleri üzerindeki ana etkisinin (F3,16 = 63,39, p < 0,0001) tek yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. Nomifensin tek başına DA seviyelerini değiştirmemiştir, ancak metamfetaminin neden olduğu azalma (p < 0.0001) nomifensin tarafından hafif ama önemli ölçüde tersine çevrilmiştir (p < 0.01). İlacın (F3,20 = 16.78, p < 0.0001) DAT seviyeleri üzerindeki ana etkisi, Şekil 6b'de gösterildiği gibi tek yönlü ANOVA ile oldukça anlamlıydı. Nomifensin DAT seviyelerini değiştirmemiş ancak metamfetaminin (p < 0.0001) neden olduğu striatal DAT azalmasına karşı kontrole kıyasla önemli bir koruma (p < 0.001) sağlamıştır. Son olarak, Şekil 6c ilacın TH seviyeleri üzerindeki ana etkisinin (F3,15 = 14.10, p < 0.0001) tek yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. DA ve DAT için görüldüğü gibi, metamfetaminin neden olduğu TH'deki azalma (p < 0.0001) nomifensin (p < 0.01) tarafından hafif ama önemli ölçüde önlenmiştir.
Şekil 6
Nomifensinin metamfetamin kaynaklı DA sinir ucu nörotoksisitesi üzerindeki etkileri. Fareler her 5.0 mg/kg metamfetamin (METH) enjeksiyonundan 30 dakika önce 5.0 mg/kg nomifensin (NOM) ile muamele edilmiş ve 2 gün sonra HPLC ile (a) DA'nın striatal seviyelerinin belirlenmesi için feda edilmiştir. (b) DAT ve (c) TH immünoblotlama ile belirlenmiş ve ImageJ kullanılarak blotlar nicelleştirilmiştir. DAT ve TH için temsili immünoblotlar sırasıyla (b) ve (c) panellerine ek olarak dahil edilmiştir. Veriler grup başına 5-7 fare için ortalama artı SEM'dir. ***p < 0.0001 vs kontrol (C) ve #p < 0.01 veya ##p < 0.001 vs tek başına metamfetamin (Tukey'in çoklu karşılaştırma testi).
Tartışma
Bu çalışmanın amacı, mefedronun metamfetaminin neden olduğu DA sinir ucu toksisitesini önleyip önlemeyeceğini belirlemekti. Metamfetamin ve MDMA ile kimyasal benzerliğine dayanarak, başlangıçta mefedronun DA nöronal sistemi üzerinde zararlı etkiler göstermesi bekleniyordu. Ancak, birkaç çalışma neredeyse eş zamanlı olarak mefedronun DA sinir uçları için toksik olmadığını ortaya koymuştur (Angoa-Perez ve ark. 2012, Baumann ve ark. 2012, Hadlock ve ark. 2011). Bu ilacın 5-HT nöronal sistemine zarar verip vermediği sorusu açık kalmaya devam etmektedir. Bir çalışma 5-HT sinir ucu işlevinde kalıcı azalmalar bildirirken (Hadlock ve ark. 2011), bir diğeri mephedrone'un hasara neden olmadığını bulmuştur (Baumann ve ark. 2012). Mefedron, DA sinir ucu ile, DAT ile etkileşimleri yoluyla gerçekten salınımı uyardığını ve DA yeniden alımını engellediğini düşündüren bir şekilde etkileşime girer. Metamfetaminin nörotoksik etki mekanizmasının kilit bir yönü, DAT aracılığıyla DA sinir uçlarına erişim sağlama ve DA homeostazını bozma yeteneğidir (Sulzer 2011). Metamfetamin nörotoksik kaskadındaki bu erken adım DAT'ın inhibisyonu ile önlenirse, toksisite önlenir (Pu ve ark. 1994, Poth ve ark. 2012, Marek ve ark. 1990, Schmidt ve Gibb 1985). Mefedronun diğer DAT inhibitörleriyle aynı koruyucu özelliğe sahip olabileceğini düşündük, ancak bunun yerine toksisitede önemli bir artış gözlemledik. Bu etkileşim, DA sinir uçlarında orta veya ciddi hasara neden olan iki farklı metamfetamin dozu (sırasıyla 4X 2,5 veya 5,0 mg/kg) kullanılarak görülmüştür. Mefedronun bu güçlendirici etkisi metamfetaminle sınırlı kalmamış ve genellikle mefedron ve diğer β-ketoamfetaminlerle birlikte kullanılan iki uyuşturucu olan amfetamin ve MDMA'ya kadar uzanmıştır (Feyissa ve Kelly 2008, Schifano ve ark. 2011, Kelly 2011). Bu nedenle, mefedron en azından striatumun DA sinir uçlarında toksisiteye neden olmamasına rağmen, diğer kötüye kullanım ilaçlarının nörotoksik etkilerini güçlendirmektedir. Bu yeni bulgu, mefedronun kötüye kullanımını daha da çarpıcı hale getirmelidir çünkü içsel nörotoksisitesinin olmaması onu zararsız gösterebilir.
Hipertermi, insanlarda metamfetamin (Greene ve ark. 2008) ve β-ketoamfetamin alımının yaygın olarak bildirilen bir akut yan etkisidir (Borek ve Holstege 2012, Prosser ve Nelson 2012). Metamfetamin gibi, β-ketoamfetamin ilaçlarının çoğu da kemirgenlerde çekirdek sıcaklığında önemli artışlara neden olmaktadır (Angoa-Perez ve ark. 2012, Hadlock ve ark. 2011, Baumann ve ark. 2012, Rockhold ve ark. 1997). Metamfetaminin neden olduğu hipertermi, morfolojik ve nöronal hasar verici etkilerine katkıda bulunabilirken, hiperterminin bu etkilerin doğrudan nedeni olması gerekmez (Kiyatkin ve Sharma 2009). Mefedron ve metamfetamin ile tedavi edilen farelerde çekirdek vücut sıcaklıklarını kaydettik ve kombine tedavinin sıcaklıkları tek başına her iki ilaçtan sonra görülen maksimum artışların ötesine yükseltmediğini gözlemledik. Metamfetamin vücut sıcaklığında doza bağlı bir artışa neden olmuş ve bu hipertermi test edilen tüm mephedrone doz aralığında değişmez olmuştur. Aslında, mephedrone tedavisinden sonra gözlenen vücut sıcaklığındaki enjeksiyon sonrası düşüş (Angoa-Perez ve ark. 2012) daha yüksek mephedrone artı metamfetamin dozlarında korunmuştur. İlacın neden olduğu hipertermi kombine ilaç tedavisi ile artmamış olsa da, nörotoksik etkiler katkı maddesidir. Bu nedenle, en azından mevcut durumda, metamfetaminin nörotoksik etkilerinin hipertermiden bağımsız bir şekilde mefedron tarafından artırılabileceği görülmektedir.
Mefedron, DAT işlevini açıkça inhibe eder ve DA'nın in vitro yeniden alımını engeller (Lopez-Arnau ve ark. 2012, Hadlock ve ark. 2011, Kehr ve ark. 2011, Martinez-Clemente ve ark. 2012, Cozzi ve ark. 1999). Mefedron, WIN-35,428'i DAT üzerindeki bağlanma bölgesinden uzaklaştırarak DA alımının rekabetçi bir inhibitörü olduğunu düşündürmektedir (Martinez-Clemente ve ark. 2012, Lopez-Arnau ve ark. 2012). Bu bağlamda mefedronun gücü metamfetamin (Cozzi ve ark. 1999) ve MDMA (Escubedo ve ark. 2011) ile çok benzerdir. Mefedronun DAT tarafından taşınıp taşınmadığı bilinmemektedir ancak metkatinon taşınmaktadır (Cozzi ve Foley 2003). DAT'a bağlanan ve DA alımını engelleyen nomifensin ve amfonelik asit, metamfetamin kaynaklı nörotoksisiteye karşı önemli ölçüde koruma sağlar (Pu ve ark. 1994, Marek ve ark. 1990, Schmidt ve Gibb 1985, Poth ve ark. 2012) ve DAT'tan yoksun fareler metamfetaminin nöronal toksisitesine dirençlidir (Fumagalli ve ark. 1998). Mefedronun nörotoksik olmadığını ve bir DAT engelleyicisi olduğunu bilmek, toksisiteyi önlemesi gerektiği tahminine yol açmaktadır. Nomifensini bu bağlamda pozitif bir kontrol olarak test ettik ve metamfetamin kaynaklı DA, DAT ve TH tükenmesine karşı koruduğunu doğruladık. Nomifensin ayrıca norepinefrin taşıyıcısını da inhibe eder (Brogden ve ark. 1979) ancak bu özellik mevcut sonuçları açıklayamaz çünkü mefedron dahil çoğu β-ketoamfetamin norepinefrin taşıyıcısını inhibe eder ve norepinefrin alımını engeller (Kelly 2011, Rothman ve ark. 2003, Cozzi ve ark. 1999, Sogawa ve ark. 2011, Lopez-Arnau ve ark. 2012). Mefedronun bazı farmakolojik etkilerinde 5-HT nöronal sisteminin rolü, bu ilacın MDMA gibi (Yamamoto ve ark. 1995) 5-HT2A reseptörleriyle etkileşimleri yoluyla striatal DA akışına neden olma kabiliyeti ışığında mümkündür (Lopez-Arnau ve ark. 2012, Martinez-Clemente ve ark. 2012). Mefedronun neden olduğu hiper-lokomosyon endojen 5-HT'ye bağlıdır (Lopez-Arnau ve ark. 2012) ve bu ilaç aynı zamanda 5-HT salınımını uyarır ve in vitro alımını engeller (Sogawa ve ark. 2011, Cozzi ve ark. 1999, Nagai ve ark. 2007, Hadlock ve ark. 2011, Lopez-Arnau ve ark. 2012, Martinez-Clemente ve ark. 2012) ve in vivo (Baumann ve ark. 2012, Kehr ve ark. 2011). Bununla birlikte, genetik olarak 5-HT'den yoksun farelerin nörotoksisiteye karşı duyarlılıklarını koruduklarını göstererek, en azından metamfetaminin DA nörotoksisitesinde endojen 5-HT'nin rolünü ekarte edebiliriz (Thomas ve ark. 2010).
Mefedron, metamfetamin nörotoksisitesini birkaç olası mekanizma ile artırabilir. İlk olarak, mefedron VMAT ile etkileşime girerek DA'nın presinaptik sinir ucunun sitoplazmasına sızmasına neden olabilir. DA'nın sitoplazmik havuzunu (yani ilaçla serbest bırakılabilir) artıran tedaviler metamfetamin nörotoksisitesini artırır (Thomas ve ark. 2008, Thomas ve ark. 2009, Schmidt ve ark. 1985). Bu mekanizma olası değildir çünkü metkatinon VMAT ile sadece zayıf bir şekilde etkileşime girer (Cozzi ve ark. 1999). İkinci olarak, mefedron artı metamfetamin kombinasyonu DA'nın veziküler olmayan salınımı üzerinde sinerjik bir etkiye sahip olabilir, ancak DAT veya SERT eksprese eden CHO hücrelerinin metilon artı metamfetamin ile muamelesinin DA veya 5-HT salınımı üzerinde ek bir etkiye sahip olmadığını gösteren sonuçlar ışığında bu olasılık da olası görünmemektedir (Sogawa ve ark. 2011). Üçüncüsü, mefedron DAT ile katkı toksisitesine katkıda bulunan yeni bir şekilde etkileşime girebilir. Metamfetamin ile birlikte metilonun DAT veya SERT eksprese eden CHO hücrelerinde sinerjik sitotoksisiteye neden olduğu, ancak taşıyıcılardan yoksun vahşi tip CHO hücrelerinde olmadığı gösterilmiştir (Sogawa ve ark. 2011). Bu çalışmalarda kültürlenmiş hücrelerde görülen sitotoksisite (yani LDH salınımı) metamfetaminin neden olduğu DA sinir uçlarındaki hasardan çok farklıdır, ancak bu mekanizma DAT için artan sitotoksisitede ilginç ancak tanımlanmamış bir rol önermektedir. Son olarak, mefedron metamfetamin metabolizmasını değiştirebilir. Mefedron, metamfetamin ve MDMA (Caldwell 1976) gibi öncelikle N-demetilasyon ile metabolize edilir (Meyer ve Maurer 2010). Bu mekanizmaya destek, metamfetamin ve MDMA'nın kendi birincil metabolitlerinin üretimini karşılıklı olarak inhibe ettiğinin ve ilaç plazma seviyelerini her iki ilacın tek başına uygulanmasından sonra görülenlerin üzerine çıkardığının gösterilmesinden gelmektedir (Kuwayama ve ark. 2012). Şu anda ve önceki çalışmamızda (Angoa-Perez ve ark. 2012) kullanılan mefedron dozları yüksek olmakla birlikte nörotoksik değildir ve insanlar tarafından kötüye kullanılan aralıkta yer almaktadır (McErath ve O'Neill 2011). Bu nedenle mefedron, metabolizmasını inhibe ederek metamfetaminin plazma seviyelerini artırmak için MDMA gibi hareket ediyor olabilir. Bu ikinci olasılığı doğrulamak için derinlemesine bir farmakokinetik analiz gerekecektir.
β-ketoamfetaminlerin kötüye kullanımı endişe verici bir oranda artmaktadır ve mefedron şu anda esrar, MDMA ve kokainden sonra en yaygın kullanılan ilaçlardan biridir (Morris 2010, Winstock ve ark. 2011b). Buna ek olarak, mephedrone insanlarda MDMA'ya kıyasla daha güçlü bir aşerme hissine neden olmaktadır (Brunt ve ark. 2011) ve mephedrone çeken kullanıcılar bunu kokainden daha fazla bağımlılık yapıcı olarak değerlendirmektedir (Winstock ve ark. 2011b). Mefedron insanlar tarafından tıkınırcasına tüketilir (yani "istifleme") ve genellikle esrar ve amfetamin psikostimülanlar gibi diğer uyuşturucularla birlikte alınır (Schifano ve ark. 2011, Fass ve ark. 2012, Winstock ve ark. 2011a, Kelly 2011, Torrance ve Cooper 2010). Mefedron, MDMA olarak satılan tabletlerde giderek daha fazla bulunmaktadır (Brunt ve ark. 2011) ve bu son uyuşturucunun saflığı düşmeye devam ettikçe kullanımı muhtemelen MDMA'yı geçecektir (Brunt ve ark. 2011, Tanner-Smith 2006, Teng ve ark. 2006). Mephedrone ve diğer "banyo tuzları" bileşenlerinin yaygın kötüye kullanım modellerine dayanarak, bu ilaçlar bilerek veya bilmeyerek amfetaminlerle birleştirildiğinde insanlarda ek sağlık risklerinin ortaya çıkıp çıkmayacağını düşünmek önemlidir. En azından mefedronun metamfetamin, amfetamin ve MDMA'nın neden olduğu striatumun DA sinir uçlarına yönelik nörotoksisiteyi önemli ölçüde artırdığını gösteren sonuçlarımız, bu β-ketoamfetaminin özellikle tehlikeli ve beklenmedik bir özelliğini ortaya koymaktadır.
Kullanılan kısaltmalar
5-HT serotonin
DA dopamin
DAT DA taşıyıcı
MDMA 3,4-metilendioksimetamfetamin
TH tirozin hidroksilaz
VMAT veziküler monoamin taşıyıcı
Mephedrone (4-methylmethcathinone) bir katinon türevi ve metamfetamin ve 3,4-metilendioksi-metamfetaminin (MDMA) yapısal analoğudur. Mefedron, metilon, butilon ve 3,4-metilendioksipirovaleron (MDPV) gibi diğer bileşiklerle birlikte "banyo tuzlarının" psikoaktif bileşenlerinden biridir. β-ketoamfetaminler, gizli laboratuvarlarda metamfetamin ve MDMA sentezi için gerekli öncüllerin oldukça kısıtlı bir şekilde bulunabilmesi ve buna bağlı olarak saflıklarının azalması nedeniyle artan oranlarda kötüye kullanılmaktadır (Winstock ve ark. 2011b, Brunt ve ark. 2011). β-ketoamfetaminlerin kötüye kullanımı artmaya devam ettikçe, yan etkilerinin listesi kardiyovasküler komplikasyonlar, ajitasyon, uykusuzluk, psikoz ve depresyonu içerecek şekilde büyümüştür (Schifano ve ark. 2011, Prosser ve Nelson 2012).
Metamfetamin ve MDMA'nın kimyasal türevleri olarak, β-ketoamfetaminlerin merkezi sinir sistemi üzerinde bu eski ilaçlarla aynı etkilere sahip olması şaşırtıcı değildir. Örneğin, bu ilaçlar dopamin (DA) ve serotonin (5-HT) taşıyıcılarını (sırasıyla DAT ve SERT) bloke eder (Cozzi vd. 1999, Rothman vd. 2003, Fleckenstein vd. 2000, Lopez-Arnau vd. 2012) ve in vitro (Kalix ve Glennon 1986, Gygi vd. 1997, Rothman vd. 2003) ve in vivo (Gygi vd. 1997, Kehr vd. 2011) monoamin salınımını uyarırlar. Metkatinon, triptofan hidroksilaz ve tirozin hidroksilaz (TH) aktivitesinde kalıcı azalmalara ve DA ve 5-HT'nin tükenmesine neden olur (Gygi ve ark. 1997, Gygi ve ark. 1996, Sparago ve ark. 1996). Yoksun metkatinon kullanıcılarında yapılan PET görüntüleme çalışmaları, DA terminallerinin kaybına işaret eden striatal DAT yoğunluğunun azaldığını ortaya koymuştur (McCann ve ark. 1998). DA salınımının eş zamanlı uyarılması ve alımının engellenmesi, metamfetamin ile ilişkili nörotoksisitenin altında yatan kritik unsurları yansıtmaktadır (Kuhn ve ark. 2008, Yamamoto ve Bankson 2005, Cadet ve ark. 2007, Fleckenstein ve ark. 2007).
Biz (Angoa-Perez ve ark. 2012) ve diğerleri (Baumann ve ark. 2012, Hadlock ve ark. 2011) yakın zamanda mefedronun metamfetamin ve MDMA gibi nörotoksisiteye neden olabileceği ihtimalini araştırdık. Şaşırtıcı bir şekilde, mefedron striatumun DA sinir uçları için toksik değildi (Hadlock ve ark. 2011, Baumann ve ark. 2012, Angoa-Perez ve ark. 2012). Mefedronun 5-HT sinir uçlarına zarar verip vermediği konusu, bir çalışmanın olumlu etkileri belgelemesi (Hadlock ve ark. 2011), diğerinin ise olumsuz olması (Baumann ve ark. 2012) nedeniyle belirsizliğini korumaktadır. Mefedronun DA sinir uçları üzerindeki nispeten iyi huylu etkisi ışığında ve bir DAT engelleyici olarak özellikleri göz önüne alındığında, DA nöronal sistemini metamfetaminin nörotoksik etkilerinden, amfonelik asit (Pu ve ark. 1994, Schmidt ve Gibb 1985, Marek ve ark. 1990) ve nomifensin (Poth ve ark. 2012) gibi diğer DAT engelleyicilerde olduğu gibi koruyabileceğini varsaydık. Şu anda mefedronun metamfetaminin nörotoksisitesini önemli ölçüde artırdığını bildiriyoruz. Bu etki, genellikle mefedron ile birlikte kullanılan ilaçlar olan amfetamin ve MDMA'ya kadar uzanmaktadır (Feyissa ve Kelly 2008, Schifano ve ark. 2011). Bu şaşırtıcı sonuçlar mefedronun kötüye kullanımına yeni bir ışık tutmakta ve bu β-ketoamfetaminin bu ince ve tehlikeli özelliğinin tanınmasına aciliyet kazandırmaktadır.
Materyaller ve yöntemler
İlaçlar ve Reaktifler
Mefedron hidroklorür ve 3,4-metilendioksimetamfetamin (MDMA) NIDA Araştırma Kaynakları İlaç Tedarik Programından temin edilmiştir. (+) Metamfetamin hidroklorür, nomifensin maleat, d-amfetamin sülfat, pentobarbital, DA ve tüm tamponlar ve HPLC reaktifleri Sigma-Aldrich'ten (St. Louis, MO, ABD) satın alınmıştır. Bisinçoninik asit protein tahlil kitleri Pierce'den (Rockford, IL, ABD) temin edilmiştir. Sıçan TH'ye karşı poliklonal antikorlar daha önce tarif edildiği şekilde üretilmiştir (Kuhn ve Billingsley 1987). Sıçan DAT'a karşı monoklonal antikorlar Dr. Roxanne A. Vaughan (Kuzey Dakota Üniversitesi, Grand Forks, ND, ABD) tarafından cömertçe sağlanmıştır. HRP-konjuge anti-IgG ikincil antikorlar Jackson ImmunoResearch Laboratories, Inc. (West Grove, PA, ABD) tarafından sağlanmıştır.
Hayvanlar
Deney sırasında 20-25 g ağırlığında olan dişi C57BL/6 fareler (Harlan, Indianapolis, IN, ABD), ışık (12 saat aydınlık/karanlık) ve sıcaklık kontrollü bir odada büyük ayakkabı kutusu kafeslerinde kafes başına 5 adet olacak şekilde barındırılmıştır. Nörotoksik amfetaminlerin nöronal hasarına karşı çok hassas oldukları bilindiğinden ve metamfetamin nörotoksisitesiyle ilgili önceki çalışmalarımızla tutarlılığı korumak için dişi fareler kullanılmıştır (Thomas ve ark. 2010, Thomas ve ark. 2008, Thomas ve ark. 2009). Farelerin yiyecek ve suya serbest erişimi vardı. Wayne Eyalet Üniversitesi Kurumsal Bakım ve Kullanım Komitesi hayvan bakımı ve deneysel prosedürleri onaylamıştır. Tüm prosedürler ayrıca NIH Laboratuvar Hayvanlarının Bakımı ve Kullanımı Kılavuzu ile de uyumluydu.
Farmakolojik, fizyolojik ve davranışsal prosedürler
Fareler, her enjeksiyon arasında 2 saat ara ile 10, 20 veya 40 mg/kg'lık 4 enjeksiyondan oluşan tıkınırcasına bir rejim kullanılarak mefedron ile tedavi edilmiştir. Bu tıkınırcasına tedavi rejimi, ikame edilmiş amfetaminleri ve katinon türevlerini enjekte etmek için kullanıldığında, kapsamlı DA sinir ucu hasarına yol açmaktadır. Şu anda kullanılan mefedron dozlarının DA sinir uçları için toksik olmadığı daha önce gösterilmiştir (Angoa-Perez ve ark. 2012). Fareler metamfetamin (4X 2,5 veya 5 mg/kg), amfetamin (4X 5 mg/kg) veya MDMA (4X 20 mg/kg) ile tek başına veya mefedron ile birlikte muamele edilmiştir. İki ilaçla muamele edildiğinde, farelere 4 metamfetamin, amfetamin veya MDMA enjeksiyonunun her birinden 30 dakika önce bir mefedron enjeksiyonu yapılmıştır. Kontroller, tek başına veya diğer amfetaminlerle kombinasyon halinde mefedron için kullanılan aynı programda fizyolojik salin enjeksiyonları aldı. Bir DAT inhibitörünün metamfetamin toksisitesi üzerindeki etkilerinin kontrolü için farelere her bir metamfetamin enjeksiyonundan (4X 5 mg/kg) 30 dakika önce nomifensin (4X 5 mg/kg) uygulanmıştır. Tüm enjeksiyonlar i.p. yolla yapılmıştır. Fareler son ilaç tedavisinden 2 gün sonra amfetaminle ilişkili nörotoksisite maksimuma ulaştığında feda edilmiştir. Vücut sıcaklığı, Bio Medic Data Systems, Inc. (Seaford, DE, ABD) tarafından sağlanan IPTT-300 implante edilebilir sıcaklık transponderleri kullanılarak telemetri yoluyla izlenmiştir. Sıcaklıklar, ilk METH enjeksiyonundan 20 dakika önce başlayarak her 60 dakikada bir non-invaziv olarak kaydedilmiş ve Bio Medic'in DAS-5001 konsol sistemi kullanılarak 9 saat boyunca devam etmiştir.
Striatal DA içeriğinin belirlenmesi
Striatal doku tedaviden sonra beyinden iki taraflı olarak diseke edildi ve -80°C'de saklandı. Dondurulmuş dokular tartılmış ve 4°C'de 10 hacim 0,16 N perklorik asit içinde sonike edilmiştir. Çözünmeyen protein santrifüjleme yoluyla uzaklaştırılmış ve DA, daha önce metamfetamin için tarif edildiği gibi elektrokimyasal saptamalı HPLC ile belirlenmiştir (Thomas ve ark. 2010, Thomas ve ark., 2009).
İmmünoblotlama ile TH ve DAT protein seviyelerinin belirlenmesi
İlaç tedavilerinin striatal TH ve DAT seviyeleri üzerindeki etkileri, striatal DA sinir uçlarına toksisitenin bir indeksi olarak immünoblotlama ile belirlendi. Fareler tedaviden sonra dekapitasyon ile feda edildi ve striatum iki taraflı olarak diseke edildi. Doku -80°C'de saklanmıştır. Dondurulmuş doku 95°C'de %1 SDS içinde sonikasyon ile parçalandı ve çözünmeyen materyal santrifüj ile çöktürüldü. Protein biksinoninik asit yöntemiyle belirlendi ve eşit miktarda protein (70 μg/lane) SDS-poliakrilamid jel elektroforeziyle çözüldü ve ardından nitroselüloza elektroblotlandı. Blotlar Tween 20 (%0,1 v/v) ve %5 yağsız kuru süt içeren Tris tamponlu salin içinde oda sıcaklığında 1 saat süreyle bloke edilmiştir. TH (1:1000) veya DAT'a (1:1000) karşı primer antikorlar blotlara eklenmiş ve 4°C'de 16 saat inkübasyona bırakılmıştır. Reaksiyona girmemiş antikorları uzaklaştırmak için blotlar Tris tamponlu salin içinde 3X yıkandı ve ardından HRP-konjuge anti-IgG sekonder antikor (1:4000) ile oda sıcaklığında 1 saat inkübe edildi. İmmünoreaktif bantlar gelişmiş kemilüminesans ile görselleştirildi ve TH- ve DAT-reaktif bantların göreceli yoğunlukları Kodak Image Station (Carestream Molecular Systems, Rochester, NY, ABD) ile görüntülenerek belirlendi ve ImageJ yazılımı (NIH) kullanılarak nicelleştirildi.
Veri analizi
Metamfetamin ve mefedronun DA, DAT ve TH üzerindeki doz etkilerini analiz etmek için iki yönlü ANOVA'lar gerçekleştirilmiştir. İlaç tedavilerinin striatal DA, TH ve DAT içeriği üzerindeki etkileri, tek yönlü ANOVA ve ardından Tukey'in çoklu karşılaştırma testi ile anlamlılık açısından test edilmiştir. İlaç tedavilerinin zaman içinde çekirdek vücut sıcaklığı üzerindeki sonuçları, tedaviden sonra ayrı zamanlarda sıcaklıktaki farklılıkların önemini belirlemek için iki yönlü ANOVA ve ardından Bonferroni testi kullanılarak analiz edildi. Farklılıklar p < 0.05 ise anlamlı kabul edilmiştir. Tüm istatistiksel analizler Windows için GraphPad Prism sürüm 5.02 kullanılarak gerçekleştirilmiştir (GraphPad Software, San Diego, CA, ABD, www.graphpad.com).
Şuraya git
Sonuçlar
Mefedronun metamfetamin kaynaklı nörotoksisite üzerindeki etkileri
DA sinir ucu toksisitesine neden olmadığı bilinen dozlarda (10, 20 veya 40 mg/kg) mefedron (Angoa-Perez ve ark. 2012) her metamfetamin enjeksiyonundan 30 dakika önce uygulanmıştır. Metamfetamin, striatumun DA sinir uçlarında orta (4X 2,5 mg/kg) veya ciddi (4X 5 mg/kg) hasara neden olan dozlarda uygulanmıştır (Thomas ve ark. 2004, Thomas ve ark. 2010). Şekil 1'de sunulan sonuçlar, metamfetamin dozunun (F1,40 = 66.60, p < 0.0001) ve mefedron dozunun (F4,40 = 131.3, p < 0.0001) striatumdaki DA seviyeleri üzerindeki ana etkilerinin iki yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. Mefedronun 2.5 mg/kg (F4,22 = 35.96, p < 0.001) veya 5.0 mg/kg metamfetamin (F4,17 = 953.9, p < 0.0001) ile birlikte verilmesinin ana etkisi de tek yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm tedaviler, ilgili kontrole kıyasla DA'da önemli ölçüde daha fazla azalmaya neden olmuştur (tümü için p < 0.0001). Şekil 1 ayrıca 20 (p < 0.01) ve 40 mg/kg (p < 0.001) mefedron dozlarının 2.5 mg/kg metamfetaminin DA üzerindeki tükenme etkilerini önemli ölçüde artırdığını, tüm mefedron dozlarının ise 5.0 mg/kg metamfetaminin DA seviyeleri üzerindeki etkilerini önemli ölçüde artırdığını göstermektedir (tümü için p < 0.0001).
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/sywobkqrnd-jpg.47/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Şekil 1
Mefedronun striatal DA'da metamfetamin kaynaklı azalmalar üzerindeki etkileri. Fareler, her 2,5 (-) veya 5,0 mg/kg (■) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiş ve 2 gün sonra HPLC ile striatal DA seviyelerinin belirlenmesi için feda edilmiştir. Veriler grup başına 5-7 fare için ortalama ± SEM'dir. Bazı hata çubukları sembollerin boyutunu geçemeyecek kadar küçüktür ve görünür değildir. ***p < 0.001 vs kontroller ve #p < 0.01, ##p < 0.001 veya ###p < 0.0001 vs ilgili metamfetamin dozu (Tukey'in çoklu karşılaştırma testi).
Şekil 2a, mefedronun immünoblotlama ile belirlendiği üzere DAT seviyelerinde metamfetamin kaynaklı azalmaları önemli ölçüde artırdığını göstermektedir. İmmünoblotlar sayısallaştırılmış ve DA sonuçlarıyla uyumlu olarak, metamfetamin dozunun (F1,92 = 9.48, p < 0.001) ve mefedron dozunun (F4,92 = 37.56, p < 0.0001) striatumdaki DAT seviyeleri üzerindeki ana etkileri iki yönlü ANOVA ile oldukça anlamlı bulunmuştur (Şekil 2b). Mefedronun 2.5 mg/kg (F4,56 = 15.55, p < 0.0001) veya 5.0 mg/kg metamfetamin (F4,39 = 24.84, p < 0.0001) ile birlikte verilmesinin ana etkisi de tek yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm tedaviler, ilgili kontrole kıyasla DAT'ta önemli ölçüde daha fazla azalmaya neden olmuştur (yalnızca 2,5 mg/kg metamfetamin için p < 0,01; diğer tüm tedaviler için p < 0,0001). Şekil 2b ayrıca 20 mg/kg (p < 0.01) ve 40 mg/kg (p < 0.001) mefedron dozlarının 2.5 mg/kg metamfetaminin neden olduğu DAT düşüşlerini önemli ölçüde artırdığını, sadece 40 mg/kg mefedron dozunun 5.0 mg/kg metamfetaminin DAT düşüşleri üzerindeki etkilerini önemli ölçüde artırdığını (p < 0.01) göstermektedir.
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/bfu3sx5dnr-jpg.4797/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Şekil 2
Mefedronun striatal DAT'ta metamfetamin kaynaklı azalmalar üzerindeki etkileri. Fareler, her 2,5 (●) veya 5,0 mg/kg (■) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiş ve 2 gün sonra immünoblotlama yoluyla striatal DAT seviyelerinin belirlenmesi için feda edilmiştir (a). Blotlar ImageJ kullanılarak nicelleştirilmiştir ve veriler grup başına 10-12 fare için ortalama ± SEM'dir (b). *p < 0.01 veya ***p < 0.0001 vs kontrol (C) ve #p < 0.01 veya ##p < 0.001 vs ilgili metamfetamin dozu (Tukey'in çoklu karşılaştırma testi).
Şekil 3a, mefedronun immünoblotlama ile belirlendiği üzere TH seviyelerinde metamfetamin kaynaklı azalmaları önemli ölçüde artırdığını göstermektedir. İmmünoblotlar nicelleştirilmiştir ve DA ve DAT için yukarıdaki sonuçlarla uyumlu olarak, metamfetamin dozunun (F1,81 = 47.89, p < 0.0001) ve mefedron dozunun (F4,81 = 63.57, p < 0.0001) ana etkileri iki yönlü ANOVA ile oldukça anlamlıdır (Şekil 3b). Mefedronun 2,5 mg/kg (F4,34 = 12,98, p < 0,0001) veya 5,0 mg/kg metamfetamin (F4,49 = 99,16, p < 0,0001) ile birlikte verilmesinin ana etkisi de tek yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm muameleler, ilgili kontrole kıyasla TH'de önemli ölçüde daha fazla azalmaya neden olmuştur (2,5 mg/kg metamfetamin + 10 mg/kg mephedrone için p < 0,001; diğer tüm kombinasyonlar için p < 0,0001); TH seviyelerini önemli ölçüde değiştirmeyen tek başına 2,5 mg/kg metamfetamin hariç (yani, toksisite yok). Şekil 3b ayrıca 20 mg/kg (p < 0.01) ve 40 mg/kg (p < 0.001) mefedron dozlarının 2.5 mg/kg metamfetaminin neden olduğu TH düşüşlerini önemli ölçüde artırdığını ve her üç mefedron dozunun da 5.0 mg/kg metamfetaminin TH düşüşleri üzerindeki etkilerini önemli ölçüde (p < 0.0001) artırdığını göstermektedir.
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/tggfrjpqru-jpg.4798/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Şekil 3
Mefedronun striatal TH'de metamfetamin kaynaklı azalmalar üzerindeki etkileri. Fareler her 2,5 (●) veya 5,0 mg/kg (■) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiş ve 2 gün sonra immünoblotlama (a) ile TH'nin striatal seviyelerinin belirlenmesi için feda edilmiştir. Lekeler ImageJ kullanılarak nicelleştirilmiştir ve veriler grup başına 10-12 fare için ortalama ± SEM'dir (b). Bazı hata çubukları sembollerin boyutunu geçemeyecek kadar küçüktür ve görünür değildir. **p < 0.001 veya ***p < 0.0001 vs kontrol (C) ve #p < 0.01, ##p < 0.001 veya ##p < 0.0001) vs ilgili metamfetamin dozu (Tukey'in çoklu karşılaştırma testi).
Mefedronun metamfetamin kaynaklı hipertermi üzerindeki etkileri
Metamfetamin gibi mefedron da önemli ölçüde hipertermiye neden olmaktadır (Hadlock ve ark. 2011, Baumann ve ark. 2012, Angoa-Perez ve ark. 2012). Her metamfetamin enjeksiyonundan 30 dakika önce mefedron verildiğinde, metamfetamin ve mefedron dozlarının (F1,300 = 11.99, p < 0.0001) zaman üzerindeki ana etkilerinin (F4,300 = 51.73, p < 0.0001) iki yönlü ANOVA ile oldukça anlamlı olduğu Şekil 4'te görülebilir. Zaman içinde 2.5 mg/kg metamfetamin (F4,120 = 41.44, p < 0.0001, panel a) (F30,120 = 3.84, p < 0.0001) veya 5.0 mg/kg metamfetamin (F4,120 = 78.09, p < 0.0001, panel b) (F30,120 = 9.98, p < 0.0001) ile birlikte verilen mefedronun ana etkileri de iki yönlü ANOVA ile oldukça anlamlıydı. Metamfetamin ± mephedrone dozlarından herhangi biriyle yapılan tüm tedaviler ilgili kontrollerden önemli ölçüde farklıydı (tüm tedaviler için p < 0.0001).
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/x0ik9hdwsw-jpg.4799/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Şekil 4
Mefedronun metamfetamin kaynaklı hipertermi üzerindeki etkileri. Fareler, her 2,5 (a) veya 5,0 mg/kg (b) metamfetamin (METH) enjeksiyonundan 30 dakika önce belirtilen dozlarda mefedron (MEPH) ile muamele edilmiştir. Çekirdek sıcaklıkları, ilk metamfetamin enjeksiyonundan 60 dakika önce başlayan telemetri ile 20 dakika aralıklarla ölçülmüştür. 4 metamfetamin enjeksiyonu x ekseninde duran oklarla gösterilmiştir. Veriler grup başına 6-8 farenin ortalama vücut sıcaklığı olarak ifade edilmiştir. SEM'ler her zaman ortalamanın <%10'u kadardır ve anlaşılır olması için atlanmıştır.
Mefedronun amfetamin ve MDMA kaynaklı nörotoksisite üzerindeki etkileri
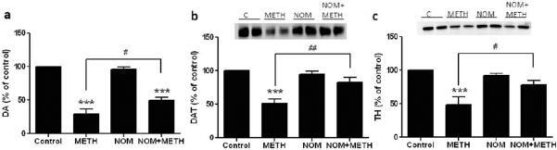
Mefedronun metamfetamin üzerindeki artırıcı etkilerinin diğer nörotoksik amfetaminlere genişletilip genişletilemeyeceğini test etmek için fareler bu β-ketoamfetamin (20 mg/kg) artı amfetamin (4X 5 mg/kg) veya MDMA (4X 20 mg/kg) ile muamele edilmiş ve sonuçlar Şekil 5'te sunulmuştur. Mefedronun kendisinin striatal DA, DAT veya TH'yi azaltmadığını hatırlayın (Angoa-Perez ve ark. 2012). İlacın ana etkisi (F5,27 = 27.18, p < 0.0001) DA azalmaları için tek yönlü ANOVA ile oldukça anlamlıydı (Şekil 5a). Şekil 5a'da ayrıca amfetamin (p < 0,001) veya MDMA (p < 0,001) ile tek başına veya mefedron ile kombinasyon halinde (her iki ilaç için p < 0,0001) yapılan tüm tedavilerin DA seviyelerini kontrolden önemli ölçüde düşürdüğü görülebilir. Mefedron, amfetamin (p < 0.01) veya MDMA'nın (p < 0.01) neden olduğu DA düşüşlerini önemli ölçüde artırmıştır. Şekil 5b, kombinasyon ilaç tedavilerinin striatumdaki DAT seviyeleri üzerindeki benzer etkilerini göstermektedir. İlacın ana etkisi (F4,49 = 42.63, p < 0.0001) DAT için tek yönlü ANOVA ile oldukça anlamlıydı. Şekil 5b'de amfetamin veya MDMA ile yapılan tüm uygulamaların kontrole kıyasla önemli ölçüde (hepsi için p < 0.0001) daha düşük olduğu da görülebilir. Mefedron ayrıca amfetamin veya MDMA'nın neden olduğu DAT azalmalarını önemli ölçüde artırmıştır (her iki durumda da p < 0.0001). Son olarak, Şek. 5c ilacın ana etkisinin (F4,50 = 75.06, p < 0.0001) TH'deki azalmalar için tek yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. Ayrıca Şekil 5c'de amfetamin veya MDMA ile yapılan tüm uygulamaların kontrole kıyasla önemli ölçüde (hepsi için p < 0.0001) daha düşük olduğu görülebilir. Mefedron ayrıca amfetamin veya MDMA'nın neden olduğu TH düşüşlerini önemli ölçüde artırmıştır (her iki durumda da p < 0.0001)
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/onvypkgxvn-jpg.4800/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Şekil 5
Mefedronun amfetamin veya MDMA kaynaklı DA sinir ucu nörotoksisitesi üzerindeki etkileri. Fareler, her 5.0 mg/kg amfetamin (AMPH) veya 20 mg/kg MDMA enjeksiyonundan 30 dakika önce 20 mg/kg mefedron (MEPH) ile muamele edilmiş ve (a) DA'nın striatal seviyelerinin HPLC ile belirlenmesi için tedaviden 2d sonra feda edilmiştir. (b) DAT ve (c) TH immünoblotlama ile belirlenmiş ve ImageJ kullanılarak blotlar nicelleştirilmiştir. DAT ve TH için temsili immünoblotlar sırasıyla (b) ve (c) panellerine ek olarak dahil edilmiştir ve her iki panel için tedaviler 1,5: kontrol; 2,6: MEPH; 3: AMPH; 4: AMPH + MEPH; 7: MDMA; ve 8: MDMA + MEPH ile gösterilmiştir. Veriler her gruptaki 5-12 fare için ortalama ± SEM'dir. **p < 0.001 veya ***p < 0.0001 vs kontrol ve #p < 0.01 veya ###p < 0.0001 vs AMPH veya MDMA (Tukey'in çoklu karşılaştırma testi).
Nomifensinin metamfetamin kaynaklı nörotoksisite üzerindeki etkileri
Bilinen kötüye kullanım veya nörotoksik potansiyeli olmayan güçlü bir DAT engelleyici olan nomifensin, metamfetamin kaynaklı nörotoksisiteye karşı koruma kabiliyeti ve metamfetamin, amfetamin ve MDMA'nın neden olduğu DA sinir uçlarına toksisite üzerindeki mefedron eylemlerinin aksine test edilmiştir. Şekil 6a'daki sonuçlar, ilacın DA seviyeleri üzerindeki ana etkisinin (F3,16 = 63,39, p < 0,0001) tek yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. Nomifensin tek başına DA seviyelerini değiştirmemiştir, ancak metamfetaminin neden olduğu azalma (p < 0.0001) nomifensin tarafından hafif ama önemli ölçüde tersine çevrilmiştir (p < 0.01). İlacın (F3,20 = 16.78, p < 0.0001) DAT seviyeleri üzerindeki ana etkisi, Şekil 6b'de gösterildiği gibi tek yönlü ANOVA ile oldukça anlamlıydı. Nomifensin DAT seviyelerini değiştirmemiş ancak metamfetaminin (p < 0.0001) neden olduğu striatal DAT azalmasına karşı kontrole kıyasla önemli bir koruma (p < 0.001) sağlamıştır. Son olarak, Şekil 6c ilacın TH seviyeleri üzerindeki ana etkisinin (F3,15 = 14.10, p < 0.0001) tek yönlü ANOVA ile oldukça anlamlı olduğunu göstermektedir. DA ve DAT için görüldüğü gibi, metamfetaminin neden olduğu TH'deki azalma (p < 0.0001) nomifensin (p < 0.01) tarafından hafif ama önemli ölçüde önlenmiştir.
http://bbzzzsvqcrqtki6umym6itiixfhni37ybtt7mkbjyxn2pgllzxf2qgyd.onion/index.php?attachments/daczg9cwfv-jpg.4801/&hash=f31155ada4e59f22a35f9110aaa6a7e5
Şekil 6
Nomifensinin metamfetamin kaynaklı DA sinir ucu nörotoksisitesi üzerindeki etkileri. Fareler her 5.0 mg/kg metamfetamin (METH) enjeksiyonundan 30 dakika önce 5.0 mg/kg nomifensin (NOM) ile muamele edilmiş ve 2 gün sonra HPLC ile (a) DA'nın striatal seviyelerinin belirlenmesi için feda edilmiştir. (b) DAT ve (c) TH immünoblotlama ile belirlenmiş ve ImageJ kullanılarak blotlar nicelleştirilmiştir. DAT ve TH için temsili immünoblotlar sırasıyla (b) ve (c) panellerine ek olarak dahil edilmiştir. Veriler grup başına 5-7 fare için ortalama artı SEM'dir. ***p < 0.0001 vs kontrol (C) ve #p < 0.01 veya ##p < 0.001 vs tek başına metamfetamin (Tukey'in çoklu karşılaştırma testi).
Tartışma
Bu çalışmanın amacı, mefedronun metamfetaminin neden olduğu DA sinir ucu toksisitesini önleyip önlemeyeceğini belirlemekti. Metamfetamin ve MDMA ile kimyasal benzerliğine dayanarak, başlangıçta mefedronun DA nöronal sistemi üzerinde zararlı etkiler göstermesi bekleniyordu. Ancak, birkaç çalışma neredeyse eş zamanlı olarak mefedronun DA sinir uçları için toksik olmadığını ortaya koymuştur (Angoa-Perez ve ark. 2012, Baumann ve ark. 2012, Hadlock ve ark. 2011). Bu ilacın 5-HT nöronal sistemine zarar verip vermediği sorusu açık kalmaya devam etmektedir. Bir çalışma 5-HT sinir ucu işlevinde kalıcı azalmalar bildirirken (Hadlock ve ark. 2011), bir diğeri mephedrone'un hasara neden olmadığını bulmuştur (Baumann ve ark. 2012). Mefedron, DA sinir ucu ile, DAT ile etkileşimleri yoluyla gerçekten salınımı uyardığını ve DA yeniden alımını engellediğini düşündüren bir şekilde etkileşime girer. Metamfetaminin nörotoksik etki mekanizmasının kilit bir yönü, DAT aracılığıyla DA sinir uçlarına erişim sağlama ve DA homeostazını bozma yeteneğidir (Sulzer 2011). Metamfetamin nörotoksik kaskadındaki bu erken adım DAT'ın inhibisyonu ile önlenirse, toksisite önlenir (Pu ve ark. 1994, Poth ve ark. 2012, Marek ve ark. 1990, Schmidt ve Gibb 1985). Mefedronun diğer DAT inhibitörleriyle aynı koruyucu özelliğe sahip olabileceğini düşündük, ancak bunun yerine toksisitede önemli bir artış gözlemledik. Bu etkileşim, DA sinir uçlarında orta veya ciddi hasara neden olan iki farklı metamfetamin dozu (sırasıyla 4X 2,5 veya 5,0 mg/kg) kullanılarak görülmüştür. Mefedronun bu güçlendirici etkisi metamfetaminle sınırlı kalmamış ve genellikle mefedron ve diğer β-ketoamfetaminlerle birlikte kullanılan iki uyuşturucu olan amfetamin ve MDMA'ya kadar uzanmıştır (Feyissa ve Kelly 2008, Schifano ve ark. 2011, Kelly 2011). Bu nedenle, mefedron en azından striatumun DA sinir uçlarında toksisiteye neden olmamasına rağmen, diğer kötüye kullanım ilaçlarının nörotoksik etkilerini güçlendirmektedir. Bu yeni bulgu, mefedronun kötüye kullanımını daha da çarpıcı hale getirmelidir çünkü içsel nörotoksisitesinin olmaması onu zararsız gösterebilir.
Hipertermi, insanlarda metamfetamin (Greene ve ark. 2008) ve β-ketoamfetamin alımının yaygın olarak bildirilen bir akut yan etkisidir (Borek ve Holstege 2012, Prosser ve Nelson 2012). Metamfetamin gibi, β-ketoamfetamin ilaçlarının çoğu da kemirgenlerde çekirdek sıcaklığında önemli artışlara neden olmaktadır (Angoa-Perez ve ark. 2012, Hadlock ve ark. 2011, Baumann ve ark. 2012, Rockhold ve ark. 1997). Metamfetaminin neden olduğu hipertermi, morfolojik ve nöronal hasar verici etkilerine katkıda bulunabilirken, hiperterminin bu etkilerin doğrudan nedeni olması gerekmez (Kiyatkin ve Sharma 2009). Mefedron ve metamfetamin ile tedavi edilen farelerde çekirdek vücut sıcaklıklarını kaydettik ve kombine tedavinin sıcaklıkları tek başına her iki ilaçtan sonra görülen maksimum artışların ötesine yükseltmediğini gözlemledik. Metamfetamin vücut sıcaklığında doza bağlı bir artışa neden olmuş ve bu hipertermi test edilen tüm mephedrone doz aralığında değişmez olmuştur. Aslında, mephedrone tedavisinden sonra gözlenen vücut sıcaklığındaki enjeksiyon sonrası düşüş (Angoa-Perez ve ark. 2012) daha yüksek mephedrone artı metamfetamin dozlarında korunmuştur. İlacın neden olduğu hipertermi kombine ilaç tedavisi ile artmamış olsa da, nörotoksik etkiler katkı maddesidir. Bu nedenle, en azından mevcut durumda, metamfetaminin nörotoksik etkilerinin hipertermiden bağımsız bir şekilde mefedron tarafından artırılabileceği görülmektedir.
Mefedron, DAT işlevini açıkça inhibe eder ve DA'nın in vitro yeniden alımını engeller (Lopez-Arnau ve ark. 2012, Hadlock ve ark. 2011, Kehr ve ark. 2011, Martinez-Clemente ve ark. 2012, Cozzi ve ark. 1999). Mefedron, WIN-35,428'i DAT üzerindeki bağlanma bölgesinden uzaklaştırarak DA alımının rekabetçi bir inhibitörü olduğunu düşündürmektedir (Martinez-Clemente ve ark. 2012, Lopez-Arnau ve ark. 2012). Bu bağlamda mefedronun gücü metamfetamin (Cozzi ve ark. 1999) ve MDMA (Escubedo ve ark. 2011) ile çok benzerdir. Mefedronun DAT tarafından taşınıp taşınmadığı bilinmemektedir ancak metkatinon taşınmaktadır (Cozzi ve Foley 2003). DAT'a bağlanan ve DA alımını engelleyen nomifensin ve amfonelik asit, metamfetamin kaynaklı nörotoksisiteye karşı önemli ölçüde koruma sağlar (Pu ve ark. 1994, Marek ve ark. 1990, Schmidt ve Gibb 1985, Poth ve ark. 2012) ve DAT'tan yoksun fareler metamfetaminin nöronal toksisitesine dirençlidir (Fumagalli ve ark. 1998). Mefedronun nörotoksik olmadığını ve bir DAT engelleyicisi olduğunu bilmek, toksisiteyi önlemesi gerektiği tahminine yol açmaktadır. Nomifensini bu bağlamda pozitif bir kontrol olarak test ettik ve metamfetamin kaynaklı DA, DAT ve TH tükenmesine karşı koruduğunu doğruladık. Nomifensin ayrıca norepinefrin taşıyıcısını da inhibe eder (Brogden ve ark. 1979) ancak bu özellik mevcut sonuçları açıklayamaz çünkü mefedron dahil çoğu β-ketoamfetamin norepinefrin taşıyıcısını inhibe eder ve norepinefrin alımını engeller (Kelly 2011, Rothman ve ark. 2003, Cozzi ve ark. 1999, Sogawa ve ark. 2011, Lopez-Arnau ve ark. 2012). Mefedronun bazı farmakolojik etkilerinde 5-HT nöronal sisteminin rolü, bu ilacın MDMA gibi (Yamamoto ve ark. 1995) 5-HT2A reseptörleriyle etkileşimleri yoluyla striatal DA akışına neden olma kabiliyeti ışığında mümkündür (Lopez-Arnau ve ark. 2012, Martinez-Clemente ve ark. 2012). Mefedronun neden olduğu hiper-lokomosyon endojen 5-HT'ye bağlıdır (Lopez-Arnau ve ark. 2012) ve bu ilaç aynı zamanda 5-HT salınımını uyarır ve in vitro alımını engeller (Sogawa ve ark. 2011, Cozzi ve ark. 1999, Nagai ve ark. 2007, Hadlock ve ark. 2011, Lopez-Arnau ve ark. 2012, Martinez-Clemente ve ark. 2012) ve in vivo (Baumann ve ark. 2012, Kehr ve ark. 2011). Bununla birlikte, genetik olarak 5-HT'den yoksun farelerin nörotoksisiteye karşı duyarlılıklarını koruduklarını göstererek, en azından metamfetaminin DA nörotoksisitesinde endojen 5-HT'nin rolünü ekarte edebiliriz (Thomas ve ark. 2010).
Mefedron, metamfetamin nörotoksisitesini birkaç olası mekanizma ile artırabilir. İlk olarak, mefedron VMAT ile etkileşime girerek DA'nın presinaptik sinir ucunun sitoplazmasına sızmasına neden olabilir. DA'nın sitoplazmik havuzunu (yani ilaçla serbest bırakılabilir) artıran tedaviler metamfetamin nörotoksisitesini artırır (Thomas ve ark. 2008, Thomas ve ark. 2009, Schmidt ve ark. 1985). Bu mekanizma olası değildir çünkü metkatinon VMAT ile sadece zayıf bir şekilde etkileşime girer (Cozzi ve ark. 1999). İkinci olarak, mefedron artı metamfetamin kombinasyonu DA'nın veziküler olmayan salınımı üzerinde sinerjik bir etkiye sahip olabilir, ancak DAT veya SERT eksprese eden CHO hücrelerinin metilon artı metamfetamin ile muamelesinin DA veya 5-HT salınımı üzerinde ek bir etkiye sahip olmadığını gösteren sonuçlar ışığında bu olasılık da olası görünmemektedir (Sogawa ve ark. 2011). Üçüncüsü, mefedron DAT ile katkı toksisitesine katkıda bulunan yeni bir şekilde etkileşime girebilir. Metamfetamin ile birlikte metilonun DAT veya SERT eksprese eden CHO hücrelerinde sinerjik sitotoksisiteye neden olduğu, ancak taşıyıcılardan yoksun vahşi tip CHO hücrelerinde olmadığı gösterilmiştir (Sogawa ve ark. 2011). Bu çalışmalarda kültürlenmiş hücrelerde görülen sitotoksisite (yani LDH salınımı) metamfetaminin neden olduğu DA sinir uçlarındaki hasardan çok farklıdır, ancak bu mekanizma DAT için artan sitotoksisitede ilginç ancak tanımlanmamış bir rol önermektedir. Son olarak, mefedron metamfetamin metabolizmasını değiştirebilir. Mefedron, metamfetamin ve MDMA (Caldwell 1976) gibi öncelikle N-demetilasyon ile metabolize edilir (Meyer ve Maurer 2010). Bu mekanizmaya destek, metamfetamin ve MDMA'nın kendi birincil metabolitlerinin üretimini karşılıklı olarak inhibe ettiğinin ve ilaç plazma seviyelerini her iki ilacın tek başına uygulanmasından sonra görülenlerin üzerine çıkardığının gösterilmesinden gelmektedir (Kuwayama ve ark. 2012). Şu anda ve önceki çalışmamızda (Angoa-Perez ve ark. 2012) kullanılan mefedron dozları yüksek olmakla birlikte nörotoksik değildir ve insanlar tarafından kötüye kullanılan aralıkta yer almaktadır (McErath ve O'Neill 2011). Bu nedenle mefedron, metabolizmasını inhibe ederek metamfetaminin plazma seviyelerini artırmak için MDMA gibi hareket ediyor olabilir. Bu ikinci olasılığı doğrulamak için derinlemesine bir farmakokinetik analiz gerekecektir.
β-ketoamfetaminlerin kötüye kullanımı endişe verici bir oranda artmaktadır ve mefedron şu anda esrar, MDMA ve kokainden sonra en yaygın kullanılan ilaçlardan biridir (Morris 2010, Winstock ve ark. 2011b). Buna ek olarak, mephedrone insanlarda MDMA'ya kıyasla daha güçlü bir aşerme hissine neden olmaktadır (Brunt ve ark. 2011) ve mephedrone çeken kullanıcılar bunu kokainden daha fazla bağımlılık yapıcı olarak değerlendirmektedir (Winstock ve ark. 2011b). Mefedron insanlar tarafından tıkınırcasına tüketilir (yani "istifleme") ve genellikle esrar ve amfetamin psikostimülanlar gibi diğer uyuşturucularla birlikte alınır (Schifano ve ark. 2011, Fass ve ark. 2012, Winstock ve ark. 2011a, Kelly 2011, Torrance ve Cooper 2010). Mefedron, MDMA olarak satılan tabletlerde giderek daha fazla bulunmaktadır (Brunt ve ark. 2011) ve bu son uyuşturucunun saflığı düşmeye devam ettikçe kullanımı muhtemelen MDMA'yı geçecektir (Brunt ve ark. 2011, Tanner-Smith 2006, Teng ve ark. 2006). Mephedrone ve diğer "banyo tuzları" bileşenlerinin yaygın kötüye kullanım modellerine dayanarak, bu ilaçlar bilerek veya bilmeyerek amfetaminlerle birleştirildiğinde insanlarda ek sağlık risklerinin ortaya çıkıp çıkmayacağını düşünmek önemlidir. En azından mefedronun metamfetamin, amfetamin ve MDMA'nın neden olduğu striatumun DA sinir uçlarına yönelik nörotoksisiteyi önemli ölçüde artırdığını gösteren sonuçlarımız, bu β-ketoamfetaminin özellikle tehlikeli ve beklenmedik bir özelliğini ortaya koymaktadır.
Kullanılan kısaltmalar
5-HT serotonin
DA dopamin
DAT DA taşıyıcı
MDMA 3,4-metilendioksimetamfetamin
TH tirozin hidroksilaz
VMAT veziküler monoamin taşıyıcı