- Joined
- May 23, 2023
- Messages
- 6
- Reaction score
- 4
- Points
- 3
Introducción:
Cierto vendedor en línea (que no se nombrará) parece sugerir una ruta "novedosa" para obtener fenetilaminas.
La reacción de aldehído a amina se produce en 3 pasos distintos:
1) Primero se utiliza una reacción Baylis-Hillman para acoplar un aldehído arílico con acrilamida utilizando una base de amina terciaria como
DMAP (4-dimetilaminopiridina) o DABCO/TEDA (trietilendiamina).
La acrilamida es un producto químico industrial que se utiliza para fabricar polímeros y también se asocia a los alimentos quemados.
2) A continuación se realiza un reordenamiento de Hofmann modificado.
A diferencia de la reacción de Hofmann "normal", es importante señalar que el producto final no es una amina.
El isocianato intermedio no sufrirá hidrólisis por el agua para formar el ácido carbámico que luego se descarboxila para dar la amina.
En su lugar, el alcohol bencílico formado en el paso 1 sufrirá una ciclización intramolecular formando un anillo de carbamato de 5 miembros (que es a la vez un éster y una amida).
Se produce una serie de intercambios rápidos de protones que isomerizan la oxazolidona no conjugada en la oxazolona conjugada más estable.
3) En el último paso se realiza una reducción de paladio sobre carbono utilizando 3 equivalentes de hidrógeno gaseoso.
El primer equivalente de hidrógeno se utiliza para romper el anillo de oxazolona, produciendo un éster de formiato y una imina que luego se reducen con los 2 equivalentes de hidrógeno restantes.
reducidos por los 2 equivalentes de hidrógeno restantes. Se forma la amina deseada junto con ácido fórmico como subproducto.
Es posible que esta reacción ya se conozca en la escena clandestina(aunque sea un secreto muy bien guardado),
sin embargo, me atrevo a decir que la reacción es "novedosa" porque nunca he oído ningún debate/informe documentado de esta reacción en ningún foro similar o en la literatura.
Sedesconoce el mecanismo exacto de la reacción, aunque he intentado dilucidarlo lo mejor que he podido.
Si no está de acuerdo con mis suposiciones mecanicistas, por favor explique sus pensamientos/críticas con un razonamiento sólido en los comentarios.
Apreciamos mucho sus comentarios.
Pruebas bibliográficas:
[1] Pedro Molina, Alberto Tarraga, en el libro "Comprehensive Organic Functional Group Transformations", 1995, ISBN: 978-0-08-044705-6
" se ha descubierto que el tetraacetato de plomo en piridina proporciona un procedimiento suave para efectuar un reordenamiento rápido, de alto rendimiento y tipo Hofmann de β-hidroxi amidas primarias a 2-oxazolidinonas, a través del correspondiente β-hidroxiisocianato"
[2] Shinobu Hazama, S. Ichikawa, Fumihiro Yonebayashi, en el Japanese Journal of Forensic Science and Technology, 2008, DOI: 10.3408/jafst.13.67
"El d-NE se trató con 1,1-carbonildiimidazol para producir el carbamato c íclico correspondiente, y el producto se trató con hidruro de sodio y yodometano para formar un derivado amínico mono-N-metilado, que se trató con paladio sobre carbón activado en atmósfera de hidrógeno para su reducción catalítica. Tras la adición de cloruro de hidrógeno (HCl) acuoso, se obtuvo l-MA como su sal HCl (rendimiento total 58%)"
Mecanismo/esquema de reacción según la bibliografía:

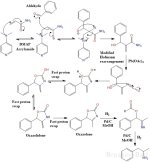
Mecanismo/esquema dereacción propuesto (hipotético):

Preguntas que aún necesitan respuesta:
1) ¿Cuáles son las condiciones exactas de reacción (temperatura, concentración, tiempo de reacción, etc.) y los reactivos necesarios para que esta reacción funcione?
2) ¿Cuáles son las condiciones de trabajo necesarias para purificar cada intermedio?
3 ) No estoy seguro de la cantidad de pruebas y el desarrollo iterativo se produce en este foro.
¿Hay alguien en el foro con un espacio de laboratorio adecuado dispuesto a probar esto y dar su opinión? No tengo los medios para probarlo yo mismo.
4) ¿Es la reacción mecánicamente correcta? ¿Existe realmente la reacción o me la he sacado de la manga?
5) ¿Existeya un procedimiento para esta reacción? Si es así, ¿dónde puedo encontrarlo?
6)¿Puede modificarse el esquema de la reacción para incluir también la síntesis de derivados n-metilados (similar al ejemplo que mostré en la bibliografía)?
7) ¿Puedenutilizarse reactivos alternativos al tetraacetato de plomo para inducir el paso de ciclización? Me parece que
hipoclorito no funcionará porque también oxidaría el alcohol bencílico a la cetona/fenona.
8) ¿Sepueden utilizar otras aminas terciarias, como la trietilamina, además de DMAP y DABCO?
9) ¿Existenreacciones secundarias dignas de mención que disminuyan la pureza del producto final?
10)¿Producirá la reducción una amina racémica o favorecerá preferentemente a un estereoisómero sobre el otro?
Es la primera vez que escribo en este foro, así que no sé qué respuesta puedo esperar.
Gracias por leernos.
Cierto vendedor en línea (que no se nombrará) parece sugerir una ruta "novedosa" para obtener fenetilaminas.
La reacción de aldehído a amina se produce en 3 pasos distintos:
1) Primero se utiliza una reacción Baylis-Hillman para acoplar un aldehído arílico con acrilamida utilizando una base de amina terciaria como
DMAP (4-dimetilaminopiridina) o DABCO/TEDA (trietilendiamina).
La acrilamida es un producto químico industrial que se utiliza para fabricar polímeros y también se asocia a los alimentos quemados.
2) A continuación se realiza un reordenamiento de Hofmann modificado.
A diferencia de la reacción de Hofmann "normal", es importante señalar que el producto final no es una amina.
El isocianato intermedio no sufrirá hidrólisis por el agua para formar el ácido carbámico que luego se descarboxila para dar la amina.
En su lugar, el alcohol bencílico formado en el paso 1 sufrirá una ciclización intramolecular formando un anillo de carbamato de 5 miembros (que es a la vez un éster y una amida).
Se produce una serie de intercambios rápidos de protones que isomerizan la oxazolidona no conjugada en la oxazolona conjugada más estable.
3) En el último paso se realiza una reducción de paladio sobre carbono utilizando 3 equivalentes de hidrógeno gaseoso.
El primer equivalente de hidrógeno se utiliza para romper el anillo de oxazolona, produciendo un éster de formiato y una imina que luego se reducen con los 2 equivalentes de hidrógeno restantes.
reducidos por los 2 equivalentes de hidrógeno restantes. Se forma la amina deseada junto con ácido fórmico como subproducto.
Es posible que esta reacción ya se conozca en la escena clandestina(aunque sea un secreto muy bien guardado),
sin embargo, me atrevo a decir que la reacción es "novedosa" porque nunca he oído ningún debate/informe documentado de esta reacción en ningún foro similar o en la literatura.
Sedesconoce el mecanismo exacto de la reacción, aunque he intentado dilucidarlo lo mejor que he podido.
Si no está de acuerdo con mis suposiciones mecanicistas, por favor explique sus pensamientos/críticas con un razonamiento sólido en los comentarios.
Apreciamos mucho sus comentarios.
Pruebas bibliográficas:
[1] Pedro Molina, Alberto Tarraga, en el libro "Comprehensive Organic Functional Group Transformations", 1995, ISBN: 978-0-08-044705-6
" se ha descubierto que el tetraacetato de plomo en piridina proporciona un procedimiento suave para efectuar un reordenamiento rápido, de alto rendimiento y tipo Hofmann de β-hidroxi amidas primarias a 2-oxazolidinonas, a través del correspondiente β-hidroxiisocianato"
[2] Shinobu Hazama, S. Ichikawa, Fumihiro Yonebayashi, en el Japanese Journal of Forensic Science and Technology, 2008, DOI: 10.3408/jafst.13.67
"El d-NE se trató con 1,1-carbonildiimidazol para producir el carbamato c íclico correspondiente, y el producto se trató con hidruro de sodio y yodometano para formar un derivado amínico mono-N-metilado, que se trató con paladio sobre carbón activado en atmósfera de hidrógeno para su reducción catalítica. Tras la adición de cloruro de hidrógeno (HCl) acuoso, se obtuvo l-MA como su sal HCl (rendimiento total 58%)"
Mecanismo/esquema de reacción según la bibliografía:
Mecanismo/esquema dereacción propuesto (hipotético):
Preguntas que aún necesitan respuesta:
1) ¿Cuáles son las condiciones exactas de reacción (temperatura, concentración, tiempo de reacción, etc.) y los reactivos necesarios para que esta reacción funcione?
2) ¿Cuáles son las condiciones de trabajo necesarias para purificar cada intermedio?
3 ) No estoy seguro de la cantidad de pruebas y el desarrollo iterativo se produce en este foro.
¿Hay alguien en el foro con un espacio de laboratorio adecuado dispuesto a probar esto y dar su opinión? No tengo los medios para probarlo yo mismo.
4) ¿Es la reacción mecánicamente correcta? ¿Existe realmente la reacción o me la he sacado de la manga?
5) ¿Existeya un procedimiento para esta reacción? Si es así, ¿dónde puedo encontrarlo?
6)¿Puede modificarse el esquema de la reacción para incluir también la síntesis de derivados n-metilados (similar al ejemplo que mostré en la bibliografía)?
7) ¿Puedenutilizarse reactivos alternativos al tetraacetato de plomo para inducir el paso de ciclización? Me parece que
hipoclorito no funcionará porque también oxidaría el alcohol bencílico a la cetona/fenona.
8) ¿Sepueden utilizar otras aminas terciarias, como la trietilamina, además de DMAP y DABCO?
9) ¿Existenreacciones secundarias dignas de mención que disminuyan la pureza del producto final?
10)¿Producirá la reducción una amina racémica o favorecerá preferentemente a un estereoisómero sobre el otro?
Es la primera vez que escribo en este foro, así que no sé qué respuesta puedo esperar.
Gracias por leernos.
Attachments
Last edited: