Yoyoyo, alguém poderia me ajudar a localizar algum tartarato de ergotamina ou medicamentos que contenham ergotamina nos EUA? Qualquer ajuda é bem-vinda 
You are using an out of date browser. It may not display this or other websites correctly.
You should upgrade or use an alternative browser.
You should upgrade or use an alternative browser.
Síntese de LSD a partir de Ergotamina
- Thread starter G.Patton
- Start date
- Language
- 🇺🇸
- Joined
- Nov 17, 2022
- Messages
- 31
- Reaction score
- 13
- Points
- 8
3 gramas de lsd dão de 20.000 a 30.000 doses, desculpe minha pergunta de iniciante, mas como eles separaram essa pequena quantidade exata para fazer o blotter em 30.000 doses?
Obrigado por qualquer resposta
Obrigado por qualquer resposta
Chefe, comprei uma solução de LSD, 100 mg em 5 ml de vodca, e quero armazená-la por tempo indeterminado. Tenho algumas perguntas...
-É melhor no freezer ou na geladeira?
É necessário borbulhar argônio ou nitrogênio na solução e preencher a parte superior vazia do conta-gotas com o gás inerte, vaselina ou algo parecido?
-Colocar alguns mg de EDTA?
Obrigado!!!
Quero armazenar por anos.
-É melhor no freezer ou na geladeira?
É necessário borbulhar argônio ou nitrogênio na solução e preencher a parte superior vazia do conta-gotas com o gás inerte, vaselina ou algo parecido?
-Colocar alguns mg de EDTA?
Obrigado!!!
Quero armazenar por anos.
G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,991
- Solutions
- 3
- Reaction score
- 3,380
- Points
- 113
- Deals
- 1
Mantenha o recipiente hermeticamente fechado. Armazene em condições frescas (use um freezer de -17-20 *C) e secas em recipientes bem fechados.
- Language
- 🇪🇸
- Joined
- Jul 11, 2023
- Messages
- 12
- Reaction score
- 5
- Points
- 3
Como posso criar uma atmosfera inerte? De quais dispositivos eu preciso?
- Joined
- Aug 8, 2022
- Messages
- 674
- Reaction score
- 512
- Points
- 63
- Deals
- 5
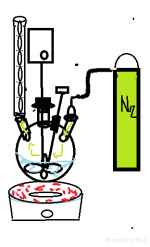
Aqui, ilustrei uma configuração clássica de reação com gás inerte. O fluxo deve ser calibrado de forma que o nitrogênio não expulse produtos de reação ou solventes que não queremos que sejam expelidos. Para isso, um borbulhador pode ser conectado entre o recipiente e o frasco para visualizar o fluxo de gás. O N2 é usado dessa forma em ambientes oficiais, pois está prontamente disponível e é barato, mas também é leve, portanto, precisa estar fluindo para não ser substituído pelo ar atmosférico.
Um gás inerte e, ao contrário do N2, muito mais pesado, é o argônio, que é mais caro e muito mais raro, mas está disponível. O argônio pode ser usado dessa forma, bastando encher o meio de reação com um recipiente e, opcionalmente, fazer vácuo na extremidade do condensador e encher novamente com argônio.
Um gás inerte e, ao contrário do N2, muito mais pesado, é o argônio, que é mais caro e muito mais raro, mas está disponível. O argônio pode ser usado dessa forma, bastando encher o meio de reação com um recipiente e, opcionalmente, fazer vácuo na extremidade do condensador e encher novamente com argônio.
Attachments
- Language
- 🇪🇸
- Joined
- Jul 11, 2023
- Messages
- 12
- Reaction score
- 5
- Points
- 3
G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,991
- Solutions
- 3
- Reaction score
- 3,380
- Points
- 113
- Deals
- 1
- Language
- 🇺🇸
- Joined
- Dec 21, 2022
- Messages
- 24
- Reaction score
- 5
- Points
- 3
O éster metílico do ácido lisérgico poderia ser usado no lugar da ergotamina?
A condição básica hidrolisaria o éster metílico?
Se isso funcionar, o restante do procedimento seria o mesmo.
O uso do lisergato de metila tornaria a síntese de LSD realmente fácil de usar e barata.
Agradecemos qualquer orientação
A condição básica hidrolisaria o éster metílico?
Se isso funcionar, o restante do procedimento seria o mesmo.
O uso do lisergato de metila tornaria a síntese de LSD realmente fácil de usar e barata.
Agradecemos qualquer orientação
- Language
- 🇬🇧
- Joined
- Jan 25, 2022
- Messages
- 87
- Reaction score
- 73
- Points
- 18
Sim, você pode hidrolisar sob as mesmas condições para clivar os grupos adicionais
- Joined
- May 10, 2023
- Messages
- 17
- Reaction score
- 10
- Points
- 3
@G.Patton
Olá, o tartarato de ergotamina pode ser trocado por "Dihydro Ergotamine Mesylate --> 6190-39-2"?
Ajustando as proporções molares e outras coisas (obviamente).
Talvez obtivéssemos o mesilato de dietilamida do ácido lisérgico (LSD)? Ou estou errado?
Olá, o tartarato de ergotamina pode ser trocado por "Dihydro Ergotamine Mesylate --> 6190-39-2"?
Ajustando as proporções molares e outras coisas (obviamente).
Talvez obtivéssemos o mesilato de dietilamida do ácido lisérgico (LSD)? Ou estou errado?
G.Patton
Expert
- Joined
- Jul 5, 2021
- Messages
- 2,991
- Solutions
- 3
- Reaction score
- 3,380
- Points
- 113
- Deals
- 1
Sim, você pode
Você não obterá mesilato de LSD se apenas substituir o sal de ergotamina. Você precisa trocar o ácido na última etapa. Não tenho certeza se é possível obter o mesilato de LSD na prática.
Você não obterá mesilato de LSD se apenas substituir o sal de ergotamina. Você precisa trocar o ácido na última etapa. Não tenho certeza se é possível obter o mesilato de LSD na prática.
- Language
- 🇬🇧
- Joined
- Jan 15, 2023
- Messages
- 609
- Reaction score
- 353
- Points
- 63
- Language
- 🇬🇧
- Joined
- Sep 26, 2023
- Messages
- 5
- Reaction score
- 1
- Points
- 3
Olá,
Que solvente você usaria para recristalizar o hidrato de ácido D-lisérgico? O acetato de etila seria adequado?
Também tenho uma pergunta semelhante para a recristalização do tartarato de dietilamida de ácido lisérgico, se houver algum outro solvente no qual o sal teria solubilidade semelhante à do metanol?
Muito obrigado
Que solvente você usaria para recristalizar o hidrato de ácido D-lisérgico? O acetato de etila seria adequado?
Também tenho uma pergunta semelhante para a recristalização do tartarato de dietilamida de ácido lisérgico, se houver algum outro solvente no qual o sal teria solubilidade semelhante à do metanol?
Muito obrigado
E para o ácido d-tartárico, o CAS correto é 147-71-7 ou 87-69-4? Muito obrigado
About Us
Our team brings together the best specialists from different fields.
We are ready to share our experience, discuss difficult issues and find new solutions.