- Joined
- May 23, 2023
- Messages
- 6
- Reaction score
- 4
- Points
- 3
Introdução:
Um determinado fornecedor on-line (que não deve ser nomeado) parece estar sugerindo uma rota "nova" para as fenetilaminas.
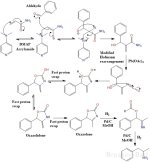
A reação de aldeído para amina ocorre em três etapas distintas:
1) Primeiro, uma reação de Baylis-Hillman é usada para acoplar um aldeído a rila com acrilamida usando uma base de amina terciária, como
DMAP (4-dimetilaminopiridina) ou DABCO/TEDA (trietilenodiamina).
A acrilamida é um produto químico industrial usado na fabricação de polímeros e também está associada a alimentos queimados.
2) Em seguida, é realizado um rearranjo de Hofmann modificado.
Diferentemente da reação de Hofmann "regular", é importante observar que o produto final não é uma amina.
O isocianato intermediário não sofrerá hidrólise pela água para formar o ácido carbâmico, que é então descarboxilado para dar a amina.
Em vez disso, o álcool benzílico formado na etapa 1 passará por uma ciclização intramolecular, formando um anel de carbamato de 5 membros (que é tanto um éster quanto uma amida).
Ocorre uma série de trocas rápidas de prótons que, em seguida, isomerizam a oxazolidona não conjugada na oxazolona conjugada mais estável.
3) Na etapa final, é realizada uma redução de paládio sobre carbono usando 3 equivalentes de gás hidrogênio.
O primeiro equivalente de hidrogênio é usado para quebrar o anel de oxazolona, produzindo um éster de formiato e uma imina que são então
reduzidos pelos 2 equivalentes de hidrogênio restantes. A amina desejada é formada junto com o ácido fórmico como subproduto.
É possível que essa reação já seja conhecida no cenário clandestino(embora seja um segredo muito bem guardado),
Entretanto, ouso dizer que a reação é "nova" porque nunca ouvi nenhuma discussão/relato documentado dessa reação em nenhum fórum semelhante ou na literatura.
O mecanismo exato da reação é desconhecido, embora eu tenha feito minha melhor tentativa de elucidar o mecanismo.
Se você discordar das minhas suposições mecanicistas, explique suas ideias/críticas com argumentos sólidos nos comentários.
Seu feedback será muito apreciado.
Evidência da literatura:
[1] Pedro Molina, Alberto Tarraga, no livro "Comprehensive Organic Functional Group Transformations", 1995, ISBN: 978-0-08-044705-6
" Descobriu-se que o tetra-acetato de chumbo em piridina fornece um procedimento suave para efetuar um rearranjo rápido, de alto rendimento e semelhante ao de Hofmann de amidas primárias β-hidroxi para 2-oxazolidinonas, por meio do β-hidroxiisocianato correspondente"
[2] Shinobu Hazama, S. Ichikawa, Fumihiro Yonebayashi, no Japanese Journal of Forensic Science and Technology, 2008, DOI: 10.3408/jafst.13.67
"Desenvolvemos um método novo e conveniente para a síntese de levo-metanfetamina usando d-norefedrina (d-NE) como material de partida. d-NE foi tratado com 1,1-carbonildiimidazol para produzir o carbamato cíclico correspondente, e o produto foi tratado com hidreto de sódio e iodometano para formar um derivado de amina mono-N-metilado, que foi tratado com paládio em carbono ativado em atmosfera de hidrogênio para redução catalítica. Após a adição de cloreto de hidrogênio (HCl) aquoso, o l-MA foi obtido como seu sal HCl (rendimento total de 58%)"
Mecanismo de literatura/esquema de reação:

Esquema de reação/mecanismoproposto (hipotético):

Perguntas que ainda precisam ser respondidas:
1) Quais são as condições exatas da reação (temperatura, concentração, tempo de reação etc.) e os reagentes necessários para que essa reação funcione?
2) Quais são as condições de trabalho necessárias para purificar cada intermediário?
3) Não tenho certeza da quantidade de testes e desenvolvimento iterativo que ocorre neste fórum.
Alguém no fórum com um espaço de laboratório adequado está disposto a testar e dar feedback? Não tenho os meios para testar isso sozinho.
4) A reação é mecanicamente sólida? A reação existe de fato ou eu simplesmente tirei isso da minha cabeça?
5) Já existe um procedimento para essa reação? Se sim, onde posso encontrá-lo?
6) O esquema da reação pode ser modificado para incluir também a síntese de derivados n-metilados (semelhante ao exemplo que mostrei na literatura)?
7) Reagentes alternativos ao tetra-acetato de chumbo podem ser usados para induzir a etapa de ciclização? Acho que o
hipoclorito não funcionaria porque também oxidaria o álcool benzílico em cetona/fenona.
8) Outras aminas terciárias, como a trietilamina, podem ser usadas além do DMAP e do DABCO?
9) Há alguma reação colateral digna de nota que diminuiria a pureza do produto final?
10) A redução produzirá uma amina racêmica ou favorecerá preferencialmente um estereoisômero em detrimento do outro?
Esta é minha primeira postagem neste fórum, portanto, não tenho certeza do feedback que posso esperar.
Obrigado pela leitura.
Um determinado fornecedor on-line (que não deve ser nomeado) parece estar sugerindo uma rota "nova" para as fenetilaminas.
A reação de aldeído para amina ocorre em três etapas distintas:
1) Primeiro, uma reação de Baylis-Hillman é usada para acoplar um aldeído a rila com acrilamida usando uma base de amina terciária, como
DMAP (4-dimetilaminopiridina) ou DABCO/TEDA (trietilenodiamina).
A acrilamida é um produto químico industrial usado na fabricação de polímeros e também está associada a alimentos queimados.
2) Em seguida, é realizado um rearranjo de Hofmann modificado.
Diferentemente da reação de Hofmann "regular", é importante observar que o produto final não é uma amina.
O isocianato intermediário não sofrerá hidrólise pela água para formar o ácido carbâmico, que é então descarboxilado para dar a amina.
Em vez disso, o álcool benzílico formado na etapa 1 passará por uma ciclização intramolecular, formando um anel de carbamato de 5 membros (que é tanto um éster quanto uma amida).
Ocorre uma série de trocas rápidas de prótons que, em seguida, isomerizam a oxazolidona não conjugada na oxazolona conjugada mais estável.
3) Na etapa final, é realizada uma redução de paládio sobre carbono usando 3 equivalentes de gás hidrogênio.
O primeiro equivalente de hidrogênio é usado para quebrar o anel de oxazolona, produzindo um éster de formiato e uma imina que são então
reduzidos pelos 2 equivalentes de hidrogênio restantes. A amina desejada é formada junto com o ácido fórmico como subproduto.
É possível que essa reação já seja conhecida no cenário clandestino(embora seja um segredo muito bem guardado),
Entretanto, ouso dizer que a reação é "nova" porque nunca ouvi nenhuma discussão/relato documentado dessa reação em nenhum fórum semelhante ou na literatura.
O mecanismo exato da reação é desconhecido, embora eu tenha feito minha melhor tentativa de elucidar o mecanismo.
Se você discordar das minhas suposições mecanicistas, explique suas ideias/críticas com argumentos sólidos nos comentários.
Seu feedback será muito apreciado.
Evidência da literatura:
[1] Pedro Molina, Alberto Tarraga, no livro "Comprehensive Organic Functional Group Transformations", 1995, ISBN: 978-0-08-044705-6
" Descobriu-se que o tetra-acetato de chumbo em piridina fornece um procedimento suave para efetuar um rearranjo rápido, de alto rendimento e semelhante ao de Hofmann de amidas primárias β-hidroxi para 2-oxazolidinonas, por meio do β-hidroxiisocianato correspondente"
[2] Shinobu Hazama, S. Ichikawa, Fumihiro Yonebayashi, no Japanese Journal of Forensic Science and Technology, 2008, DOI: 10.3408/jafst.13.67
"Desenvolvemos um método novo e conveniente para a síntese de levo-metanfetamina usando d-norefedrina (d-NE) como material de partida. d-NE foi tratado com 1,1-carbonildiimidazol para produzir o carbamato cíclico correspondente, e o produto foi tratado com hidreto de sódio e iodometano para formar um derivado de amina mono-N-metilado, que foi tratado com paládio em carbono ativado em atmosfera de hidrogênio para redução catalítica. Após a adição de cloreto de hidrogênio (HCl) aquoso, o l-MA foi obtido como seu sal HCl (rendimento total de 58%)"
Mecanismo de literatura/esquema de reação:
Esquema de reação/mecanismoproposto (hipotético):
Perguntas que ainda precisam ser respondidas:
1) Quais são as condições exatas da reação (temperatura, concentração, tempo de reação etc.) e os reagentes necessários para que essa reação funcione?
2) Quais são as condições de trabalho necessárias para purificar cada intermediário?
3) Não tenho certeza da quantidade de testes e desenvolvimento iterativo que ocorre neste fórum.
Alguém no fórum com um espaço de laboratório adequado está disposto a testar e dar feedback? Não tenho os meios para testar isso sozinho.
4) A reação é mecanicamente sólida? A reação existe de fato ou eu simplesmente tirei isso da minha cabeça?
5) Já existe um procedimento para essa reação? Se sim, onde posso encontrá-lo?
6) O esquema da reação pode ser modificado para incluir também a síntese de derivados n-metilados (semelhante ao exemplo que mostrei na literatura)?
7) Reagentes alternativos ao tetra-acetato de chumbo podem ser usados para induzir a etapa de ciclização? Acho que o
hipoclorito não funcionaria porque também oxidaria o álcool benzílico em cetona/fenona.
8) Outras aminas terciárias, como a trietilamina, podem ser usadas além do DMAP e do DABCO?
9) Há alguma reação colateral digna de nota que diminuiria a pureza do produto final?
10) A redução produzirá uma amina racêmica ou favorecerá preferencialmente um estereoisômero em detrimento do outro?
Esta é minha primeira postagem neste fórum, portanto, não tenho certeza do feedback que posso esperar.
Obrigado pela leitura.
Attachments
Last edited: