- Language
- 🇺🇸
- Joined
- Nov 16, 2023
- Messages
- 373
- Reaction score
- 290
- Points
- 63
Czy ktoś może mi pomóc zrozumieć, czy możliwe jest użycie generycznych inhalatorów do nosa, które zawierają "lewmetamfetaminę 50 mg", aby uzyskać d-met.
https://bbgate.com/threads/methamphetamine-synthesis-vicks-inhaler.4974/#post-46343 Czy te instrukcje będą działać w teorii?
Czy też muszę użyć powyższej racemizacji i rozdzielczości dostarczonej przez Amphibian? Lub 41Dxflatline itp?
https://bbgate.com/threads/methamphetamine-synthesis-vicks-inhaler.4974/#post-46343 Czy te instrukcje będą działać w teorii?
Czy też muszę użyć powyższej racemizacji i rozdzielczości dostarczonej przez Amphibian? Lub 41Dxflatline itp?
Chociaż to by zadziałało... niektóre z tych chemikaliów są trudne do zdobycia lub mogą być niebezpieczne, tak jak moja nazwa użytkownika, zamiast tego powinieneś użyć naproksenu i skorzystać z naproksenu z NASID Naproxen. Poniżej zamieściłem pełny przewodnik
↑View previous replies…
- By azides
Tłumaczenie zostało opublikowane wcześniej, ale jeszcze raz
Jest to ....
Badanie mechanizmu rozdzielczości optycznej N-metyloamfetaminy poprzez tworzenie soli diastereoizomerycznej metodą Pope-Peachey, jak omówiono później w retorcie
https://sci-hub.wf/10.1016/s0957-4166(00)86170-4
https://www.sciencedirect.com/science/article/abs/pii/S0957416600861704
referencje i uwagi
I.) Newman,P. Optical Resolution Procedures for Chemical Compounds, vols.l-3, Optical Resolution Information
Catre, Manhattan College, Nowy Jork, 1978-84;
2.) Jacques,J.; Collet,A.; Wilen,SH. Enantiomers, Racemates and Resolutions, Wiley and Sons, New York,
1981,378.p.
3.) Fogassy,E.; hs,M.; Faigl,F ; Rohonczy,J, Ecsery,Z. J.Chem.Soc.Perkin Trans.2, 1986, 1881.
4.) Pope,W.J.; Peachey,S.J. J.Chem.Soc.,1899,75,1066
5.) 7,84 g (0,0525 mol) racemicznej N-metyloamfetaminy i 9,73 g (0,0525 mol) racemicznego chlorowodorku N-
metyloamfetaminy rozpuszczono w 70 ml etanolu abs., a 7,91 g (0,0525 mol) kwasu R,R-
kwasu tartazynowego w 56 ml etanolu abs. Oba roztwory podstawowe podzielono na piętnaście porcji objętościowych za pomocą biurety
i poddano reakcji w temperaturze 22 + 1 ° C Mieszaniny pozostawiono w stanie niezakłóconym przez 15, 90 minut i 5, 24, 1 IS
godzin, po czym osady przefiltrowano i wysuszono. Z 0,4 g każdej soli uwolniono zasadę za pomocą ccNaOH
i ekstrahowano z fazy wodnej dikblorometanem.
6.) Wszystkie eksperymenty przeprowadzono przy tym samym stole roboczym w temperaturze pokojowej 2Ul'C. Roztwory podstawowe
racematu i środka rozdzielającego zostały użyte w celu uniknięcia błędu pomiaru masy. Wszystkie używane kolby
miały identyczny rozmiar i kształt
7.)Zawartość winianu i chlorowodorku soli oznaczono metodą potencjometryczną za pomocą automatycznego titratora RADIOMETER-
85 TTT przy użyciu 0,1 N NaOH i 0,1 N AgNO.
8.) Obroty właściwe mierzono za pomocą polarhametru Perkin Elmer 241. Rotacja właściwa
optycznie czystej R-N-metyloamfetaminy wynosi [a]: - -18.90 (c 0.1, IN HCI).
9.) Sole nie zostały przemyte podczas filtrowania. Niewielka ilość chlorowodorku znaleziona w solach prawdopodobnie pochodzi
z ługu macierzystego przyklejonego i wysuszonego do powierzchni soli.
10.) Jest to zgodne z wynikami3, że R-l II jest bardziej stabilną solą niż S-1.11
Jeśli chcesz więcej, możesz również przeczytać poniższą ripostę, wszystko powinno być w https://sci-hub.wf w dużej mierze, chociaż
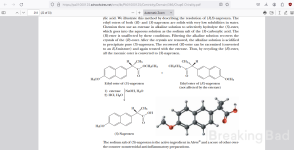
Zamiast tego w tym skręcie użyto tylko pół ekwiwalentu chiralnej aminy. W jej miejsce stosuje się połowę równoważnika tańszej, optycznie nieaktywnej zasady aminowej. To nie tylko sprawia, że proces jest tańszy, ale skutkuje bardziej dramatyczną różnicą w rozpuszczalności. Sprzężona zasada pożądanego (d)-(+)-enancjomeru krystalizuje ze sprzężonym kwasem chiralnej aminy z wysoką selektywnością. Pozostawia to w roztworze bardziej rozpuszczalny produkt soli (l)-(-)-naproksenu i achiralnej aminy.
Jest to ....
Badanie mechanizmu rozdzielczości optycznej N-metyloamfetaminy poprzez tworzenie soli diastereoizomerycznej metodą Pope-Peachey, jak omówiono później w retorcie
https://sci-hub.wf/10.1016/s0957-4166(00)86170-4
https://www.sciencedirect.com/science/article/abs/pii/S0957416600861704
referencje i uwagi
I.) Newman,P. Optical Resolution Procedures for Chemical Compounds, vols.l-3, Optical Resolution Information
Catre, Manhattan College, Nowy Jork, 1978-84;
2.) Jacques,J.; Collet,A.; Wilen,SH. Enantiomers, Racemates and Resolutions, Wiley and Sons, New York,
1981,378.p.
3.) Fogassy,E.; hs,M.; Faigl,F ; Rohonczy,J, Ecsery,Z. J.Chem.Soc.Perkin Trans.2, 1986, 1881.
4.) Pope,W.J.; Peachey,S.J. J.Chem.Soc.,1899,75,1066
5.) 7,84 g (0,0525 mol) racemicznej N-metyloamfetaminy i 9,73 g (0,0525 mol) racemicznego chlorowodorku N-
metyloamfetaminy rozpuszczono w 70 ml etanolu abs., a 7,91 g (0,0525 mol) kwasu R,R-
kwasu tartazynowego w 56 ml etanolu abs. Oba roztwory podstawowe podzielono na piętnaście porcji objętościowych za pomocą biurety
i poddano reakcji w temperaturze 22 + 1 ° C Mieszaniny pozostawiono w stanie niezakłóconym przez 15, 90 minut i 5, 24, 1 IS
godzin, po czym osady przefiltrowano i wysuszono. Z 0,4 g każdej soli uwolniono zasadę za pomocą ccNaOH
i ekstrahowano z fazy wodnej dikblorometanem.
6.) Wszystkie eksperymenty przeprowadzono przy tym samym stole roboczym w temperaturze pokojowej 2Ul'C. Roztwory podstawowe
racematu i środka rozdzielającego zostały użyte w celu uniknięcia błędu pomiaru masy. Wszystkie używane kolby
miały identyczny rozmiar i kształt
7.)Zawartość winianu i chlorowodorku soli oznaczono metodą potencjometryczną za pomocą automatycznego titratora RADIOMETER-
85 TTT przy użyciu 0,1 N NaOH i 0,1 N AgNO.
8.) Obroty właściwe mierzono za pomocą polarhametru Perkin Elmer 241. Rotacja właściwa
optycznie czystej R-N-metyloamfetaminy wynosi [a]: - -18.90 (c 0.1, IN HCI).
9.) Sole nie zostały przemyte podczas filtrowania. Niewielka ilość chlorowodorku znaleziona w solach prawdopodobnie pochodzi
z ługu macierzystego przyklejonego i wysuszonego do powierzchni soli.
10.) Jest to zgodne z wynikami3, że R-l II jest bardziej stabilną solą niż S-1.11
Jeśli chcesz więcej, możesz również przeczytać poniższą ripostę, wszystko powinno być w https://sci-hub.wf w dużej mierze, chociaż
Zamiast tego w tym skręcie użyto tylko pół ekwiwalentu chiralnej aminy. W jej miejsce stosuje się połowę równoważnika tańszej, optycznie nieaktywnej zasady aminowej. To nie tylko sprawia, że proces jest tańszy, ale skutkuje bardziej dramatyczną różnicą w rozpuszczalności. Sprzężona zasada pożądanego (d)-(+)-enancjomeru krystalizuje ze sprzężonym kwasem chiralnej aminy z wysoką selektywnością. Pozostawia to w roztworze bardziej rozpuszczalny produkt soli (l)-(-)-naproksenu i achiralnej aminy.
Last edited: